
- •3.Глутатионовая защита, которая включает участие глутатиона, а так же ферментов глутатионтрансферазы, глутатионредуктазы и
- •4. Пептидная конъюгация – связывание с аминокислотой глицин и другими аминокислотами. Характерно для
- •5. Тиоционатная конъюгация - для
- •Наиболее существенными процессами в биотрансформации считается:
- •Клиническая оценка процесса биотрансформации.
- •2 фаза оценивается в основном по глутатионовой защите:
- •ПУТИ ОБЕЗВРЕЖИВАНИЯ ЭТАНОЛА В ПЕЧЕНИ
- •Цитохром Р450-зависимая микросомальная
- •Окисление этанола каталазой
- •РЕАКЦИИ БИОАКТИВАЦИИ КСЕНОБИОТИКОВ
- •ВЛИЯНИЕ КСЕНОБИОТИКОВ НА АКТИВНОСТЬ
- •ФАКТОРЫ, ВЛИЯЮЩИЕ НА
- •ФАКТОРЫ, ВЛИЯЮЩИЕ НА АКТИВНОСТЬ
- •БИОХИМИЯ НЕРВНОЙ ТКАНИ
- •Нейрохимия – раздел биохимии, изучающий химический состав нервной ткани и особенности ее метаболизма
- •История развития нейрохимии
- •Городисская Г.Я.
- •Особенности мозга
- •Химический состав серого и белого вещества мозга
- •Липиды мозга (% )
- •Особенности липидов
- •Функции липидов
- •Brain lipids as electric insulators
- •Белки головного мозга
- •Сократительные белки и белки цитоскелета
- •Нейроспецифические глиальные
- •Нейроспецифические
- •Секретируемые белки
- •Белки миелина
- •Пептиды мозга: либерины
- •Пептиды мозга: статины
- •Пептиды мозга: энкефалины и
- •Пептиды мозга: гормоны аденогипофиза
- •Пептиды мозга: гормоны
- •Пептиды мозга: панкреатические
- •индуцирующий пептид (ДСИП, дельтаран-
- •Пептиды
- •Пептиды мозга: субстанция Р
- •Другие пептиды мозга
- •Аминокислоты мозга
- •Аминокислоты мозга
- •Углеводы мозга
- •Особенности метаболизма
- •Особенности использования энергии
- •ИТОГ
3.Глутатионовая защита, которая включает участие глутатиона, а так же ферментов глутатионтрансферазы, глутатионредуктазы и глутатионпероксидазы. ГТ играют важную роль в инактивации собственных метаболитов: стероидных гормонов, простагландинов, билирубина, жёлчных кислот, продуктов ПОЛ.
•R + GSH → GSRH
•Коньюгация субстрата
(R) c глутатионом
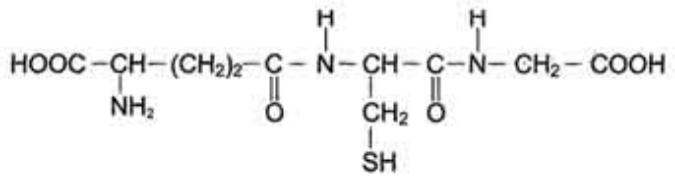
Глутатион (GSH) трипептид Глу-Цис-Гли
Глутатион конъюгирует с обезвреживаемым веществом с участием глутатионтрансферазы. Это наиболее мощный путь детоксикации.
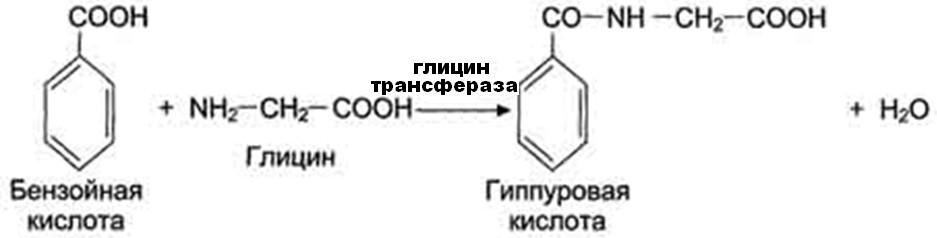
4. Пептидная конъюгация – связывание с аминокислотой глицин и другими аминокислотами. Характерно для ароматических карбоновых кислот (бензойная к-та).
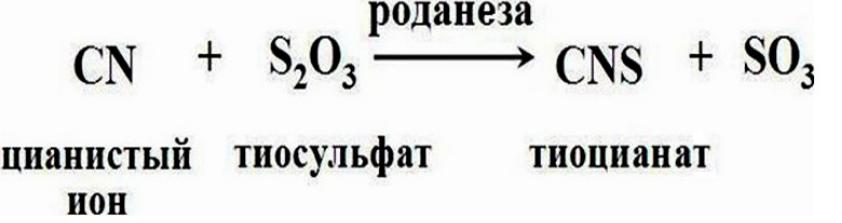
5. Тиоционатная конъюгация - для
обезвреживания эндогенного цианистого иона;
Наиболее существенными процессами в биотрансформации считается:
•Глюкуронидная конъюгация;
•Сульфатная конъюгация;
•Глутатионовая конъюгация
Клиническая оценка процесса биотрансформации.
1 фаза оценивается по:
-Антипириновая проба на Цитохром
Р450;
-АДГ-активность как тест на латентную недостаточность печени (у детей);
2 фаза оценивается в основном по глутатионовой защите:
-Содержание глутатиона в его окисленной и восстановленной форме;
-Активность глутатионтрансферазы;
-Содержание глутатиона совместно со всеми ферментами глутатионовой защиты
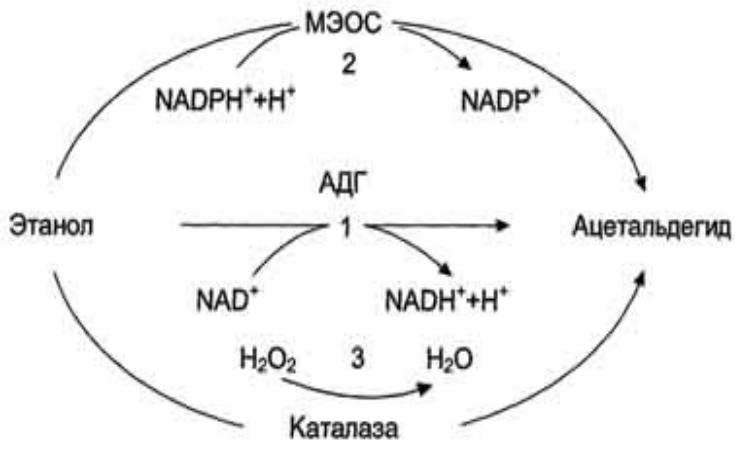
ПУТИ ОБЕЗВРЕЖИВАНИЯ ЭТАНОЛА В ПЕЧЕНИ
1- окисление этанола NAD+- зависимой алкогольдегидрогеназой (АДГ); 2 - МЭОС - микросомальная этанолокисляющая система; 3 - окисление этанола каталазой
Цитохром Р450-зависимая микросомальная
этанолокисляющая система (МЭОС)
локализована в мембране гладкого ЭР гепатоцитов. МЭОС играет незначительную роль в метаболизме небольших количеств алкоголя, но индуцируется этанолом, барбитуратами и приобретает существенное значение при злоупотреблении ими. При хроническом алкоголизме окисление этанола ускоряется на 50 - 70% за счёт гипертрофии ЭР и индукции цитохрома Р450 II E1.
С2Н5ОН + NADPH + Н+ +О2 → СН3СНО + NADP+ +2Н2О.
Окисление этанола каталазой
Второстепенную роль в окислении этанола играет каталаза, находящаяся в пероксисомах клеток печени. Этот фермент расщепляет примерно 2% этанола, но при этом утилизирует пероксид водорода.
СН3СН2ОН + Н2О2 → СН3СНО + 2Н2О.
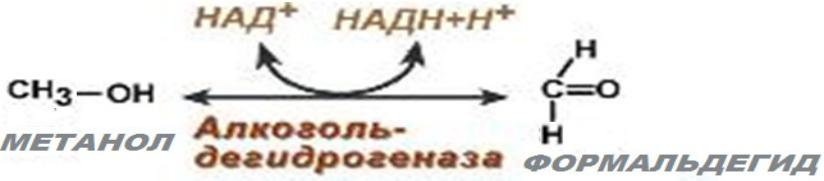
РЕАКЦИИ БИОАКТИВАЦИИ КСЕНОБИОТИКОВ
Реакции биотрансформации, в которых образуются продукты, имеющие большую токсичность по сравнению с исходным ксенобиотиком, называют реакциями БИОАКТИВАЦИИ
• - тиофосфат, нейротоксичность основана на взаимодействии ферментом ацетилхолинэстеразой. Сродство этого фермента к параоксону во много раз выше, чем к исходному соединению- паратиону.
•Тяжесть отравления этиленгликолем прямо пропорциональна степени окисления его до щавелевой кислоты. В ходе биопревращения щавелевая кислота, способная повреждать паренхиматозные органы и,
в частности, почки.
