
- •Полиморфные превращения в металлах.
- •Серые чугуны. Структура, свойства, область применения.
- •Ковкие чугуны. Структура, свойства, область применения.
- •Высокопрочные чугуны. Структура, свойства, область применения.
- •22. Классификация, маркировка и применение углеродистых сталей.
- •Маркировка сталей
- •23. Структурные классы легированных сталей. Влияние легирующих элементов на полиморфизм железа.
- •24.Маркировка легированных сталей.
- •Нагрев при термообработке. Окисление и обезуглероживание поверхности стали.
- •Цементация. Термообработка стали после цементации.
1. Материаловедение - научная дисциплина, изучающая связь между химическим составом, структурой, свойствами материалов, а также изменение этих свойств при различных внешних воздействиях.
Все металлы, затвердевающие в нормальных условиях, представляют собой кристаллические вещества, то есть укладка атомов в них характеризуется определенным порядком – периодичностью, как по различным направлениям, так и по различным плоскостям. Этот порядок определяется понятием кристаллическая решетка. Другими словами, кристаллическая решетка это воображаемая пространственная решетка, в узлах которой располагаются частицы, образующие твердое тело.
Элементарная
ячейка –
элемент объема из минимального числа
атомов, многократным переносом которого
в пространстве можно построить весь
кристалл. Элементарная ячейка характеризует
особенности строения кристалла. Основными
параметрами кристалла являются:![]()
размеры ребер элементарной ячейки. a, b, c – периоды решетки – расстояния между центрами ближайших атомов. В одном направлении выдерживаются строго определенными.
).,, углы между осями (
координационное число (К) указывает на число атомов, расположенных на ближайшем одинаковом расстоянии от любого атома в решетке.
базис решетки - количество атомов, приходящихся на одну элементарную ячейку решетки.
плотность упаковки атомов в кристаллической решетке – объем, занятый атомами, которые условно рассматриваются как жесткие шары. Ее определяют как отношение объема, занятого атомами к объему ячейки (для объемно-центрированной кубической решетки – 0,68, для гранецентрированной кубической решетки – 0,74)
Различают 7 форм кристаллических решеток. По типу расположения частиц - 14 типов (решетки Браве).
Три типа наиболее распространенных кристаллических решеток.
Объемно-центрированная
кубическая (ОЦК) атомы
располагаются в вершинах куба и в его
центре (V, W, Ti, Fe,
щелочные, щелочноземельные металлы)![]()
Гранецентрированная кубическая (ГЦК) атомы рассполагаются в вершинах куба и по центру каждой из 6 граней (Ag, Au, Fe)
Гексагональная, в основании которой лежит шестиугольник. (Ti,Zn, Be, Mn)
простая – атомы располагаются в вершинах ячейки и по центру 2 оснований (углерод в виде графита);
плотноупакованная (ГПУ) (если с/а=1,633) – имеется 3 дополнительных атома в средней плоскости (цинк).
Из жидкого расплава можно вырастить монокристалл. Их обычно используют в лабораториях для изучения свойств того или иного вещества.
Металлы и сплавы, полученные в обычных условиях, состоят из большого количества кристаллов, то есть, имеют поликристаллическое строение. Эти кристаллы называются зернами. Они имеют неправильную форму и различно ориентированы в пространстве. Каждое зерно имеет свою ориентировку кристаллической решетки, отличную от ориентировки соседних зерен, вследствие чего свойства реальных металлов усредняются, и явления анизотропии не наблюдается
В кристаллической решетке реальных металлов имеются различные дефекты (несовершенства), которые нарушают связи между атомами и оказывают влияние на свойства металлов. Различают следующие структурные несовершенства:
точечные – малые во всех трех измерениях;
линейные – малые в двух измерениях и сколь угодно протяженные в третьем;
поверхностные – малые в одном измерении.
Вакансия – отсутствие атомов в узлах кристаллической решетки, «дырки», которые образовались в результате различных причин. Концентрация вакансий в значительной степени определяется температурой тела. Перемещаясь по кристаллу, одиночные вакансии могут встречаться. И объединяться в дивакансии. Скопление многих вакансий может привести к образованию пор и пустот.
Дислоцированный атом – это атом, вышедший из узла решетки и занявший место в междоузлие. Концентрация дислоцированных атомов значительно меньше, чем вакансий, так как для их образования требуются существенные затраты энергии. При этом на месте переместившегося атома образуется вакансия.
Примесные
атомы всегда присутствуют в металле,
так как практически невозможно выплавить
химически чистый металл. Они могут иметь
размеры больше или меньше размеров
основных атомов и располагаются в узлах
решетки или междоузлиях. 
Линейные дефекты:
Дислокация – это дефекты кристаллического строения, представляющие собой линии, вдоль и вблизи которых нарушено характерное для кристалла правильное расположение атомных плоскостей.
Краевая дислокация представляет собой линию, вдоль которой обрывается внутри кристалла край “лишней“ полуплоскости
Неполная плоскость называется экстраплоскостью..
Большинство дислокаций образуются путем сдвигового механизма. Ее образование можно описать при помощи следующей операции. Надрезать кристалл по плоскости АВСD, сдвинуть нижнюю часть относительно верхней на один период решетки в направлении, перпендикулярном АВ, а затем вновь сблизить атомы на краях разреза внизу.
Наибольшие
искажения в расположении атомов в
кристалле имеют место вблизи нижнего
края экстраплоскости. Вправо и влево
от края экстраплоскости эти искажения
малы (несколько периодов решетки), а
вдоль края экстраплоскости искажения
простираются через весь кристалл и
могут быть очень велики (тысячи периодов
решетки).![]()
Если
экстраплоскость находится в верхней
части кристалла, то краевая дислокация
– положительная, если в нижней, то –
отрицательная. Дислокации одного знака
отталкиваются, а противоположные
притягиваются.
В процессе кристаллизации атомы вещества, выпадающие из пара или раствора, легко присоединяются к ступеньке, что приводит к спиральному механизму роста кристалла.
Линии дислокаций не могут обрываться внутри кристалла, они должны либо быть замкнутыми, образуя петлю, либо разветвляться на несколько дислокаций, либо выходить на поверхность кристалла.
Дислокационная структура материала характеризуется плотностью дислокаций.
Плотность
дислокацийв
кристалле определяется как среднее
число линий дислокаций, пересекающих
внутри тела площадку площадью 1 м2,
или как суммарная длина линий дислокаций
в объеме 1 м3![]()
Плотность дислокаций изменяется в широких пределах и зависит от состояния материала. После тщательного отжига плотность дислокаций составляет 105…107 м-2, в кристаллах с сильно деформированной кристаллической решеткой плотность дислокаций достигает 1015…10 16 м –2.
Плотность
дислокации в значительной мере определяет
пластичность и прочность материала.
Минимальная прочность определяется критической плотностью дислокаций
Если плотность меньше значения а, то сопротивление деформированию резко возрастает, а прочность приближается к теоретической. Повышение прочности достигается созданием металла с бездефектной структурой, а также повышением плотности дислокаций, затрудняющим их движение.
Поверхностные дефекты:
Высоко- и малоугловые границы.
Граница
между зернами - поверхностный деффект,
в котором угол разориентировки между
соседними кристалическими решетками
составляет 5-10 градусов (высокоугловая
граница)![]()
Угол разориентировки между отдельными блоками менее 5 градусов(малоугловая граница). Пространство между блоками - совокупность линейных дислокаций.
Поверхностные деффекты оказывают сильное влияние на механические свойства.
т=0+kd-1/2 - предел текучести (d - размер зерна).
4. Процесс
кристаллизации металлов.
Кристаллизацией называется переход из жидкого в твердое состояние с образованием кристаллических решеток или кристаллов. В реальных металлических телах кристаллизация расплавов заканчивается образованием структуры сложно переплетенных кристаллов - дендритов. Их морфология определяет свойства материалов. При образовании кристаллов их развитие идет в основном в направлении, перпендикулярном плоскостям с максимальной плотностью упаковки атомов. Это приводит к тому, что первоначально образуются длинные ветви, так называемые оси первого порядка. Одновременно с удлинением осей первого порядка на их ребрах зарождаются и растут перпендикулярные к ним такие же ветви второго порядка. в свою очередь на них растут оси третьего порядка и т.д. Образуются кристаллы древовидной - дендритной формы.
Процесс кристаллизации происходит в два этапа: образование зародышей кристаллов; рост образовавшихся кристаллов.
В реальных металлах центрами кристаллизации являются тугоплавкие частицы и стенки литейной формы.
В чистых металлах центрами кристаллизации служат области с дальним порядком расположения атомов (кластеры), т.е. их строение близко к строению кристаллической решетки.
Чем больше скорость охлаждения (степень переохлаждения), тем более мелкозернистая структура образуется. Если скорость охлаждения порядка 105-106 градусов в секунду, получается аморфная структура.
Полиморфные превращения в металлах.
Металлы и сплавы в зависимости от температуры могут сосуществовать в разных кристаллических формах, или в разных модификациях. При полиморфном превращении одна кристаллическая решетка сменяет другую. Полиморфное превращение происходит в том случае, если при данной температуре может существовать металл с иной кристаллической решеткой и меньшим уровнем свободной энергии. Показана кривая охлаждения чистого железа и полиморфные превращения в металле.
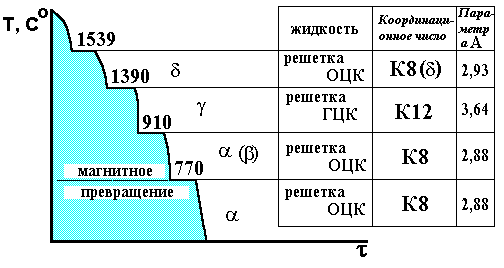
Полиморфное превращение - кристаллизационный процесс и осуществляется путем образования зародышей и последующего их роста. Образование зародышей идет с соблюдением принципа структурного и размерного соответствия. Рост зерен новой фазы происходит путем неупорядоченных, взаимно не связанных переходов отдельных атомов (группы атомов) через мажфазную границу. В результате граница новых зерен передвигается в сторону исходных, поглощая их. Зародыши новой фазы возникают по границам старых зерен или в зонах с повышенным уровнем свободной энергии.
Вновь образующиеся кристаллы закономерно ориентированы по отношению к кристаллам исходной модификации. В результате полиморфного превращения образуются новые зерна, имеющие другой размер и форму. Происходит скачкообразное изменение свойств материала. Полиморфное превращение также называют перекристаллизацией. Если нагрев металла проведен до температуры, немного превышающей температуру полиморфного превращения (критической точки), получается очень мелкое зерно. Это явление используется в практике термической обработки металлов.

Кривая ликвидуса - ABCD; кривая солидуса - AHIECF; углерод понижает температуру плавления железа (линия ABC); - железо также понижает температуру плавления углерода (и Fe3C) (V- образная форма диаграммы, D - C); - температура А4 (линия NH) растет c увеличением содержания углерода (линия N - I); - температура А3 (линия GOS) уменьшается с увеличением содержания углерода; - область - твердого раствора расширяется с увеличением содержания углерода.
Э в т е к т о и д н ы й сплав: точка S = 0.83 % С = перлит.
Д о э в т е к т о и д н ы е сплавы: от точки Р к точке S = 0.02 до 0.83 % С = - Fe + перлит.
З а э в т е т о и д н ы е сплавы: от точки S к перпендикуляру из точки Е= от 0.83 до 2,06 % С= Fe3C + перлит.
Э в т е к т и ч е с к и й сплав: точка С = 4.3 % С = ледебурит.
Д о э в т е т и ч е с к и е сплавы : от перпендикуляра из точки Е к перпендикуляру из точки С = от 2.06 до 4.3 % С = Fe3C + перлит + ледебурит.
З а э в т е к т и ч е с к и е сплавы: от точки С к точке F (перпендикуляр); более 4.3% С = Fe3C + ледебурит
Фазы и структурные составляющие стали и белых чугунов. Основными компонентами, из которых состоят стали и чугуны, являются железо и углерод. В системе железо цементит имеются следующие фазы: 1. жидкая фаза, 2. Аустенит- твердый раствор углерода в - Fe. 3. Цементит - карбид железа Fe3C. 4. Феррит - - Fe .твердый раствор углерода в
Структурными составляющими диаграммы железо - углерод являются:
1. Феррит. Может содержать в твердом растворе только 0.00001 ... 0.000001 % С. Поэтому область его существования очень мала (узка). Максимум растворимости около 0.02 % (723 С, точка Р).
2. Перлит. - твердого раствора и Fe3C (ниже точки S). Мелкодисперсная смесь обеих фаз.Эвтектоид, состоящий из Наименование перлит (также предложено Хоу) связано с перламутровым блеском. - твердого раствора связан с выделением при непрерывном охлаждении тонких параллельных цементитных пластин; образуется пластинчатый перлит.Происходящий при непрерывном охлаждении при 723 С эвтектоидный распад
3. Ледебурит. Назван в честь Ледебура. - твердый раствор и Fe3C) и ледебурит II (перлит и Fe3C). - твердого раствора и цементита. Эвтектика (точка С, 4.3 % С). Сплавы, содержащие от 2,06 до 6,67 % С и имеющие в структуре ледебурит являются белыми чугунами. Возможно также следующие обозначение: ледебурит I (Смесь
Формы существования цементита :
- При содержании С более 0.00001 % происходит выделение третичного цементита. При медленном охлаждении процесс идет по линии PQ. При быстром охлаждении часть углерода остается в твердом растворе, выделение третичного раствора подавляется. Форма - пластинки и прожилки, а также иголки в ферритном зерне.
- Цементит перлита. Наблюдается уже при содержании углерода более 0.02 %. Тонкопластинчатая форма зерен цементита.
- Вторичный цементит. твердого раствора. При охлаждении выделение происходит по линии ES. Форма: цементитная сетка, цементит по границам зерен.Продукт выделения из
- Цементит ледебурита. При содержании углерода более 2.06 % - цементит в до- и заэвтектоидных сплавах.
- Первичный цементит. При 4.3 % С; в общем случае появляется при очень быстром охлаждении высокоуглеродистых сплавов до комнатной температуры. Форма: длинные крупные пластины.
