
- •3.1. Физико-химические и взрывчатые свойства ……………………
- •Физические свойства ……………………………………………
- •Химические свойства …………………………………………...
- •Взрывчатые свойства ……………………………………………
- •Таблица 1.2
- •Компоненты,%
- •Наполнитель
- •Свойства триаминотринитробензола
- •Детонационные характеристики ТАТНБ
- •Метансульфокислота
- •2.2. Получение в лаборатории и в промышленности
- •Стадия аминирования
- •2.3. Использование
- •3.1. Физико-химические и взрывчатые свойства
- •Рис.3.1. Пространственная структура нитротриазол-5-она (β-форма):
- •–атом азота, – атом углерода, – атом кислорода, – атом водорода
- •Таблица 3.5
- •Чувствительность НТО к различным видам воздействия
- •Позднее [131] условия синтеза были изменены: смешение компонентов проводили при 65 – 700С и мольном отношении ТО : НNО3 = 1: 4 – 8, и выход превысил 80%.
- •Схема получения ГНС из ТНТ при использовании NaOCl
- •Состав продуктов взаимодействия ТНТ с гипохлоритом натрия
- •Соединение
- •Содержание,%
- •Хроматография
- •ВЭЖХ*, время выхода, мин
- •6.3. Применение
Спектрометрический метод анализа разработал Д. Гловер. ТАТНБ растворяют в концентрированной серной кислоте и определяют поглощение при длинах волн 325 и 272 нм. Интенсивность поглощения на первой из них в 1,93–1,97 раза выше, чем на второй.
В ИК-спектрах наиболее интенсивное поглощение наблюдается в области 1180–1240 см-1 (2 полосы). Характерные полосы нитрогруппы слабо выражены и сильно смещены – 1450 и 1570 см-1; две полосы N-H- связей находятся при 3200 и 3300см -1.
2.2. Получение в лаборатории и в промышленности
Впервые ТАТНБ был синтезирован при нитровании 1,3,5- трихлорбензола олеумно-азотной кислотной смесью и последующем замещении атомов хлора на аминогруппу под действием аммиака. Позднее B. Flurscheim и H. Hоlmes получили его при действии 10% водного аммиака на пентанитроанилин. В 50-е годы в США для его получения использовали также 1,3,5-трибром-2,4,6-тринитробензол.
Так как 1,3,5-трихлорбензол является малодоступным соединением и его получают диазотированием трихлоранилина, в МХТИ им. Д. И. Менделеева к 1960 г. был разработан альтернативный метод получения ТАТНБ, основанный на окислении трихлоранилина персульфатом аммония в среде серной кислоты и метанола. Синтез проводили в соответствии со схемой, приведенной ниже [66].
При получении трихлорнитрозобензола использовали следующую методику: 10 г (0,05 моль) 2,4,6-трихлорбензола растворяли в смеси 28 г метанола и 14 г H2SO4 и при 300С присыпали 46,4 г (0, 2 моль) персульфата аммония и выдерживали 10 ч при 300С. После охлаждения полученный продукт отфильтровывали, промывали метанолом, водой и снова метанолом и сушили при 1000С. Получали 9,25 – 9,30 г 2,4.6-
37
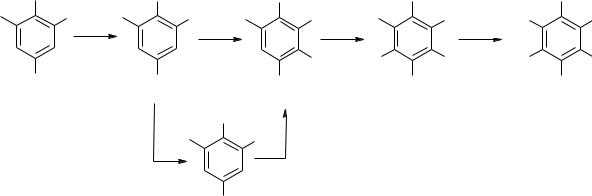
трихлорнитрозобензола. Выход 86,5%, температура плавления 141 – 1420С.
|
NH2 |
NO |
|
NO2 |
|
NO2 |
|
NO2 |
Cl |
Cl Cl |
Cl |
Cl |
Cl |
Cl |
Cl |
H2N |
NH2 |
|
|
|
|
NO2 |
O2N |
NO2 |
O2N |
NO2 |
|
Cl |
Cl |
|
Cl |
|
Cl |
|
NH2 |
|
|
|
NO2 |
|
|
|
|
|
|
|
Cl |
|
Cl |
|
|
|
|
Cl
Позднее в США [67,68] и в СССР [69] были разработаны другие варианты получения трихлорнитрозобензола, основанные на использовании пероксида водорода вместо персульфата аммония.
Одновременно разрабатывались альтернативные методы получения ТАТНБ и параллельно с ним – 1,3-диамино-2,4,6-тринитробензол (ДАТНБ). Так, Бензигер [70] разработал метод получения ТАТНБ из 3,5- дихлоранизола через тринитропроизводное. В МХТИ [71] при получении ДАТНБ из тетранитроанилина для уменьшения количества примесей, образующихся на стадии аминирования, первоначально получали 3- амино-2,4,6-тринитроанизол и лишь затем проводили аминирование.
В качестве альтернативного можно рассматривать и усовершенствованный Аткинсом [72] метод Флюршейма, в соответствии с которым ТАТНБ получают из 2,4,6-ТНТ через 4-амино-2,6- динитротолуол и пентанитроанилин. В конечном продукте присутствуют в качестве примеси полинитроаминофенолы. В предлагаемом процессе
38
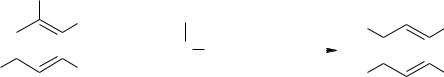
используются недорогие реагенты, но велики затраты, связанные с обезвреживанием отходов.
В последние годы предложен ряд новых методов получения ТАТНБ, в которых отказались от использования малодоступного 1,3,5- тринитро-2,4,6-трихлорбензола. В основе этих процессов лежит нуклеофильное замещение водорода в основных средах.
В Лаборатории им. Лоуренса в Ливерморе США разработан метод, основанный на реакции иодида 1,1,1-триметилгидразиния с пикрамидом в среде диметилсульфоксида (ДМСО) при комнатной температуре.
|
|
|
NO2 |
|
|
|
|
|
|
|
|
|
NO |
||||
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
2 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
H N |
|
|
|
|
NH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
+ |
|
N+ |
2 |
2 |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
O2N |
|
|
|
|
NH2 * I |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
NO2 |
|
|
|
|
|
|
|
O N |
|
|
|
|
NO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
2 |
|
|
2 |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
||
Рассматриваемый процесс был создан в рамках программы по утилизации устаревших боеприпасов. В России имелось около 30000 т подлежащего уничтожению 1,1-диметилгидразина, а в США – несколько тысяч тонн взрывчатого вещества «D» _ пикрата аммония, который может быть превращен в пикрамид [73].
Реакцию проводят в условиях большого избытка аминирующего агента (4–5 моль на 1 моль пикрамида) и основания (10 моль). При этом выход ТАТНБ достигает 89%, а чистота его более 99%. Уменьшение расхода иодида 1,1,1-триметилгидразиния до 3,1 моль снижает выход до 81%. На качество получаемого продукта сильное влияние оказывает концентрация пикрамида в растворе. При ее увеличении до 0,2 моль/л чистота продукта снижается до 97%. Основной примесью в продукте является диаминотринитробензол, в некоторых образцах зафиксировано присутствие иода. Процесс характеризуется большим расходом растворителя (до 40 мас. частей на 1 мас. часть пикрамида), и поэтому
39
ТАТНБ находится в растворе. Реакцию прекращают, разбавляя реакционную смесь водой или водным раствором минеральной кислоты. При этом образуются частицы ТАТНБ с размером 0,2 – 1 мкм. При добавлении органической кислоты (моногидрата лимонной кислоты) размер частиц увеличивается до 1–10μ ., и продукт имеет более светлую окраску.
Для синтеза можно использовать как товарный иодид 1,1,1- триметилгидразиния, так и приготовленный непосредственно перед синтезом, при добавлении к ДМСО последовательно диметилгидразина и метилиодида и соответствующей выдержке. Затем к полученному раствору прибавляют пикрамид, потом щелочь и продолжают реакцию до завершения.
Выход при обеих методиках близок между собой и составляет 82–88%. Позднее было показано, что в этом процессе метилиодид может быть заменен более дешевым диметилсульфатом, что одновременно исключает наличие атомов галогена в ТАТНБ [74,75].
В качестве основания используют метилат или этилат натрия, причем чистота последних (содержание в них соды) сильно влияет на выход ТАТНБ. Даже непродолжительное пребывание метилата натрия на воздухе приводит к существенному снижению выхода целевого продукта.
На качество ТАТНБ сильное влияние оказывают примеси в пикрамиде, в первую очередь, тринитрохлорбензол (из которого, получали пикрамид). Их присутствие приводит к значительному потемнению продукта и изменению его кристаллической структуры.
Полученный этим методом ТАТНБ по всем рабочим характеристикам подобен продукту, изготовленному из 1,3,5-трихлор-2,4,6- тринитробензола (ТХТНБ), однако температура разложения, определенная
40
К недостаткам метода могут быть отнесены относительно высокая токсичность и стоимость реагентов.
Сравнительно новый метод получения ТАТНБ из пикрамида основан на использовании в качестве аминирующего агента солей гидроксиламина в сильно основных средах. Взаимодействие полинитросоединений с гидроксиламином в основных средах известно давно, однако основными продуктами реакции были моноаминосоединения [76]. А.P. Митчел и П.Ф. Пагориа с сотрудниками [77] описали получение ТАТНБ из пикрамида при действии на последний солянокислым гидроксиламином и этилатом натрия, взятыми с большим избытком, в среде ДМСО при 650С в течение 6–12 ч. Получен продукт с чистотой более 99%, однако выход не приводится. Позднее было сообщено, что выход составлял 70–80% [74]. Продукт реакции может иметь зеленоватую окраску, обусловленную присутствием 1,3,5-триамино-2,4-динитро-6-нитрозобензола [78]. Этот продукт обнаружен также при облучении ТАТНБ ультрафиолетом. Использование О-эфиров гидроксиламина для нуклеофильного замещения водорода в ядре ароматических нитросоединений было предложено Секо [79].
Некоторые результаты опытов по получению ТАТНБ (а также ДАТНБ) сведены в табл.2.4 [75].
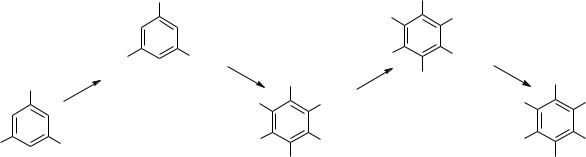
Еще один метод синтеза ТАТНБ был разработан в Англии в 2001– 2004 гг. Изменив природу алкилирующего агента в синтезе, где в качестве исходного вещества используют флороглюцин [80] (см схему), они создали два варианта процесса, в первом из которых использовали вместо диазометана диметилсульфат, а во втором – алкил-орто-формиаты [81]. При применении изопропил-ортоформиата можно алкилировать сам флороглюцин и в три стадии получить целевой продукт с выходом 87%.
41
Таблица 2.4
Получение ТАТНБ и ДАТНБ из пикрамида (ПА) при нуклеофильном замещении водорода в среде сухого ДМСО и в присутствии метилата натрия*
Нуклеофильный агент |
Моль** Моль*** |
ДМСО, |
T, 0С |
Время, |
Прекращение реакции |
Продукт |
Выход, |
||
|
|
|
мл/г |
|
ч |
|
|
реакции |
% |
Триметигидразиний |
1,9 |
3,9 |
33 |
20 |
3 |
водный раствор |
ДАТНБ |
|
|
иодид |
|
|
|
|
|
НС1, рН 4 |
|
|
|
Триметигидразиний |
4 |
8 |
34 |
20 |
16 |
лед, НС1 до рН 7 |
ТАТНБ |
95 |
|
иодид |
|
|
|
|
|
|
|
|
|
Метилиодид + |
5 |
11 |
33 |
20 |
40 |
5 моль лимонной |
ТАТНБ |
91 |
|
диметилгидразин |
5 |
|
|
|
|
кислоты/моль ПА |
|
|
|
Гидроксиламин |
5 |
11,3 |
37 |
20 |
4 |
100 |
мл насыщенного |
ДАТНБ |
27 |
гидрохлорид |
|
|
|
|
|
раствора NH4Cl|/ммоль |
|
|
|
Гидроксиламин |
5 |
16,1 |
45 |
90 |
12,5 |
5 моль лимонной |
ТАТНБ |
74 |
|
гидрохлорид |
|
|
|
|
|
кислоты/ моль |
|
|
|
О-бензил-гидроксиламин |
5 |
17 |
31 |
20 |
15 |
100 |
мл 0,12 н НС1/ммоль |
ДАТНБ |
87 |
4-амино-1,2,4-триазол |
7,3 |
16 |
13,5 |
20 |
2 |
100 |
мл 0,12 н НС1/ммоль |
ТАТНБ** |
98 |
*Аналогичные реакции осуществлены с ТНТ и рядом других ароматических и гетероциклических нитросоединений **моль нуклеофильного агента на 1моль нитросоединения
***моль основания на 1 моль нитросоединения
****В качестве исходного соединения использовали 1,3,5-тринитробензол
|
|
OAc |
|
OMe |
|
|
|
|
O2N |
NO2 |
|
|
OAc |
OAc |
MeO |
OMe |
|
|
OH |
|
OH |
NO |
NO |
|
|
|
2 |
2 |
|
|
|
O2N |
NO2 |
H2N |
NH2 |
HO |
OH |
HO |
OH |
O N |
NO |
|
|
2 |
2 |
||
|
|
|
NO2 |
|
NH2 |
Использование в качестве промежуточного соединения трипропокси-2,4,6- тринитробензола позволяет исключить присутствие хлора в очищенном ТАТНБ, который по чистоте и термической стабильности не уступает продукту, полученному из ТХТНБ. Аналогично можно получать ДАТНБ [82]. Использованию метода препятствует высокая стоимость флороглюцина.
Несмотря на наличие ряда альтернативных методов синтеза ТАТНБ, в промышленном масштабе осуществлено только получение его из трихлорбензола [74]. Описана установка для получения ТАТНБ по этой технологии [83]. Она состоит из
◦ эмалированного реактора (типа Pfaudler) вместимостью 40 литров, пригодного для проведения процесса при 20 – 1500С и давлениях от 0,01 до 0,7 МПа. Перемешивание осуществлялось якорной мешалкой с числом оборотов от 20 до 200 в минуту;
◦эмалированного холодильника-конденсатора паров, соединенного с реактором;
◦реактора из нержавеющей стали вместимостью 200 л с мешалкой, предназначенного для разбавления реакционной массы;
◦двух стальных резервуаров вместимостью 240 л, используемых для хранения фильтрата;
◦рамного фильтра-пресса из нержавеющей стали размером 28▪28▪5 см.
43
Стадия нитрования
Мольное соотношение реагентов : трихлорбензол : NaNO3 : SO3 = 1 : 6,6 : 15,6.
В реактор загружают 57,2 кг 30% олеума и при интенсивном перемешивании и охлаждении медленно присыпают 7,7 кг нитрата натрия. С помощью охлаждающей рубашки температуру поддерживают в интервале 60–700С. После прохождения экзотермического пика нагревают содержимое реактора до 1000С и при этой температуре присыпают 2,5 кг трихлорбензола. Затем температуру осторожно поднимают до 145–1550С с помощью подачи пара в рубашку и выдерживают при этой температуре 4 ч при работающем конденсаторе-холодильнике. После завершения выдержки реакционную массу охлаждают до 400С и выливают в разбавитель, в который предварительно помещают 113,5 кг мелко измельченного льда. Температура во время разбавления не должна превышать 400С, чтобы исключить гидролиз готового продукта. Операцию проводят при интенсивном перемешивании, нитрозные газы удаляются из раствора с помощью вакуум-насоса. 1,3,5- ТХТНБ выпадает в виде светло– желтых кристаллов. Реакционную массу после разбавления качают насосом на фильтры-прессы. В качестве фильтрующего полотна используют Dynel-ткань. Для выделения твердого осадка достаточно двух фильтров. Фильтры-прессы соединены с охлаждаемыми емкостями для хранения отработанной кислоты. Осадок промывают несколько раз на фильтре водой (общий расход воды 80 л), каждый раз взмучивая его воздухом, пока рН воды не станет равным 6 – 7. Отфильтрованный осадок сушат на полочной сушилке 16 ч при 600С. Выход на стадии нитрования 85%, температура плавления полученного ТХТНБ 189-192 0С.
44
