
Комплексные соединения
.pdf
11
Устойчивость комплексных соединений в растворе –
это вопросы химической связи в комплексных соединениях.
Многообразие свойств комплексных соединений вызвало к жизни, помимо теории Вернера, ещё ряд теорий, объясняющих природу связи между комплексообразователем и лигандами:
1. Теория валентных связей - рассматривая строение электронных оболочек атомов, объясняет природу ковалентной и донорно-акцепторной связей в комплексах, а также определённые значения координационных чисел.
2.Метод молекулярных орбиталей более тонко учитывает электронные взаимодействия в комплексах, показывает механизм образования многоцентровой делокализованной электронной системы.
3.Электростатическая теория, развившаяся в теорию кристаллического поля, рассматривает взаимодействие комплексообразователя и лигандов как заряженных частиц, с
учётом конфигурации валентных орбиталей.
4.Объединённая теория – теория поля лигандов –наиболее полно освещает характер связи в комплексных соединениях и причины их устойчивости.
12
Все эти теории согласны в следующем: СВЯЗИ МЕЖДУ СОСТАВНЫМИ ЧАСТЯМИ КОМПЛЕКСНОГО СОЕДИНЕНИЯ СИЛЬНО РАЗЛИЧАЮТСЯ ПО СВОЕЙ ПРОЧНОСТИ.
Первичная диссоциация комплексных соединений протекает по типу сильных электролитов, т.е. нацело:
[Ag(NH3)2]NO3 |
[Ag(NН3)2]+ + NO3¯ |
Связь между комплексообразователем и лигандами
значительно прочнее, тем не менее, в растворе имеет место
вторичная диссоциация, равновесие которой смещено в сторону
комплексного иона, это диссоциация слабого электролита:
[Ag(NH3)2]+ |
Ag+ + 2 NH3 |
В соответствии с законом действия масс, это равновесие
характеризуется константой равновесия, называемой константой
нестойкости комплексного иона:
С(Ag+) · C2(NH3)
Кн =
C([Ag(NH3)2]+)
Как следует из определения константы равновесия, в выражение константы нестойкости входят равновесные концентрации комплексного иона, комплексообразователя и лигандов.

13
Кн характеризует прочность данного комплексного иона: чем больше Кн , тем меньше его устойчивость.
Речь идёт об устойчивости только ВНУТРЕННЕЙ СФЕРЫ !
К3[Fe(CN)6]
С(Fe3+) · C6(CN¯)
Kн =
C([Fe(CN)6]3-)
На самом деле диссоциация комплексных ионов всегда протекает по стадиям, аналогично диссоциации многоосновных кислот. Кн учитывает суммарную устойчивость внутренней сферы.
Иногда прочность комплексного иона характеризуют
константой устойчивости:
1
Ку =
Кн
Условия разрушения комплексного иона.
Хотя связь комплексообразователя с лигандами прочная,
она всё же может быть разорвана. Это означает, что комплексный ион можно разрушить, т.е. заставить его полностью
продиссоциировать. |
|
|
|
|
Комплекс |
разрушается, |
если |
при |
действии |

14
соответствующего реагента образуется:
а) ещё более прочный комплекс (т.е. имеющий меньшую Кн)
или |
б) очень плохо растворимое вещество. |
||
|
Например, |
|
|
|
|
Кн |
|
|
|
|
|
|
[Ag(NH3)2]+ |
7·10-8 |
|
|
[Pt(NH3)4]2+ |
5·10-34 |
|
|
[NH4]+ |
5·10-10 |
|
Поэтому под действием кислот комплекс серебра разрушается, а комплекс платины – нет:
[Ag(NH3)2]+ + 2H+ |
Ag+ + 2NH4+ , |
[Pt(NH3)4]2+ + H+
Другой пример: если на раствор, содержащий комплексный
ион |
|
[Ag(NH3)2]+ |
Ag+ + 2NH3 |
подействовать раствором какого-нибудь хлорида, то |
осадка |
||
AgCl не образуется. |
Это означает, что концентрация |
Ag+ |
|
|
|
|
|
в растворе очень мала, и труднорастворимое соединение AgCl
образуется в том количестве, которое позволяет ему ещё находиться в растворе:

15
С(Ag+) · C(Cl¯) < ПРAgCl
При добавлении раствора любого сульфида к тому же
комплексу сразу образуется осадок Ag2S, это вещество характеризуется крайне низкой растворимостью:
|
AgCl |
Ag2S |
|
|
|||
|
|
|
|
Растворимость |
10-5 моль/л |
10-17 моль/л |
|
2[Ag(NH3)2]+ + Na2S |
Ag2S↓ + 4NH3 + 2Na+ |
C2(Ag+) · C(S2-) > ПР(Ag2S)
Изомерия комплексных соединений.
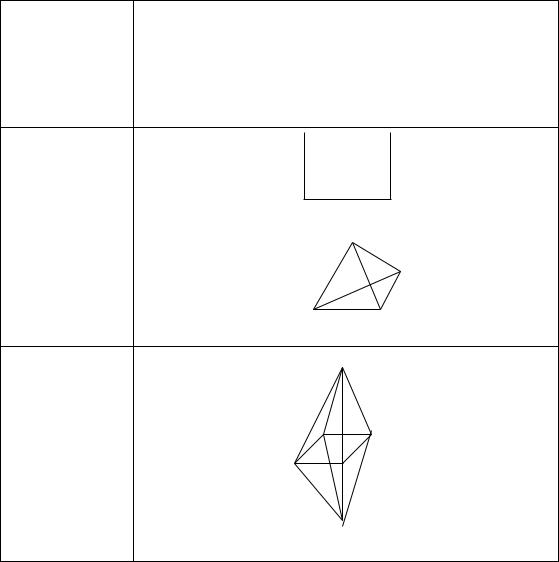
Одинаковые лиганды располагаются в пространстве вокруг комплексообразователя симметрично. Наиболее распространённым значениям координационных чисел 2, 4 и 6
соответствуют следующие геометрические конфигурации комплексов:
16
Координационное |
|
|
Конфигурация |
|
|
число |
|
|
|
|
|
|
|
|
|
|
линейная |
2 |
■ |
■ |
|||
|
|
|
|
|
|
|
|
|
|
■ |
■ |
||
4 |
|
|
плоская квадратная |
■ |
■ |
||
|
|
|
|
|
|
■ |
|
4 |
|
|
■ |
|
|
|
тетраэдрическая |
|
■ |
■ |
|
|
|
■ |
|
6 |
■ |
■ |
октаэдрическая |
|
|
|
|
|
■ |
■ |
|
|
|
■ |
|
Для координационного числа 4 и тетраэдрической конфигурации все положения лигандов относительно комплексообразователя эквивалентны. Поэтому
тетраэдрические комплексы типа
[ М А2 В2 ]
к.о. лиганды

17
не имеют изомеров
А в квадратных комплексах того же состава возможно
два способа расположения лигандов и, следовательно,
существование двух изомеров. Например, изомеры комплекса
[Pt(NH3)2Cl2] различаются по цвету, растворимости, дипольному моменту, реакционной способности и способам получения:
Cl- ● |
●NH3 |
|
Pt2+ |
H3N ● |
●Cl- |
транс-изомер |
|
Cl- ● |
●NH3 |
|
Pt2+ |
Cl- ● |
●NH3 |
|
цис-изомер |
Это ГЕОМЕТРИЧЕСКАЯ изомерия.
При увеличении числа различных заместителей число геометрических изомеров растёт.
Этот вид изомерии присущ и октаэдрическим комплексам.
Кроме геометрической изомерии известны:
Гидратная изомерия – наблюдается при переходе воды из внутренней сферы во внешнюю и наоборот:
III |
|
[Cr(H2O)6]Cl3 |
[Cr(H2O)5Cl]Cl2·H2O |
[Cr(H2O)4Cl2]Cl·2H2O |
|
сине-фиолетовый |
светло-зелёный |
18
Ионизационная изомерия - при различном распределении ионов между внутренней и внешней сферами:
IV |
|
|
[Pt(NH3)4Cl2]Br2 |
и |
[Pt(NH3)4Br2]Cl2 |
Координационная изомерия связана с переходом лигандов от одного комплексообразователя к другому:
[Co(NH3)6][Cr(CN)6] |
|
и |
[Cr(NH3)6][Co(CN)6] |
|
Для |
асимметрических |
комплексных соединений, не |
||
имеющих |
плоскости |
симметрии, |
известна оптическая |
|
(зеркальная) изомерия. |
Зеркальные изомеры (антиподы) имеют |
|||
сходную структуру, но, поскольку они как бы являются
зеркальным отражением друг друга (как, например, руки человека), то в пространстве они не совместимы. Один из антиподов вращает плоскость поляризации света влево (l-изомер),
а другой – вправо (d-изомер). Зеркальные изомеры имеют одинаковые физические и химические свойства, но их биологическая активность может быть совершенно различной.
