
Акулов, Федотов. Основы теории биотехнических систем
.pdf
Количество уравнений, входящих в систему, задает точность вычисления UM. Можно показать, что для ошибки, не превышающей 0,5%; достаточно выбрать N =5, т.е. влияние соседних перехватов на формирование напряжения на мембране «нулевого» перехвата быстро ослабевает.
При учете только нулевого перехвата (k =0) получаем первое приближение модели, имеющее упрощенный вид
|
|
τ M |
dUM , 0 |
+UM , 0 = − |
2Ga |
|
(3.23) |
|||||||
|
|
|
|
dt |
|
GM (−UM , 0 + Ve, 0 ) |
|
|||||||
|
|
τ M′ |
dUM |
+UM |
2Ga |
Icmρe |
= Ucm |
(3.24) |
||||||
|
|
|
dt |
= aGM |
4π r0 |
|
||||||||
|
τ M |
= |
|
τ M |
|
|
|
|
2G |
|
|
|
||
где: |
|
, |
a = 1+ |
|
|
|
|
|
||||||
′ |
|
|
|
|
|
|
a |
|
|
|
|
|||
|
|
a |
|
|
G |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
M |
|
|
|
|
Решение данного уравнения определяется заданием параметров стимулирующего тока и начальными условиями задачи. Допустим, стимуляция осуществляется прямоугольными импульсами тока, имеющего вид единичной ступенчатой функции:
Icm = Icm01(t)
Кроме того, предположим, что в отсутствие стимула мембранный потенциал находится в равновесном состоянии, т.е. UM = −UMпок . Тогда решение уравнения (3.23) будет иметь вид:
|
|
|
|
|
|
|
|
t |
|
|
U |
|
= −U |
|
+U |
1 |
− exp |
− |
|
|
|
M |
Mпок |
τ ′ |
||||||||
|
|
|
cm |
|
|
|
||||
|
|
|
|
|
|
|
|
M |
||
Напряжение на мембране при воздействии стимулирующего тока прямоугольной формы будет изменяться по экспоненциальному закону. Установившееся значение напряжения на мембране определяется величиной стимулирующего тока, расположением электрода и зависит от проводимостей аксоплазмы, мембраны и среды, окружающей нервный проводник.
Время установления напряжения определяется постоянной времени мембраны и зависит от соотношения проводимостей мембраны и аксоплазмы.
190
Более строгое описание процессов возбуждения нервного волокна дает использование в кабельной модели нерва уравнений Ходжкина-Хаксли-Франкенхаузера для описания ионных токов мембраны, которые имеют численные решения и были использованы далее для иллюстрации исследования закономерностей процессов электростимуляции нервного волокна. Первое приближение модели, имеющее аналитическое решение, позволяет исследовать некоторые характеристики электростимуляции нервного волокна.
В соответствии с параметрической моделью возбуждения нервного волокна возникновение потенциала действия осуществляется при достижении напряжением на мембране порогового значения. Если прямоугольные стимулы имеют конечную длительность, то величина порогового тока возбуждения, формируемая генератором стимулирующего тока, будет зависеть от соотношения длительности стимула и постоянной времени нарастания мембранного тока.
UM = UMПОР; I0 |
= I0ПОР; |
|
t = tИ |
|
|
|
|
||||||||
|
|
|
I |
ПОР |
ρ G |
a |
|
|
|
t |
И |
−1 |
|||
U ПОР = −U ПОК + |
|
0 |
|
e |
|
1 |
− exp |
− |
|
|
|||||
2πr aG |
|
|
τ |
|
|||||||||||
M |
|
M |
M |
|
|
|
|
|
|||||||
|
|
|
|
|
0 |
|
|
|
|
|
|
М |
|||
|
|
|
|
|
t |
И |
−1 |
|
|
|
|
|
|||
I ПОР = I |
P |
1− exp |
− |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||||||
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
τ M |
|
|
|
|
|
|
|
|||
где: Ip – реобазовое значение тока.
Полученное соотношение определяет зависимость «сила - длительность», устанавливающую связь между выбором амплитуды и длительности прямоугольного стимула, вызывающего возбуждение нерва. Кривая «сила-длительность» (рисунок 3.16) показывает, что для сохранения возбуждения нерва при укорочении длительности стимула необходимо увеличивать его амплитуду. Уменьшение амплитуды порогового тока при увеличении длительности стимула ограничено значением реобазы, определяющим
191
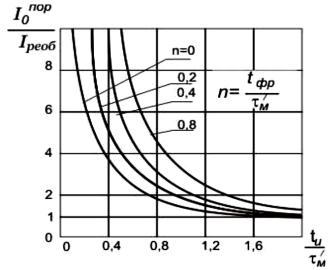
асимптоту кривой «сила – длительность» при увеличении длительности стимула.
Гиперболический характер кривой «сила – длительность» связан с влиянием емкостных свойств возбудимой структуры. Действительно, для достижения порогового потенциала необходимо сообщить мембране некоторый пороговый заряд. Относительное постоянство этого заряда при изменении параметров стимуляции обуславливает обратную пропорциональность между током и длительностью порогового стимула. В частности, параметры кривых «сила – длительность», характеризующие возбудимые свойства тканей при электростимуляции, оказываются различными при изменении условий стимуляции и различных объектах воздействия.
Рисунок 3.16 – Зависимость «сила-длительность» для стимулов прямоугольной формы с длительностью фронта tфр
Возбудимость нерва падает с увеличением длительности фронта прямоугольного стимула. Порог возбудимости растет тем быстрее, чем меньше длительность стимула, так как при коротких стимулах увеличение фронта ведет к резкому падению заряда сообщаемого мембране, что требует значительного увеличения амплитуды тока стимула, необходимого для достижения порогового
192

потенциала. Таким образом, стимулы с крутым фронтом обладают более сильным раздражающим действием, чем стимулы, нарастающие медленно.
Величина проводимости среды, окружающей нерв, влияет на ее релаксационные свойства и, тем самым, изменяет условия возбуждения. С ростом проводимости среды падает постоянная времени нарастания мембранного потенциала, однако возрастает шунтирующее действие среды, что может привести к резкому снижению возбудимости нерва.
Возбудимость нервного волокна зависит от его диаметра. Кривые «сила – диаметр», построенные для различных значений длительности стимулов показывают, что с увеличением диаметра волокна порог возбуждения падает сначала обратно пропорционально квадрату диаметра, затем уменьшение порога ослабевает.
Рисунок 3.17 – Зависимость «сила – диаметр» для стимулов прямоугольной формы с различной длительностью
С укорочением длительности стимулов (рисунок 3.17) возрастает дифференциация порогов возбуждения толстых и тонких волокон, что свидетельствует о рациональности использования ко-
193
ротких стимулов для избирательного воздействия на волокна требуемой модальности. Данная зависимость подтверждается экспериментально при изучении дифференциации порогов тактильной и болевой электрокожной чувствительности, относящихся к нервными структурам различных типов.
Модель возбуждения нервного волокна позволяет исследовать влияние на характеристики возбуждения геометрии системы «нервный проводник – электрод», изменений условий среды распространения тока, параметров формирователя стимулирующего тока.
3.5. Формирование стимулирующего воздействия в биотехнических системах электронейростимуляции
Анализ структуры БТС электронейростимуляции показывает, что достижение высокой эффективности электронейростимуляции определяется выбором параметров и формы стимулирующего тока, который должен быть согласован как с параметрами физиологической системы организма, на которую оказывается воздействие, так и с условиями передачи стимулов от электродов к возбудимым нервным структурам.
При определении параметров необходимо учитывать общие закономерности возбуждения нервных структур, а также особенности электронейростимуляции, обусловленные влиянием частотных характеристик биологических тканей, заключенных в межэлектродном промежутке.
Для анализа влияния электрофизических свойств тканей на процессы возбуждения удобно представить пассивную биологическую ткань в виде модели – электрической эквивалентной схемы замещения, обладающей импедансными свойствами живой ткани.
Импульсный ток, используемый при электронейростимуляции, имеет широкий частотный спектр (длительность импульса tи = 10…100 мкс, верхняя граничная частота порядка 100 Гц…10 кГц), таким образом требуется описание свойств тканей в достаточно широком диапазоне частот.
194

В рассматриваемом диапазоне ткани показывают резистивноемкостной характер сопротивления. Активные составляющие импеданса характеризуют компоненты тока в жидких электролитах (кровь, лимфа, межтканевая жидкость и др.) и обусловлены переносом зарядов в электрической цепи. Емкостные составляющие связаны с явлениями разделения зарядов, которые наблюдаются в многокомпонентных тканях с разнородной структурой.
Особенно важную роль играют пассивные биологические ткани при чрескожной электронейростимуляции. В данном случае (рисунок 3.18) цепь, включающая электрод, контактную пасту, кожу, подлежащие ткани, ткани, окружающие возбудимую нервную структуру, выполняет функцию своеобразного фильтра, ослабляющего отдельные частотные компоненты спектра стимула, что приводит к изменению формы напряжения на возбудимой структуре.
Рисунок 3.18 – Чрескожная электронейростимуляция
Спад АЧХ тканей в области высоких частот приводит к увеличению длительности фронта импульса (tфр), что ведет к падению возбудимости нервной структуры. Увеличение стимулирующего тока, которое может компенсировать падение возбудимости, ограничено возникновением неприятных ощущений и повреждений изза прохождения тока в тканях. Кроме того, следует отметить, что на импеданс тканей влияет также деятельность потовых желез, местного кровотока, температура, влажность, давление окружающего воздуха.
Определение биоимпедансных свойств пассивных биологических тканей можно проводить методом функционально– структурной идентификации биологических звеньев БТС. Данный метод был рассмотрен выше. Характер зависимости активной и
195

реактивной составляющих биоэлектрического импеданса от частоты при чрескожных измерениях аналогичен случаю имплантируемых электродов.
На низких частотах (f < 100Гц), емкостная составляющая биоэлектрического импеданса мала и основной вклад вносит активная составляющая, которая может быть отнесена к верхним слоям кожи, обладающим на этих частотах низкой проводимостью.
На высоких частотах (f >10кГц) емкостная составляющая биоэлектрического импеданса падает, что может быть объяснено уменьшением влияния структур, разделяющих заряды. Активная составляющая при этом стремится к постоянному значению, характеризующему свойства электролитных тканей, имеющих высокую проводимость.
Синтез эквивалентной схемы замещения биоэлектрического импеданса тканей дает модель, состоящую из RC – звеньев (рисунок 3.19). Количество звеньев модели определяется требуемой точностью аппроксимации характеристик модели и биологической ткани. Для 10% точности необходимо 3 звена, часто пользуются двухзвенной цепочкой, упрощающей анализ.
Рисунок 3.19 – Двухзвенная модель биоэлектрического импеданса
Для анализа процессов электронейростимуляции с имплантируемыми электродами часто используют модель биоэлектрического импеданса в виде параллельно соединенных элементов R и С; эквивалентная схема замещения показана на рисунке 3.20: ЭС – электростимулятор, ПБТ – пассивные биологические ткани, ВНС – возбудимая нервная структура. Поскольку R1 << Ra , RM , то цепь
ПБТ+ЭС можно рассматривать как генератор ЭДС для цепи возбудимой нервной структуры.
196
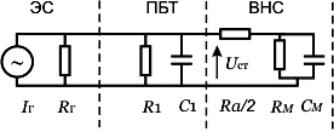
Рисунок 3.20 – Эквивалентная схема для анализа процессов электронейростимуляции
|
|
|
|
|
|
|
|
|
1 |
|
R R |
|
|
|
1 |
I |
R' |
||
UСТ |
= IГ |
(R1 |
RГ |
|
|
) = IГ |
1 Г |
|
|
|
|
= |
|
Г 1 |
|||||
|
|
|
|
|
|
|
|
' |
|||||||||||
R' |
= |
|
R1 |
|
|
|
jωC1 |
|
R1 + RГ |
|
|
|
jωC1 |
1+ jωR1C1 |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
1 |
|
1 + |
|
R1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
RГ |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Рассмотрим формирование UСТ при использовании прямоугольного стимула.
I Г = I01(t) |
|
|
|
|
|
I R' |
|
|
|
' |
|||
; UСТ ( р) = |
|
0 |
1 |
; |
Т1 |
= R1C1 |
|||||||
р(1+ рТ1 ) |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
||||
|
−1 |
U |
( p) |
|
U |
|
|
|
' |
(1− exp(−t / T )) |
|||
U (t) = L |
|
; |
|
(t) = I R |
|||||||||
СТ |
|
|
{ СТ |
|
|
СТ |
|
0 |
1 |
|
1 |
||
|
|
} |
|
|
|
||||||||
Таким образом, расположение нервного волокна в среде с большой инерционностью определяет замедление роста амплитуды напряжения импульса, прикладываемого к мембране. Это приводит к тому, что импульс не достигает своего амплитудного значения, определяемого параметрами выходного каскада электростимулятора, поэтому требуется увеличение амплитуды тока стимула, что и приводит к росту энергетических потерь тока в тканях.
Полученные соотношения позволяют проанализировать влияние выходного сопротивления генератора стимула на процесс электростимуляции. Видно, что уменьшение RГ ведет к падению напряжения на возбудимой структуре из-за шунтирования тканей,
197
поэтому для достижения пороговых значений возбуждения требуется увеличение амплитуды стимула.
Снижение выходного сопротивления генератора не желательно с точки зрения предотвращения неконтролируемого изменения тока стимула, вследствие протекания различных физиологических процессов, например, усиления кровотока. Это затрудняет дозирование тока и поддержание постоянных значений параметров электростимуляции.
Обычно выбирают выходное сопротивление электростимулятора, по крайней мере, в 10 раз превышающее сопротивление биологической цепи, т.е. в выходных каскадах электростимулятора используется режим генератора тока.
При прохождении стимулирующего тока по цепи пациента, образованной из выходного каскада электростимулятора, электродов, участка пассивной биологической ткани и возбудимой нервной структуры, в пассивных биологических тканях возникают энергетические потери тока. Данные потери связаны с прохождением тока по активной составляющей импеданса межэлектродного промежутка, что приводит к выделению тепла в тканях.
Рассмотрим два аспекта выбора параметров электростимуляции, связанных с минимизацией энергетических потерь стимулирующего тока в тканях:
1.Для чрескожной электронейростимуляции распределение тока в тканях под электродами приводит к нагреву тканей и ноцицептивным раздражениям кожных рецепторов, приводящим к болевым ощущениям, что является ограничением увеличения стимулирующего тока.
2.Для имплантируемых систем тепловые потери тока в пассивных биологических тканях ограничивают срок службы автономных источников питания.
В обоих случаях задача поиска адекватных параметров тока формулируется как задача нахождения параметров стимула, обладающего способностью порогового возбуждения нерва при условии минимизации энергетических потерь в тканях.
198
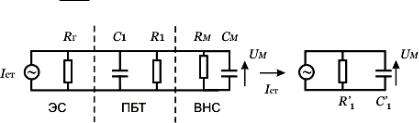
При условии работы выходного каскада электростимулятора в режиме генератора тока, для параметрической модели возбуждения можно принять для анализа модель ЭНС, показанную на рисунке 3.21, при этом:
|
|
R' |
' |
|
|
|
|
|
|
|
|
|
' |
= C1 + CM |
||||
|
1 |
|
|
|
|
|
|
|
|
|
|
|||||||
U |
М = ICT |
1+ jωC' |
R' |
, R1 |
= RГ |
|
|
|
R1 |
|
|
|
RM , |
C1 |
||||
|
|
|
|
|
||||||||||||||
|
1 |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
R' |
ICT = I01(t), |
I0 ( p) = I |
1 |
|||||||||||
UМ ( p) = ICT ( p) 1+ pT ' , |
0 p |
|||||||||||||||||
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
UM = I0 R1' (1− exp(−t / T1' )),
Если UM = UMпор , то t = tи , тогда:
I0пор = I p (1− exp(−tи / T1' ))−1
U пор
где: Ip = М' .
R1
Рисунок 3.21 – Модель ЭНС для параметрической модели возбуждения
Энергия, затрачиваемая при возбуждении нерва:
tи
W = ∫ IСТ2 Rэdt
0
где: Rэ – активная составляющая импеданса.
Для прямоугольного стимула:
W = IСТ2 Rэtи
Энергия для случая порогового значения стимулирующего тока:
Wпор = Iр2 (1−exp(−tи / T1' ))−2 R1'tи
199
