
- •2. Марганец и его соединения. Биологическая роль.
- •3. Железо и его соединения. Биологическая роль.
- •4. Ионное произведение воды. Водородный показатель.
- •5. Силы Ван-дер-Вальса.
- •7. Упругость пара над раствором. Законы Рауля.
- •9. Ионная связь.
- •11. Кислородосодержащие кислоты хлора. Соли этих кислот. Биологическая роль.
- •12. Координационная теория Вернера.
- •13. Классификация и изомерия комплексных соединений.
- •15. Кислородосодержащие кислоты серы. Соли этих кислот.
- •16. Понятие о квантовой механике.
- •17. Многоэлектонные атомы и периодический закон.
- •18. Окисли азота.
- •19. Окислительно-восстановительные реакции.
- •20. Аммиак и его свойства.
- •21. Водородные соединения галогенов. 22. Галогеноводородные кислоты.
- •23. Метод молекулярных орбиталей.
- •25. Константа и степень электролитической диссоциации.
- •26. Азотная кислота и ее соли.
- •27. Гибридизация атомных орбиталей.
- •29. Периодичность изменения свойств элементов и их соединений.
- •30. Гидролиз.
- •32. Благородные газы.
- •35. Металлическая связь.
- •38. Современная химическая атомистика.
- •39. Осмос. Осмотическое давление. Закон Вант Гоффа.
- •41. Теория Бора.
- •43. Скорость химических реакций. Химическое равновесие.
- •44. Понятие об активном комплексе и энергии активации.
- •45. Серная кислота
- •46. Растворы. Растворимость как физико-химический прочес (гидратная теория, теория Менделеева).
45. Серная кислота
тяжелая маслянистая жидкость ("купоросное масло"),нелетучая, хорошо растворима в воде – с сильным нагревом; Производство:1стадия.Печь для обжига колчедана. 4FeS2 + 11O2 2Fe2O3 + 8SO2 + Q Процесс гетерогенный:1) измельчение железного колчедана (пирита); 2) метод "кипящего слоя"; 3) 800°С; отвод лишнего тепла; 4)увеличение конц-ции O2 в воздухе.
2-я стадия. После очистки, осушки и теплообмена сернистый газ поступает в контактный аппарат, где окисл-ся в серный ангидрид (450°С – 500°С; катализатор V2O5): 2SO2 + O2 -> 2SO3.
3-я стадия. Поглотительная башня: nSO3 + H2SO4(конц) -> (H2SO4 • nSO3)(олеум).Пром:4FeS2 + 11O2 = 2Fe2O3 + 8SO2\2SO2 +O2 (V2O5) → 2SO3\SO3+H2O→H2SO4(оксидSo2+O2-газ\жид\тв)
Хим св-ва:- сильная двухосновная кис-та: 1)Взаимод=вие с ме:a) разбав-ная серная кис-та раств-ет только ме, стоящие в ряду напряжений левее H2: Zn+ H2SO4(разб) -> Zn+2SO4 + H2O;
b) конц-ная H2+6SO4 – сильный окис-ль; при взаимод-вии с ме (кроме Au, Pt) может восстан-ся до S+4O2, S0 или H2S-2 (без нагревания не реагируют также Fe, Al, Cr - пассивируются):
2Ag + 2H2+6SO4 ->Ag2+1SO4 + S+4O2 + 2H2O;
8Na + 5H2+6SO4 ->4Na2+1SO4 + H2S-2 + 4H2O
2)конц-ная H2S+6O4 реаг-ет при нагревании с некот неме за счет своих сильных окисл-ных св-в, превращаясь в соед-ния серы более низкой степ окисл-я, (например, S+4O2):
С + 2H2S+6O4(конц) -> C+4O2 + 2S+4O2 + 2H2O; S+ 2H2S+6O4(конц) -> 3S+4O2 + 2H2O; 2P+ 5H2S+6O4(конц) -> 5S+4O2 + 2H3P+5O4 + 2H2O
3)с основными оксидами\гидроксидамиCuO+H2SO4 ->CuSO4 +H2O;
5)обменные р-ции с солями: BaCl2 +H2SO4 ->BaSO4+ 2HCl.
Качественная реакцияBa(2+) + SO4(-2) = BaSO4
Сульфаты
— минералы, солиH2SO4.
В их кристаллической структуре
обособляются комплексные анионы SO42−
.Р-ция с хлоридом бария даёт белый
кристаллический осадок сульфата бария:![]() В
ионном виде:
В
ионном виде:![]() Р-ция
с ацетатом свинца даёт белый кристаллический
осадок сульфата свинца:
Р-ция
с ацетатом свинца даёт белый кристаллический
осадок сульфата свинца:![]() В
ионном виде:
В
ионном виде:![]() Гидросульфаты, бисульфаты — кислые
соли серной кислоты H2SO4, напр NaHSO4.
Получение Гидросульфаты получают при
избытке серной кис-ты:Na2CO3 + H2SO4(изб.)=
2NaHSO4 + H2O + CO2↑Также умеренным нагреванием
сульфатов с серной кис-той:K2SO4 + H2SO4 =
2KHSO4Св-ва: Гидросульфаты калия и натрия
при нагревании теряют воду, превращаясь
в пиросульфаты:2KHSO4 = K2S2O7 + H2O В свою очередь
пиросульфаты тоже при нагревании
разлагаются:K2S2O7 = K2SO4 + SO3↑Применение:мин удобрений;электролит в свинцовых
аккумуляторах;в производстве химических
волокон, красителей, дымообразующих и
взрывчатых веществ;в нефтяной,
металлообрабатывающей, текстильной,
кожевенной и др. отраслях промышленности;в
пищ,
Гидросульфаты, бисульфаты — кислые
соли серной кислоты H2SO4, напр NaHSO4.
Получение Гидросульфаты получают при
избытке серной кис-ты:Na2CO3 + H2SO4(изб.)=
2NaHSO4 + H2O + CO2↑Также умеренным нагреванием
сульфатов с серной кис-той:K2SO4 + H2SO4 =
2KHSO4Св-ва: Гидросульфаты калия и натрия
при нагревании теряют воду, превращаясь
в пиросульфаты:2KHSO4 = K2S2O7 + H2O В свою очередь
пиросульфаты тоже при нагревании
разлагаются:K2S2O7 = K2SO4 + SO3↑Применение:мин удобрений;электролит в свинцовых
аккумуляторах;в производстве химических
волокон, красителей, дымообразующих и
взрывчатых веществ;в нефтяной,
металлообрабатывающей, текстильной,
кожевенной и др. отраслях промышленности;в
пищ,
в орг синтезе.Сульфат магния, или горькая соль (МgSO4 * 7Н2О) применяется в медицине как слабительное.
46. Растворы. Растворимость как физико-химический прочес (гидратная теория, теория Менделеева).
Растворы –
это однородные (гомогенные) системы
переменного состава находящиеся в
состоянии химического равновесия,
представляют собой дисперсные системы,
в кот частицы одного в-ва равномерно
распределены в другом. (газ,жид,ТВ- медь
в золоте); а по степени дисперсности –
взвесями, коллоидными и истинными
растворами.Для описания состояния в-ва
исп-ют физ и хим теории.Согласно физ:при
растворении в-ва в р-ле идёт процесс
распределения частиц,не наблюдается
тепловых.эфектов,изменений объема(она
имеет место в близких к идеальных
р-рам).Хим.теория р-ров Менделеева:согласно
ей растворение явл-ся физ-хим
процессом,помимо фих.процесса молекулы
в-ва с мол воды образуютгидраты(NH3∙2H2O,H2SO4∙2H2O,
[Cu(H2O)4]+2)При
этом:ТЭ,изм.объема,оптич.эф(цвет)( (при
смешении воды со спиртом объем
уменьшается,при растворении белого
безводного сульфата меди в воде раствор
окрашивается в голубой цвет – образование
гидратированног ионаCu).Общие
св-ва р-ров-это такие св-ва кот зависят
от числа равных частиц,т.е. концентрации,а
не от их природы.Массовая доля: wВ =
mB / m(р).Моляр.конц.сВ = nВ / V(р).Закон
Вант-Гофф: для разбавленных растворов
независимо от природы растворителя и
раств в-ва мат выражение для осм давления
имеет вид:Р = CRT.Количественно связь
между концентрацией летучего вещества
в идеальном растворе и давлением его
пара над раствором выражаетсязаконом
Рауля: относительное понижение
упругости пара над раствором равно
мольной доле растворенного вещества.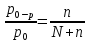 (ость
пара чист.р-ля,упр пара р-ра,число моль
р-ля и раств.в-ва)Следствие:р-ры кипят
при Т более выс чем р-ль.Р-ры кристаллизуются
при Т ниже Т р-ля.2закон Рауля:Повышение
Ткип и понижение Тзам прямопропорциональн
моляр.концентрации раст.в-ва.t=
(ость
пара чист.р-ля,упр пара р-ра,число моль
р-ля и раств.в-ва)Следствие:р-ры кипят
при Т более выс чем р-ль.Р-ры кристаллизуются
при Т ниже Т р-ля.2закон Рауля:Повышение
Ткип и понижение Тзам прямопропорциональн
моляр.концентрации раст.в-ва.t= *С.Физ.смысл
К:показывает на сколько выше кипит
одномолярный р-р сравнимо с чист.р-лем.
*С.Физ.смысл
К:показывает на сколько выше кипит
одномолярный р-р сравнимо с чист.р-лем.
47. Мышьяк .Степени окисления +3, +5, –3 (валентности III, V).
Физ и хим св-ва. Мышьяк — серое с металлическим блеском хрупкое вещ-во с ромбоэдрической кристаллической решеткой. При нагревании до 600 °C As сублимирует. При охлаждении паров возникает новая модификация — желтый мышьяк. Выше 270 °C все формы As переходят в α-мышьяк. При хранении на воздухе порошкообразный мышьяк восплам-ся с образ-ем кисл-го оксида As2O3. В земной корев связанном состоянии, хотя изредка встречается и самородный мышьяк: сульфиды мышьяка (реальгарAsSи аурипигментAs2S3) и сульфоарсениды и арсениды металлов (арсенопиритFeAsS, мышьяковистый колчеданFeAs2).Получение путём обжига прир.сульфидных руд:2As2S+9J2=2As2O3+6SO2,As2O3+3C=2As+3CO\Реакции мелкораздробленного:As+O2=As2O3\As+Cl2=AsCl2\As2S2\As+ 5HNO(конц.) = H3As04+ 5N02+ Н20\As+NaOHконц=H3AsO3+H2/Соединение с водородом=арсин.(вост-ль)Mg3As2+6HCl=3MgCl2+2AsH2\H3PO3+AsH3=H3PO2+2As+3H2O\12AgNO3+2AsH3+3H2O=12Ag+As2O3+12HNO3/Соединения с кислородом:As2O3-бел.крист.=As+O2; As2O3+H2O=H3AsO3(мышьяковистая) As2O3+KOH=K3AsO3+H2O\) As2O3+KOH+H2O=2K[As(OH)4]As2O5-бел.порошок;)H3AsO4= As2O5+Н2О\As2O5+КОН=K3AsO4+3H2O;As2O5+Li2O=Li3AsO4.Соединение с галогенамиAs+F2=AsF3\ 2AsF3+3H2O=As2O3+2HF\AsF3+3NH3=[As(NH3)3]F3\AsF5+H2O=H3AsO4+5HF\Соединения с серой:желтое в-воAs2S3+3Na2S=2Na3AsS3\As2S5+3(NH4)2S=2(NH4)3AsSСоединения с Ме=арсениды.Применение:типографич. И антифрикционные сплавы,сплавы бронз,латуни,свинцовой дроби;пиротехника,стекл.пром-ть обесцвечивание,соединения-люминофоры в производстве люминисцентных ламп)хлорид –в фарм.преп,для стоматологии
Биолог. роль .ядовит\15мг почках,печени,селезенке,кишечнике,легких,больше всего-в волосах и костях.Содержится в рыбе,виноградных соках,табач.дым;участвует в окислительном распаде УВ,в малых дозах усиливает метаболизм,кроветворение,проявляет антимикроб.св-ва,. При остром отравлении мышьяком наблюд-ся рвота, боли в животе, понос, угнетение центральной нервной сис-мы.,ис-ся в препаратах от кожных,венерических,туберкул,ЖКТ,неврастении.
1
