
Минералогия_2 / Бетехтин / betehtin_1
.pdf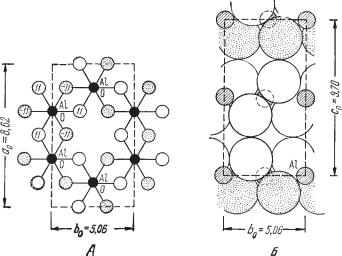
Раздел IV. Окислы (оксиды) |
371 |
железа Fe[OH]3, образующийся в первые моменты при гидролизе солей этого металла, неустойчив и быстро подвергается обезвоживанию. Ион Fe3+
внебольших количествах иногда входит лишь изоморфно в состав Al[ОН]3. В гидратах алюминия также в виде изоморфной примеси присутствует Ga3+
взначительно повышенных против кларка количествах.
ГИББСИТ — Аl[ОН]3. Назван в честь минералога из США Д. Гиббса (1776—1833). Впервые был установлен в XIX столетии на Урале. Сино ним: гидраргиллит, от греч. гидор — вода и аргиллос — белая глина.
Химический состав. Аl2О3 — 65,4 %, Н2О — 34,6 %. В виде изоморф ной примеси устанавливаются Fe2O3 (до 2 %), а также Ga2O3 (до 0,006 %). Химические анализы часто обнаруживают почти полное совпадение со става с теоретической формулой.
Сингония моноклинная; призматический в. с. L2PC. Пр. гр. Р21/п(С22h). a0 = 8,624; b0 = 5,060; с0 = 9,700, β = 94°34′. Кристаллическая структура слоистая, близкая к искаженной структуре брусита. Некоторые особен ности ее обусловлены тем, что ион алюминия по сравнению с ионом маг ния обладает большим зарядом и меньшей величиной ионного радиуса. В гиббсите, так же как и в брусите, каждая пачка состоит из двух слоев плотно упакованных гидроксильных ионов, между которыми располага ется слой катионов Аl3+ (рис. 197). Так как заряд иона алюминия больше, чем заряд иона магния, то для нейтрализации отрицательного заряда гид роксильных ионов требуется меньшее число катионов Al3+. Поэтому ка тионы Аl3+ занимают не все октаэдрические пустоты между слоями ОН, как это имеет место в брусите, а только две трети их.
В связи с этим ионы Аl3+ располагаются не в виде центрированных гек сагонов, как в структуре брусита, а по корундовому мотиву в виде простых
Рис. 197. Кристаллическая структура гиббсита

372 Описательная часть
шестиугольников (ср. расположение черных точек на рис. 196 и 197). Если оконтурить такой шестиугольник, то легко видеть, что на него в пачке струк туры брусита приходится шесть гидроксильных ионов и три полных иона Mg2+ (один центральный ион плюс шесть периферических, каждый по 2/6 валентности), т. е. формула гексагона будет Mg3[OH]6. Для структуры же гиббсита, при том же числе гидроксильных ионов, в формуле гексагона будет только два иона Аl3+, т. е. она будет иметь вид Аl2[ОН]6. Различие заключается также в способе сочленения пачек друг с другом: в то время как в структуре брусита каждый ион [ОН]1– приурочивается к центру между тремя ионами [ОН]1– следующего слоя, в структуре гиббсита каждый ион [ОН]1– одного слоя противостоит каждому иону [ОН]1– следующего слоя (см. правые части рис. 196 и 197).
|
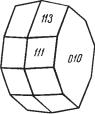
Облик кристаллов шестиугольно таблитчатый (рис. |
|
198). Распространены сложные двойниковые сростки по не |
|
скольким законам, обычно по (100) и (110). Чаще наблюда |
Рис. 198. |
ется в лучисто листовых агрегатах, иногда в виде сфероли |
Кристалл |
товых корок или в виде бобовидных или шаровидных |
гиббсита |
конкреций. В главной же своей массе на земной поверхнос |
ти распространен в тонкочешуйчатых или скрытокристаллических массах. Цвет гиббсита белый или он слабо окрашен в сероватый, зеленова тый и красноватый оттенки. Блеск стеклянный, на плоскостях спайнос
ти перламутровый. Ng = 1,587, Nm = 1,566 и Np = 1,566.
Твердость 2,5–3,5. Спайность весьма совершенная по базопинакоиду {001}. Уд. вес 2,43. Прочие свойства. При нагревании сначала превраща ется в бёмит — AlOOH, затем, при прокаливании до 950 °С, в γ Аl2О3 (ку бической структуры типа шпинели).
Диагностические признаки. Для гиббсита характерными признака ми являются следующие: весьма совершенная спайность, стеклянный блеск и малый удельный вес. От похожего на него диаспора отличается по твердости (у диаспора 6–7). От слюды отличается по удельному весу
иоптическим свойствам (слюды оптически отрицательны).
П.п. тр. не плавится; выделяя ОН, белеет и становится непрозрачным. Гид роксил при этом теряется в два этапа: 1) при температуре 196–202° (превра щение в бёмит); 2) при температуре 510 °С (дальнейшая дегидратация). Про каленный, будучи смочен раствором Co, окрашивается в ярко синий цвет. Как
игидраты других металлов, переходит в раствор в солянокислой вытяжке.
Происхождение и месторождения. Образуется при разложении
игидролизе алюминийсодержащих силикатов отчасти при гидротермаль' ных процессах (при сравнительно низких температурах), но главным об разом при экзогенных процессах выветривания, и притом преимуществен но в условиях жаркого климата в тропических и субтропических странах.
Гиббсит гидротермального происхождения встречается сравнитель но редко и в очень небольших количествах. Он наблюдается в некоторых

Раздел IV. Окислы (оксиды) |
373 |
эндогенных месторождениях как один из последних минералов, образо вавшихся из низкотемпературных гидротермальных растворов.
При процессах выветривания в жарких странах гидраты глинозема,
втом числе и гиббсит, образуются обычно совместно с гидратами железа. Гиббсит в значительно больших количествах присутствует в так называ емых латеритах1, т. е. продуктах выветривания, широко распространен ных в пределах современных тропических стран в виде покрова на корен ных горных породах и состоящих в основном из гидроокислов, содержащих
Fe2O3 и в меньшей степени Аl2О3 и SiO2. Он наблюдается и в бокситах, состоящих преимущественно из гидратов Al и образующихся также оса' дочным путем в водных бассейнах, очевидно, при размыве коры выветри вания горных пород.
Образование бокситов для ряда месторождений приписывают также процессам разложения известняков и доломитов в экзогенных условиях, допуская, что глинистые остатки от выщелачивания могли в щелочной среде подвергаться дальнейшему разложению с выносом освободивше гося кремнезема.
При процессах регионального метаморфизма гиббсит, обезвоживаясь, переходит в диаспор, а в более глубинных условиях — в корунд (наждак)
или, в присутствии SiO2, — в силикаты алюминия, или алюмосиликаты. Как спутник диаспора гиббсит установлен в месторождениях боксита
вТихвинском районе Ленинградской области и в других местах. Кристал лы гиббсита до 5 см в поперечнике, имеющие минералогическое значе ние, были встречены среди гидротермальных образований в Шишимских и Назямских горах в Златоустовском районе (Ю. Урал) среди метамор фических сланцев, а также в виде продуктов изменения нефелина в пег матитах Вишневых гор (Ср. Урал).
Практическое значение. Гиббсит, так же как и диаспор и бёмит, вхо дящие в состав бокситов, является источником глинозема, из которого, как известно, выплавляется один из наиболее легких металлов — алюми ний. Для этих целей используются бокситы с содержанием кремнезема не выше 10–15 %.
Вхимической промышленности применяются маложелезистые (свет лой окраски) бокситы с целью получения солей алюминия, главным об разом сульфатов. Более низкие сорта бокситов используются для произ водства абразивов (алунда и алоксита). Из них изготовляются также огнеупоры для высокотемпературных печей (температура плавления выше 2000 °С). Возрастает применение специальных сортов бокситов в качестве адсорбента при очистке нефтяных и растительных масел, для изготовления красок, в качестве катализаторов и пр.
1 «Латер» — кирпич (продукты выветривания по своему цвету напоминают хорошо обожженный кирпич).
374 |
Описательная часть |
САССОЛИН — B[ОН]3. Сингония триклинная; пинакоидальный в. с. Наблюдается в тонкочешуйчатых, шестигранно таблитчатых бесцвет ных или слабоокрашенных кристалликах. Блеск стеклянный, на плоско стях спайности перламутровый. Оптически отрицательный. Ng = 1,459, Nm = 1,456 и Np = 1,340.
Твердость 1. Спайность весьма совершенная по {001}. Уд. вес 1,48. Легко плавится. Пламя окрашивает в зеленый цвет. В холодной воде ра створяется плохо, обладает слабосолоноватым холодящим вкусом.
Выделяется в виде белых выцветов как продукт деятельности фума рол в вулканических районах: в больших количествах на о. Вулкано (Ли парские острова, у северо восточного конца о. Сицилия), в трещинах вул кана Авача на Камчатке и других местах. Впервые был найден в Сассо в Тоскане (Италия). В растворенном состоянии гидрат бора часто устанав ливается в нефтяных водах и в выбросах грязевых вулканов (на Керчен ском полуострове и на Кавказском побережье Каспийского моря).
3. Группа лепидокрокита–гётита
Сюда относятся так называемые моногидраты трехвалентных метал лов. Al, Fe, Mn и Со. Эти соединения диморфны; кристаллизуются оба полиморфа в ромбической сингонии.
К подгруппе лепидокрокита (FeOOH) относится его алюминиевый аналог— бёмит (AlOOH), а к подгруппе гётита (HFeO2) — диаспор (HAlO2). Здесь же опишем манганит, эмпирическая формула которого аналогична указанным соединениям, хотя по остальным признакам он имеет мало общего с ними.
БЁМИТ — γ АlООН. Назван по фамилии немецкого минералога И. Бёма (1857—1938), установившего путем рентгенометрических иссле дований присутствие этого минерала в боксите, сходного по кристалли ческой структуре с лепидокрокитом (FeOOH).
Химический состав такой же, как диаспора. Аl2О3 — 84,97 % (по фор муле). Содержит также SiO2, Fe2O3 (по видимому, в виде механической примеси опала и гидроокислов железа), а также Ga2O3.
Сингония ромбическая; ромбо дипирамидаль
|
ный в. с. Пр. гр. Amam(D18). a = 3,78; b = 11,8; с = 2,85. |
||||
|
2h |
0 |
0 |
0 |
|
|
Кристаллическая структура аналогична структуре ле |
||||
|
пидокрокита и описана ниже. Облик кристаллов. |
||||
|
В трещинах и порах среди боксита, а также продуктов |
||||
|
разложения нефелина устанавливается в виде очень |
||||
|
мелких пластинчатых или чечевицеобразных кристал |
||||
Рис. 199. Кристалл |
ликов (рис. 199), представленных обычно комбинаци |
||||
бёмита |
ями (010), (111), (113), {110} и др. Характерно, что гра |
||||
из Вишневых гор |
ни {010} являются блестящими, а грани остальных |
||||
(по Э. М. Бонд |
|||||
форм матовыми. Обычно же распространен в виде |
|||||
штедт Куплетской) |
|||||
Раздел IV. Окислы (оксиды) |
375 |
скрытокристаллической массы или в колломорфных образованиях (в бокситах).
Цвет. Бесцветный или белый с желтоватым оттенком. Средний показа тель преломления для скрытокристаллических разностей равен 1,640–1,645.
Твердость 3,5. Спайность совершенная по {010}. Уд. вес 3,01–3,06. При прокаливании превращается в γ Аl2О3 (кубическую модификацию, крис таллизующуюся в структуре шпинели).
Диагностические признаки. Ввиду ничтожности размеров кристалликов наиболее надежно устанавливается рентгеновским методом. От диаспора от личается меньшим показателем преломления и более низкой твердостью.
П. п. тр. не плавится, белеет и расщепляется по спайности. В стеклян ной трубке выделяет воду. В кислотах нерастворим.
Происхождение и месторождения. Некоторое время бёмит был из вестен лишь в экзогенных месторождениях боксита (см. гиббсит). Он встречен в древней коре выветривания в Яковлевском месторождении (КМА) в ассоциации с каолинитом на метаморфических сланцах желе зо магнезиально глиноземистого состава. Позже он был установлен как низкотемпературный гидротермальный минерал в виде мелких кристал ликов (см. рис. 199) в пустотах среди пегматитов щелочных пород в Виш' невых горах (Ср. Урал) в ассоциации с водяно прозрачным гиббситом на игольчатых кристаллах цеолита (натролита). Он образовался, по види мому, в результате гидротермального изменения нефелина.
ЛЕПИДОКРОКИТ — γ FeOOH. От греч. лепидос — пластинка, кро' кос — шафран. Синоним: рубиновая слюдка.
Химический состав тождествен составу гётита. Согласно имеющим ся анализам, примесей гораздо меньше, чем в гётите. Так же как и для гётита существуют разности, содержащие адсорбированную воду (в тон кокристаллических колломорфных массах), носящие название гидроле пидокрокита — FeOOH . aq.
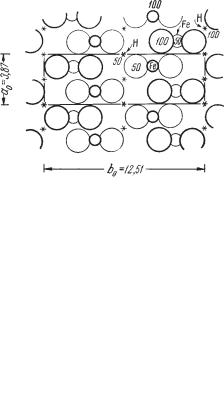
Сингония ромбическая; ромбо дипирамидальный в. с. Пр. гр. Атат(D172h). а0 = 3,87; b0 = 12,51; с0 =3,06. Кристаллическая структура. Как можно видеть на рис. 200, катионы Fe3+ находятся в шестерном окруже нии ионов кислорода (не показаны лишь передний и задний анионы). По следние располагаются по вершинам искаженных октаэдров, связанных между собой в цепи, вытянутые параллельно оси а. Эти цепи боковыми связями (через ребра октаэдров) соединены друг с другом в непрерыв ные двойные слои параллельно (010), т. е. перпендикулярно плоскости чертежа (в вертикальном направлении). Как изображено на рис. 200, та кие двойные слои соединены друг с другом слабыми водородными связя ми в виде непрерывных зигзагообразных шнурков: —О—Н—О—Н—О—. Каждый примыкающий к Н ионам анион О2–, с одной стороны, связан
сдвумя катионами Fe3+, получая от них по 1/2 валентности, с другой —
сдвумя Н катионами, в результате чего имеет место полное насыщение его валентности.
376 |
Описательная часть |
||
|
|
Что касается анионов О2–, распо |
|
|
|
ложенных внутри двойных слоев |
|
|
|
(рис. 200), то их валентность также |
|
|
|
полностью удовлетворяется долями |
|
|
|
валентностей, отдаваемых катиона |
|
|
|
ми Fe3+ (каждый анион O окружен |
|
|
|
четырьмя катионами Fe). Таким об |
|
|
|
разом, в строении структуры лепи |
|
|
|
докрокита принимают участие два |
|
|
|
типа ионов кислорода, и формулу |
|
Рис. 200. Кристаллическая структура |
этого минерала поэтому приходится |
||
писать в виде FeOOH. Гидроксиль |
|||
лепидокрокита — FeOOH. Крупные |
ные ионы как таковые отсутствуют в |
||
кружки — ионы кислорода, малые |
|||
структуре. В структуре же гётита |
|||
кружки — ионы Fe3+. Звездочками |
|||
показаны вероятные положения иона Н1+ |
(HFeO2) все кислородные ионы хи |
||
|
|
мически эквивалентны. Упаковка |
|
|
ионов в структуре лепидокрокита менее плотная, что |
||
|
сказывается в меньшем его удельном весе. Облик криj |
||
|
сталлов. Лепидокрокит встречается в виде пластин |
||
|
чатых по (010) кристалликов в пустотах (рис. 201) но |
||
|
чаще в виде тонкочешуйчатых или волокнистых аг |
||
|
регатов. Наблюдались и почковидные агрегаты на |
||
|
стенках жеод. |
|
|
|
Цвет лепидокрокита темно красный до красновато |
||
Рис. 201. Кристалл |
черного; иногда с золотистым оттенком (в чешуйчатых |
||
массах). Черта оранжеваяиликирпично красная. Блеск |
|||
лепидокрокита: |
|||
алмазный. В тонких шлифах прозрачен. Ng = 2,51, |
|||
а {100}, b {010}, |
|||
Nm = 2,20 и Np = 1,94. |
|||
с {001}, d {201}, w {031} |
|||
Твердость 4. Спайность весьма совершенная по {010} и совершенная по {001}. Уд. вес 4,09–4,10.
Диагностические признаки. Часто ошибочно принимают за гематит, особенно в плотных агрегатах. Отдельные пластинки лепидокрокита легко узнаются по форме кристалликов, просвечиваемости их красным цветом, оранжево красной или красной черте и малому удельному весу (отличие от гематита).
П. п. тр. не плавится; при высоких температурах становится черным, магнитным. В стеклянной трубке выделяет воду. В HCl растворяется.
Происхождение и месторождения. Лепидокрокит в виде пластинча тых кристалликов (рубиновой слюдки) иногда наблюдается как один из наиболее поздних минералов гидротермальных месторождений, напри мер, в Зигене в Вестфалии (Германия), в жильных железорудных место рождениях Ангаро'Илимского района (в пустотах тонких кварцевых про жилков) и в других случаях. Гораздо чаще он наблюдается в виде
Раздел IV. Окислы (оксиды) |
377 |
концентрических слоев чешуйчатых агрегатов в экзогенных бурых же лезняках или на стенках жеод поверхностного происхождения: в Поле' таевских месторождениях (к юго западу от Челябинска), в окрестностях Липецка и в других местах.
Как по данным микроскопических исследований, так и по данным рент генометрического изучения продуктов, образующихся при систематиче ском нагревании, оказывается, что лепидокрокит способен переходить в гётит. Условия, при которых происходят эти превращения, а также усло вия образования в природе различных модификаций моногидрата окиси железа еще не изучены. Вероятно, здесь играет роль степень кислотности среды (pH), при которой происходит образование гидратов окиси железа.
ДИАСПОР — HAlO2. От греч. диаспор — рассеяние (некоторые об разцы при нагревании, растрескиваясь, распадаются на мелкие частич ки). Впервые установлен еще в позапрошлом столетии на Урале.
Химический состав. Аl2О3 — 85 %, Н2О — 15 %. Известны разности, содержащие в виде изоморфной примеси Fe2O3 (до 7 %), Мn2О3 (Mn ди аспор), Cr2O3 (до 5 %) и SiO2 (до 4 %). Устанавливается также повышен ное содержание Ga2O3 (до нескольких сотых процента).
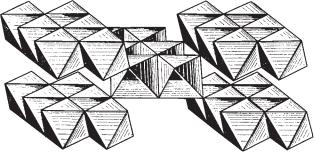
Сингония ромбическая; ромбо дипирамидальный в. с. 3L23РС. Пр. гр. Pbnm(D162h). a0 = 4,40; b0 = 9,36; с0 = 2,84. Кристаллическая структура изобра жена на рис. 202. Она характеризуется плотной гексагональной упаковкой ионов О2–, причем ионы Al3+ размещаются в октаэдрических пустотах, т. е. между шестью ионами О. Каждый ион кислорода связан с тремя ионами Аl, т. е. координационные числа для Аl и О те же, что и в кристаллической структуре рутила (6 и 3). Протоны Н1+ располагаются, вероятно, между парами ионов кислорода (рис. 202) и в силу совершенной ничтожности своих размеров не требуют какого либо особого пространства в кристал лической структуре. Таким образом, практически структура диаспора сло жена ионами Аl и О в отношении 1 : 2 (как в рутиле). Сходство с рутилом, как показал Н. В. Белов, заключается и в самих структурах этих минера лов, с той разницей, что в диаспоре (гётите) вместо одинарных колонок из структуры рутила вдоль оси с тянутся сдвоенные колонки — фрагменты
Рис. 202. Кристаллическая структура диаспора в полинговских полиэдрах
378 |
Описательная часть |
|
|
|
плотнейшей упаковки. Этим объясня |
|
|
ются досковидный облик кристаллов, |
|
|
спайность и коленчатые двойники с уг |
|
|
лом около 122°. |
|
|
Облик кристаллов. Встречающи |
|
|
еся кристаллы имеют тонкопластин |
|
|
чатые, иногда таблитчатые по (010) |
|
|
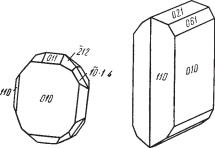
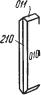
формы (рис. 203), нередко столбчатые |
|
|
по оси с. Наблюдается вертикальная |
|
Рис. 203. Кристаллы диаспора. |
штриховатость граней. Обычно рас |
В левой фигуре вторая ось направлена |
пространен в листоватых или тонко |
|
|
к наблюдателю |
чешуйчатых агрегатах. |
|
|
|
Цвет диаспора бесцветный, белый, желтовато бурый, светло фиолето вый, зеленый, зеленовато серый. Блеск стеклянный, на плоскостях спай ности перламутровый. Черта белая. Ng = 1,750, Nm = 1,722 и Np = l,702.
Твердость 6–7. Очень хрупкий. Спайность по {010} ясная. Уд. вес 3,3– 3,5. При прокаливании переходит в α Аl2О3 (корунд).
Диагностические признаки. Для диаспора характерны листоватые агрегаты, высокая твердость (отличие от гиббсита, слюд и др.). Смешать можно только с некоторым почти не различимыми по внешним призна кам разностям хлоритоида (ортосиликата Fe, Mg и Аl), встречающегося иногда совместно с ним и корундом в метаморфических породах. В отли чие от него диаспор не разлагается в H2SO4 и, кроме того, отличается по некоторым оптическим свойствам.
П. п. тр. не плавится. В кислотах и КОН не растворяется. В H2SO4 раз лагается лишь после сильного прокаливания. В пробирке при накалива нии распадается на мелкие белые чешуйки.
Происхождение и месторождения. Изредка встречается в некоторых
контактово'метасоматических и гидротермальных месторождениях сре ди мраморизованных известняков в ассоциации с корундом, мусковитом, гематитом, рутилом и др.
Вбольших массах в виде тонкочешуйчатых агрегатов распространен
вэкзогенных месторождениях бокситов в парагенезисе с гиббситом, бё митом и др.
Часто встречается в метаморфических породах совместно с корундом, хло ритоидом и другими минералами (в месторождениях наждака, вероятно, как продукт метаморфизма бокситов), иногда в кристаллических сланцах как породообразующий минерал в сопровождении кианита и других минералов.
Вассоциации с корундом и алюмосиликатами встречается в место рождениях наждака на Урале: Косой Брод (около Екатеринбурга) в мра моризованных известняках, по р. Борзовке (Кыштымский район).
Наблюдается также в месторождении Акташ (Узбекистан) в ассоци ации с дюмортьеритом, пирофиллитом, алунитом и корундом, а также
вдругих местах.
Раздел IV. Окислы (оксиды) |
379 |
В крупных пластинках и кристаллах распространен в наждачных ко пях Честер в Массачусетсе (США), на о. Наксос (Греция) и в месторож дениях Милас и Селкук (Турция).
О практическом значении бокситов см. выше (гиббсит).
ГЁТИТ — HFeO2. Гётит назван в честь поэта Гёте (1749–1832). Пер воначально этот минерал был назван онегитом (по месту нахождения на Волк'острове в Онежском озере), но так как его свойства не были описаны, это название не привилось в минералогической литературе. Синоним: «игольчатая железная руда» (в немецкой литературе). Явля ется главной составной частью такого неоднородного, но широко рас пространенного и общеизвестного минерального образования, каким яв ляется лимонит (гидрогётит) — HFeO2 . aq.
Название лимонит происходит от греческого слова лемон — луг (име лись в виду луговые и болотные руды гидроокислов железа).
Химический состав. Fe2O3 — 89,9 %, Н2О — 10,1 %. Содержание воды часто бывает выше, чем полагается по формуле: до 12–14 % (лимонит). В связи с этим раньше выделяли несколько минеральных видов, отлича ющихся друг от друга по содержанию воды и некоторым физическим свой ствам. Рентгенометрически установлено, что в действительности суще ствует одно соединение с отношением Fe2O3 : Н2О = 1 : 1, обладающее определенной кристаллической структурой. Все более богатые водой разности гидроокислов железа по существу являются гидрогелями и со держат адсорбированную воду в разных количествах (в зависимости от сте пени дегидратации). Поэтому лимонит не является отдельным минераль ным видом, представляя собой гидратированную разновидность гётита.
Так называемый турьит по рентгенометрическим и термическим ис следованиям оказался смесью гётита с гидрогематитом и не принадле жит к числу самостоятельных минералов.
Скопления природных гидроокислов железа в своей массе, как пра вило, представляют собой гидратированные смеси гётита с лепидокро китом, а также гидроокислами кремнезема, глинистым веществом и др.
Такие смеси обычно называются бурыми железняками. |
|
Сингония ромбическая; ромбо дипирамидальный в. с. Пр. |
|
гр Pbпт. а0 = 4,64; b0 = 10,0; с0 = 3,03. Кристаллическая струкj |
|
тура аналогична структуре диаспора. Облик кристаллов и агj |
|
регаты. Редко встречающиеся кристаллы имеют игольчатый |
|
или столбчатый облик (рис. 204). Может давать двойники, |
|
аналогичные коленчатым двойникам рутила по (011). Обыч |
|
но наблюдается в скорлуповатых, почковидных или сталак |
Рис. 204. |
титовых формах (см. рис. 45) с тонким радиально или па |
Кристалл |
раллельно волокнистым строением в изломе («игольчатая |
гётита |
железная руда») или в сплошных плотных, пористых ноздреватых, шла ковидных, порошковатых массах. Распространены псевдоморфозы по
380 |
Описательная часть |
кристаллам пирита и другим сульфидам железа. Встречается также в виде оолитов, бобовин, конкреций и жеод.
Цвет лимонита и гётита темно бурый до черного. Порошковатый или охристый лимонит, нередко образующийся при физическом выветрива нии за счет плотного черного лимонита и силикатов железа, обладает до вольно светлым желто бурым цветом. Как показали сравнительные хи мические и рентгенометрические исследования, эта охристая разность ничем особенным не отличается от плотного лимонита. Черта гётита бу рая с красноватым оттенком. Лимонит большей частью имеет светло бу рую или желто бурую окраску. Блеск гётита алмазный до полуметалли ческого. На поверхности почковидных или сталактитовых масс лимонита часто обнаруживается гётит в виде блестящих смоляно черных тонких корочек. Nm = 2,35–2,39.
Твердость гётита 4,5–5,5, лимонита — 4–1 (в зависимости от физи ческого состояния). Спайность гётита по {010} совершенная. Уд. вес гё тита 4,0–4,4, у лимонита колеблется от 3,3 до 4,0.
Диагностические признаки. Гётит и лимонит сравнительно легко уз наются по неяснокристаллическим формам выделения, бурой черте
ижелто бурым охристым примазкам.
П.п. тр. плавятся; при продолжительном нагревании становятся силь но магнитными. В стеклянной трубке выделяют воду, краснеют, превра
щаясь в безводную Fe2O3. В HCl медленно растворяются.
Происхождение и месторождения. Гётит в виде игольчатых или столбчатых кристалликов крайне редко наблюдается как эндогенный ми нерал: в пустотах мелафиров, в аметистовых жеодах на Волк'острове (Онежское озеро, Карелия); в пустотах пегматитовых жил Волыни (Ук раина), иногда в гидротермальных месторождениях как один из наибо лее низкотемпературных минералов в пустотах, например в Пршибраме (Чехия), в ассоциации с более ранними, не затронутыми выветриванием сфалеритом и пиритом.
В главной же массе гётит и лимонит распространены как экзогенные минералы и притом почти исключительно в виде колломорфных или зем листых масс. Они образуются преимущественно в результате гидролиза солей возникающих при окислении и разложении железосодержащих ми нералов: сульфидов, карбонатов, силикатов и других, в которых железо при сутствует в двухвалентной форме. Образование гидроокислов железа на поверхности мы наблюдаем буквально всюду и притом в самых различных видах. В значительных массах бурые железняки образуются в зонах окис ления сульфидных месторождений. Это так называемые железные шляпы, представленные рыхлыми, комковатыми и плотными массами, состоящи ми главным образом из лимонита, гётита, иногда лепидокрокита и др.
Большие массы гидроокислов железа заключены в осадочных место рождениях бурых железняков молодого (неогенового) возраста, образо
