
- •Лекция 12
- •СТАБИЛИЗАЦИЯ СТРУКТУРНО-ФАЗОВОГО СОСТОЯНИЯ МАТЕРИАЛОВ
- •СТАБИЛИЗАЦИЯ СТРУКТУРНО-ФАЗОВОГО СОСТОЯНИЯ МАТЕРИАЛОВ
- •1. Проблемы стабильности структурно-фазового состояния материалов
- •1.Проблемы стабильности структурно-фазового состояния материалов
- •1.Проблемы стабильности структурно-фазового состояния материалов
- •1.Проблемы стабильности структурно-фазового состояния материалов
- •2. Движущие силы изменения структурно-фазового состояния
- •2. Движущие силы изменения структурно- фазового состояния
- •2. Движущие силы изменения структурно-фазового состояния
- •3. Основные механизмы изменения структурно-фазового состояния
- •3. Основные механизмы изменения структурно-фазового состояния
- •4. Нестабильность СФС, вызванная изменением химической составляющей
- •4.1. Нестабильность, вызванная неравномерным распределением растворенных компонентов
- •4.2.Внутрикристаллитная ликвация и междендритная сегрегация атомов
- •4.2.Внутрикристаллитная ликвация и междендритная сегрегация атомов
- •4.2.Внутрикристаллитная ликвация и междендритная сегрегация
- •4.2.Пути устранения ликвации и сегрегации атомов
- •Проблемы гомогенизации (продолжение):
- •4.3. Распад пересыщенного твердого раствора
- •Особенности спинодального распада
- •4.3. Распад пересыщенного твердого раствора
- •Зарождение частиц второй фазы
- •Гетерогенное зарождение второй фазы
- •Образование переходных фаз
- •Влияние примесей на зарождение выделений второй фазы
- •Рост выделений из пересыщенного твердого раствора
- •Рост выделений, контролируемый диффузией
- •Рост выделений, контролируемый диффузией
- •концентрации компонента В при росте выделения во времени t в направлении Х (Ri
- •Растворение, контролируемое диффузией
- •Роль кинетики реакций на поверхности раздела
- •Управление распадом твердых растворов
- •Управление распадом твердых растворов
- •Управление распадом с целью упрочнения сплава
- •5. Нестабильность структуры, обусловленная влиянием энергии деформации
- •5.1. Запасенная энергия холодной деформации
- •5.2. Механизмы накопления энергии деформации
- •5.2. Механизмы накопления энергии деформации
- •Фильм по процессам в деформированном материале
- •5.3. Возврат
- •Механизмы возврата
- •Модели зарождения новых зерен
- •Модели зарождения новых зерен
Лекция 12
Модуль 3. Структура и ее роль в обеспечении заданного комплекса свойств материалов.
Тема 3.4. Стабилизация структурно-фазового состояния материалов
СТАБИЛИЗАЦИЯ СТРУКТУРНО-ФАЗОВОГО СОСТОЯНИЯ МАТЕРИАЛОВ
Равновесное состояние сплавов - это частным случаем реального термодинамически нестабильного состояния, в котором эксплуатируется большинство материалов.
Более того, сложнолегированные материалы с заданным уровнем свойств почти во всех случаях термодинамически нестабильны, а равновесное состояние не всегда является оптимальным с точки зрения свойств материала.
Учитывая, что свойства в значительной степени определяются структурно-фазовым состоянием (СФС) материалов, целесообразно рассматривать относительную стабильность материала, т.е. сохранение СФС и, следовательно, свойств в реальных условиях в течение всего времени работы материала.
Заданную структуру обычно получают, комбинируя определенным образом операции деформации, термообработки и диффузионного отжига, причем происходящие превращения искусственно затормаживаются, как правило, охлаждением до комнатной температуры в выбранный момент времени.
Например, материалы, полученные посредством
СТАБИЛИЗАЦИЯ СТРУКТУРНО-ФАЗОВОГО СОСТОЯНИЯ МАТЕРИАЛОВ
(ПРОДОЛЖЕНИЕ)
Например, материалы, полученные посредством плавления и литья, обладают далеко не оптимальной (литой) структурой, для разрушения которой и гомогенизации состава традиционно
применяют термомеханическую (ТМО) или многократную термомеханическую (МТМО) обработки
Механическая обработка может быть холодной (Тобр < Трекр) или
горячей
(Тобр > Трекр). Последующий нагрев стимулирует рекристаллизацию, т.е. получение заданного размера зерна.
Реальные материалы, обладающие избытком свободной энергии, нестабильны или относительно стабильны. Всегда могут протекать процессы, связанные с увеличением энтропии ( S max) и уменьшением свободной энергии материала ( G min)
Если исходное СФС было оптимальным, то эти изменения будут приводить к ухудшению состояния и свойств материала.
1. Проблемы стабильности структурно-фазового состояния материалов
G |
|
G |
GA1 |
|
Сплав |
||
|
|
||
Металл |
Коррозия |
G1 |
GA2 |
Руда |
|
G2 |
GA3 |
|
|
||
|
|
|
|
|
Время |
|
Время |
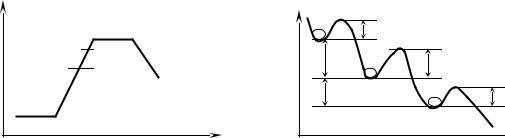
Представление о присущей металлическим материалам нестабильности показано на рис. 1,а на примере изменения свободной энергии атомов при переходе из руды в металл или сплав ( G возрастает), а затем – при коррозии ( G уменьшается).
С этой точки зрения состояние атомов в руде является наиболее стабильным, и металл неизменно стремится вновь перейти в более стабильное химическое состояние, отличающееся от металлического.
Изменение уровня свободной энергии атомов при переходе в более стабильное состояние показано на рис. 1,б. Меньшему уровнюG соответствует более стабильное состояние атома.
1.Проблемы стабильности структурно-фазового состояния материалов
G |
|
G |
(продолжение) |
|
|
|
||
|
Сплав |
|
GA1 |
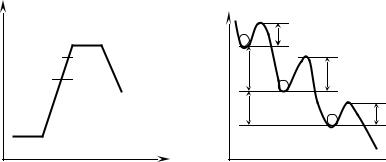
Для перехода в более стабильное |
||||
Металл |
Коррозия |
G1 |
GA2 |
|||||
состояние (меньшее по G) |
||||||||
|
|
|
GA3 |
|||||
|
|
G2 |
требуется активировать процесс и |
|||||
|
|
|
|
|
|
|
||
Руда |
|
|
|
преодолеть |
тот |
или |
иной |
|
|
|
|
|
|||||
|
Время |
|
Время |
потенциальный барьер ( GА). |
|
|||
Дополнительную свободную энергию, необходимую для перехода из одного положения в другое, атом получает за счет тепловых флуктуаций.
Величина Gi (как и Si) указывает общее направление процесса
взаимодействия атомов: чем меньше уровень свободной энергии, тем стабильнее положение атомов и СФС.
Кинетика процесса перестроения атомов (и СФС) будет определяться энергией активации (GAi) этого процесса. В большинстве
практических случаев GA > kТ, так что скорость преодоления
энергетического барьера очень мала.
Хорошо известно, что скорость того или иного термически активируемого процесса перехода атомов из одного состояния в другое
определяется энтальпией активации ( HAi = GAi + Т SAi) и температурой: |
|||
. |
|
Ае |
Н |
v |
kT |
||
|
перех |
|
|
1.Проблемы стабильности структурно-фазового состояния материалов
(продолжение)
Скорость перехода весьма чувствительна к температуре: Пример: энергия активации НА= 2 эВ/ат. T = 300 K , то 10–33
T = 1000 K, то 10–10
Скорость перехода увеличится на 23 порядка: это 1 с и 3 1014 лет, а температура возрасла всего на 700 К. Переходы заметны при Т 0,3Тпл.
Нестабильности СФС:
-метастабильность (промежуточные менее стабильные состояния с повышенной энергией, отделенные одно от другого потенциальным барьером. Наличие барьера вызвано, например, зарождением и ростом зародыша новой фазы (зерна) до критического размера;
-истинная нестабильность - выход из этого состояния безбарьерный, исходное нестабильное СФС может переходить в другое состояние без предварительного увеличения энергии.
.
1.Проблемы стабильности структурно-фазового состояния материалов
(продолжение)
В реальности перестроение СФС обусловлено движением атомов в решетке твердого тела, а для этого необходима активация этого движения.
Разница между двумя типами стабилизации СФС состоит в том, что при метастабильных превращениях в стадии активации участвует множество атомов, тогда как для превращения второго типа достаточна последовательная активация лишь одного атома.
Величины избытка свободной энергии состояния одного атома ( G1 ) над другим ( G2) более стабильным можно рассматривать как
относительные движущие силы процесса перехода атомов в более стабильное состояние.
Чем больше по абсолютной величине G, тем больше стимул к
переходу системы в новое состояние.
2. Движущие силы изменения структурно-фазового состояния
Причиной изменения СФС материала могут быть внутренние и внешние факторы:
-внутренние факторы, приводящие к избытку свободной энергии и
снижению стабильности системы – это:
-неравномерное распределение компонентов в сплаве; -пересыщение твердого раствора; -наличие разнозеренной микроструктуры;
-наличие второй фазы, границ раздела фаз, зерен и субзерен; -дефекты микроструктуры; -остаточные напряжения и др.
-внешние факторы, приводящие к избытку свободной энергии, - это действующие на твердое тело:
-тепловые потоки (рост температуры); -внешнее давление; -воздействие среды;
-воздействие физических полей, включая облучение материала, действие электромагнитных полей и др.
2. Движущие силы изменения структурно- фазового состояния
(продолжение)
Избыток свободной энергии условно представляют в виде трех слагаемых: избытка химической энергии, поверхностной энергии и энергии деформации, т.е.
G = Gхим + Gпов + Gдеф.
Химическая составляющая изменения например при изменении температуры: -плавление или кристаллизация
-гомогенизация твердого раствора -образование второй фазы
свободной энергии,
( Gхим 13 кДж/моль); ( Gхим 5,7 кДж/моль). ( Gхим 1250 Дж/моль).
Таким образом, химическая составляющая изменения свободной энергии имеет величины порядка ~ кДж/моль.
2. Движущие силы изменения структурно-фазового состояния
(продолжение)
G = Gхим + Gпов + Gдеф.
Типичные величины «поверхностной» и «деформационной» составляющих изменения свободной энергии значительно меньше химической части.
Например, при увеличении деформации меди от 10 до 120 % запасенная энергия в металле с исходным зерном 30 мкм возрастает от 10,5 до 50,6 Дж/моль.
Изменение свободной энергии при увеличении размера мелкодисперсных выделений (снижении площади межфазной поверхности) составляет порядка 20 Дж/моль.
Таким образом, движущие силы, вызванные деформациями или межфазными поверхностями, имеют в целом небольшие значения по сравнению с возникающими за счет химической свободной энергии, т.е. Gхим >> Gдеф Gпов.
