
Орг химия / 1-10_Nomenklatura_svyazi_izomeria
.pdf
1) КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Каждый период развития органической химии отмечен попытками ученых каким-то образом привести разнообразие химических соединений в единую систему.
Важнейшими признаками, которые положены в основу современной классификации органических соединений, являются строение углеродной цепи и природа функциональных групп.
Классификация по строению углеродной цепи
В зависимости от расположения углеродных атомов в молекуле органические соединения делят на несколько больших групп.
Различают два типа органических соединений: ациклические и циклические. Ациклические или алифатические (отдревнегреч. алифар– жир) – вешества с открытой (незамкнутой) цепью, другое их название – соединения жирного ряда. По строению углеводородной цепи среди ациклических соединений различают; насыщенные (предельные) вешества, содержащие только простые углерод-углеродные связи и ненасыщенные (непредельные) алифатические – структуры с кратными (двойными,тройными) углерод-углеродными связями.
К циклическим относятся соединения, содержащие в своей структуре замкнутые цепи атомов – циклы (от греч. циклос – круг). Природа атомов, входящих в цикл, лежит в основе деления всех циклических соединений на две большие группы: карбоци клические и гетеро циклические. В молекулах карбоциклических соединений цикл состоит только из атомов углерода. Гетероциклические соединения имеют в своей структуре циклы, содержащие наряду с атомами углерода атомы других элементов, чаще всего О, S, N.
1
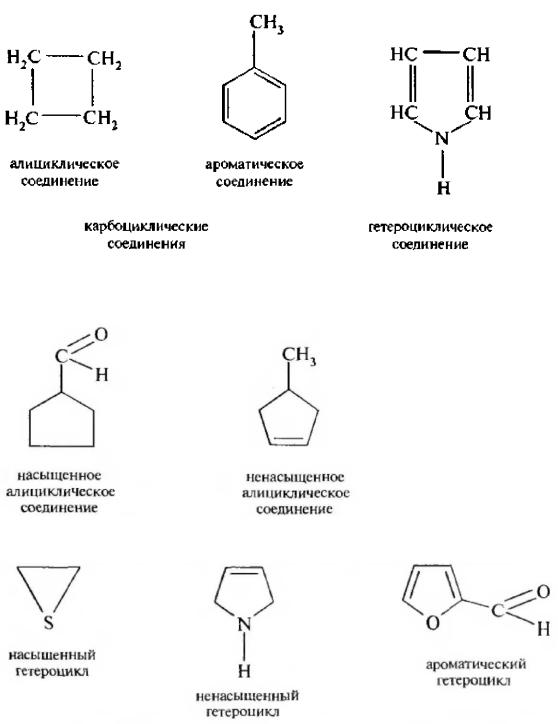
Карбоциклические соединения в свою очередь делятся на алициклические и ароматические, Алициклические структуры подобно алифатическим соединениям по степени
насыщенности подразделяются на насыщенные и ненасыщенные:
Среди гетероциклических соединений различают насыщенные, ненасыщенные и ароматические структуры:
Соединения, молекулы которых состоят только из атомов углерода и водорода, называются углеводородами. Замещение одного или нескольких атомов водорода на функциональные группы ведет к образованию других классов органических соединений.
Классификация по природе функциональной группы
Функциональная группа – структурный фрагмент молекулы, характеризующий свойства соединений данного класса. Например, свойства карбоновых кислот характеризуются наличием карбоксильной группы -СООН; в спиртах функциональная группа – спиртовый гидроксил –ОН; к аминам относятся соединения, содержащие группу -NH2 и т. д.
По количеству и однородности функциональных групп органические соединения делят на моно-, поли- и гетерофункциональные.
2

Вещества с одной функциональной группой называют монофункциональными, с несколькими одинаковыми функциональными группами – полифункциональными. Соединения, содержащие несколько различных функциональных групп, – гетерофункциональные.
Соединения одного класса объединены в гомологические ряды. Гомологический ряд – это ряд органических соединений с одинаковыми функциональными группами и однотипным строением, каждый представитель гомологического ряда отличается от предыдущего на постоянную единицу (–СН2–), которую называют гомологической разностью. Члены гомологического ряда называются гомологами.
3
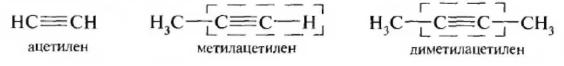
2) НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИИ
Химическая номенклатура – совокупность названий индивидуальных химических веществ, их групп и классов, а также правила составления их названий.
Соблюдать соответствия между существующей классификацией веществ и их наименованиями позволяют номенклатурные системы.
Номенклатура органических соединений складывалась на протяжении всего периода возникновения и становления органической химии как науки. Для названий органических соединений применяют несколько номенклатурных систем: тривиальную, рациональную, международную (ИЮПАК),
Тривиальная номенклатура
На первых этапах развития органической химии соединения назывались случайно. Это было связано с их нахождением в природе; щавелевая кислота, яблочная кислота и другие, или с источником их получения: древесный спирт, муравьиная кислота и др. Многие тривиальные названия прочно укоренились и до сих пор широко применяются.
Рациональная номенклатура
Воснове рациональной номенклатуры используется принцип деления органических соединений на гомологические ряды. Вещества рассматриваются как производные простейшего представителя данного ряда: для алканов -- метана, алкенов – этилена, алкинов – ацетилена и т. д., например:
Внастоящее время применение рациональной номенклатуры ограничено. Основные ее принципы нашли свое отображение в радикало-функциональной номенклатуре.
Международная номенклатура (ИЮПАК)
Первая попытка создать номенклатурную систему, которая позволяла бы дать однозначное название любому органическому соединению, была предпринята химиками в 1892 году на международном конгрессе в Женеве (женевская номенклатура). Правила современной номенклатуры были разработаны на XIX конгрессе Международной: союза теоретической и прикладной химии в 1957 году. Эти правила известны под названием номенклатуры ИЮПАК.
Номенклатурные правила ИЮПАК предусматривают несколько способов образования названий органических соединений. Наиболее широко применяются заместительная и радикалофункииональная номенклатуры.
Заместительная номенклатура
Прежде чем перейти к рассмотрению заместительной номенклатуры, дадим определение основным понятиям.
Родоначальная структура – структурный фрагмент молекулы (молекулярный остов), лежащий в основе названия соединения: главная углеродная цепь атомов для ациклических соединений, для карбо- и гетероциклических – цикл:
4

Родоначальное название может быть систематическим, тривиальным или полусистематическим.
В органической химии для sp3-гибрилизованного углерода существует такое понятие, как первичный, вторичный, третичный.
Атом углерода, связанный σ-связью только с одним атомом углерода, называется первичным, с двумя – вторичным, стремя – третичным.
Радикал – остаток углеводорода, образующийся в результате удаления одного или нескольких атомов водорода. Свободную валентность в радикалах обозначают черточкой.
По количеству свободных валентностей различают одно-, двух-, трехвалентные радикалы:
В зависимости оттого, у какого атома углерода находится свободная валентность, различают первичные, вторичные и третичные радикалы:
Заместителем называют любой атом или группу атомов, включая радикал и функциональную группу, которые не входят в родоначальную структуру.
Положение заместителей в молекуле указывают с помощью цифр или букв, которые называют локантами. Для обозначения нескольких одинаковых заместителей или кратных связей в данной
5

молекуле применяют множительные (умножающие) приставки: ди- (два), три- (три), тетра- (четыре), пента- (пять) и т д.
Согласно заместительной номенклатуре органические соединения рассматривают как производные углеводородов, в молекулах которых один или несколько атомов водорода замешены на другие атомы или атомные группы.
Составление названий проводят в определенном порядке:
1. Среди всех функциональных групп, имеющихся в соединении, выбирают старшую. Следующие группы перечисляют в порядке уменьшения их старшинства:
В названии органического вещества лишь старшая функциональная группа обозначается в суффиксе, все остальные – в префиксе, но некоторые функциональные группы всегда находят свое отражение в префиксе:
Их не рассматривают по старшинству.
2.Устанавливают родоначальную структуру. Если соединение содержит кратные связи, то они должны войти в родоначальную структуру,
3.Проводят нумерацию атомов родоначальной структуры таким образом, чтобы старшая функциональная группа получила по возможности меньший номер,
4.Составляют название соединения в целом: первым указывают в алфавитном порядке функциональные группы (кроме старшей) и углеводородные радикалы в префиксе, затем – название родоначальной структуры в корне и в конце названия – старшую функциональную группу в суффиксе.
Степень насыщенности обозначается специальными суффиксами: -ан – для насыщенных, -ен – для двойной, -ин – для тройной связи.
Локанты, буквенные или цифровые, и множительные приставки располагают перед названием заместителей или кратных связей.
Пример составления названий:
6

Радикало-функциональная номенклатура
В основе радикало-функииональной номенклатуры лежит название класса (спирт, кетон и др), перед которым перечисляют названия радикалов и функциональных групп (кроме старшей), например:
Родоначальную структуру чаще обозначают с помощью тривиального названия, а положение радикалов – с помощью буквенных локантов; α, β, γ, δ (греческий алфавит). Буквой α обозначают ближайший к старшей функциональной группе атом углерода.
В дальнейшем при изучении различных классов органических соединений мы расширим приведенные краткие пояснения на многочисленных примерах.
7

3) ТИПЫ ХИМИМЧЕСКИХ СВЯЗЕЙ
Остановимся на одном из важнейших вопросов химии, как осуществляется связь атомов в молекулах? Используя знания, полученные в курсе неорганической химии, рассмотрим вопросы природы химической связи между атомами или типы химических связей.
Современная теория химической связи базируется на квантово-механических представлениях о строении молекулы. предложили в 1916 г. немецкий ученый В. Косселъ и американский ученый Дж. Н.Льюис, Авторы электронной теории выдвинули идею о том, что химическая связь – результат взаимодействия внешних электронных оболочек атомов. Согласно электронной теории химической связи, образуя химическую связь, каждый атом стремится заполнить внешнюю электронную оболочку до конфигурации, присущей инертным газам. При этом он принимает участие в образовании общей электронной пары, отдает или принимает электроны. Принцип заполнения валентных оболочек до конфигурации инертных газов получил название октетное правило.
ТИПЫ ХИМИЧЕСКИХ СВЯЗЕЙ
Согласно принятой в настоящее время классификации существует несколько типов химической связи: ионная, ковалентная, водородная, металлическая и др. По способу образования химической связи различают две основные: ионную и ковалентную.
ИОННАЯ СВЯЗЬ
Ионная связь – характерна для атомов значительно отличающихся по электроотрицательности. Ионный тип связи характерен для неорганических соединений.
Рассмотрим, как осуществляется связь в хлориде натрия:
Хлор по сравнению с натрием обладает большей электроотрицательностью, то есть большим сродством к электрону. Вследствие этого электрон переходите внешней оболочки натрия на внешнюю оболочку хлора, при этом образуются положительный и отрицательный заряды, между которыми действуют силы электростатического притяжения. Ион натрия приобретает электронную конфигурацию неона, а нон хлора – конфигурацию аргона.
Соединения с ионной связью характеризуются относительно большим дипольным моментом, хорошей электропроводимостью, высокими температурами плавления.
КОВАЛЕНТНАЯ СВЯЗЬ
Ковалентная связь – основной тип связи в органических соединениях, характеризующийся увеличением электронной плотности меж ду химически связанными атомами в молекуле по сравнению с распределением электронной плотности в свободных атомах.
Ковалентная связь возникает между атомами, имеющими одинаковую или близкую по значению электроотрицательность. Для образования ковалентной связи каждый из атомов предоставляет по одному электрону, при этом образуется общая пара электронов, которая в равной степени принадлежит обоим атомам. На письме ковалентная связь изображается черточкой между атомами.
Классическим примером ковалентной связи является молекула метана:
8
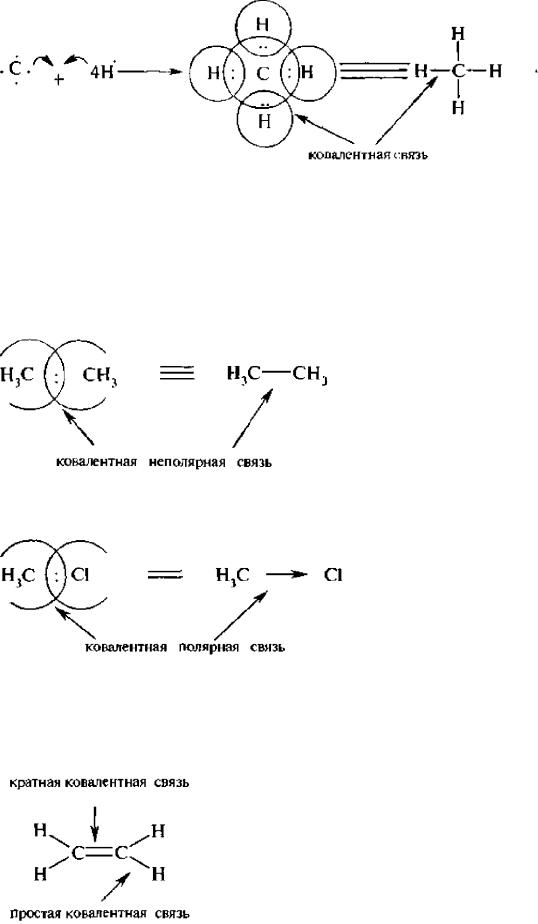
Атом углерода содержит на внешнем электронном уровне четыре валентных электрона и, чтобы доукомплектовать этот слой до октетной конфигурации, он образует четыре общие электронные пары с четырьмя атомами водорода.
В зависимости от электроотрицательности атомов между которыми образовалась ковалентая связь, она может быть полярной или неполярной.
Если электроотрицательность атомов одинакова, то общая электронная пара находится на одинаковом расстоянии от ядра каждого из атомов, Такая связь называется ковалентной неполярной:
При возникновении ковалентной связи между атомами с различной электроотрицательностью общая электронная пара смещается к более электроотрицательному атому. В этом случае образуется ковалентная полярная связь.
Стрелка в формуле указывает на полярность ковалентной связи. С помощью греческой буквы δ {«дельта») обозначают частичные заряды на атомах: δ+ – пониженную, δ- – повышенную электронную плотность.
По числу электронных пар, образующих ковалентную связь, различают связи простые – с одной парой электронов и кратные – с двумя или тремя парами.
Основные характеристики ковалентной связи:
длина связи (расстояние между центрами атомов в молекуле); энергия связи (энергия, которую необходимо затратить на разрыв связи);
9

полярность связи (неравномерное распределение электронной плотности между атомами, обусловленное различной электроотрицательностью);
поляризуемость (легкость, с которой смещается электронная плотность связи к одному из атомов под влиянием внешних факторов);
направленность (ковалентная связь, направленная до линии, соединяющей центры атомов). Атомы некоторых элементов (кислорода, азота, серы, галогенов и др.) расходуют не все внешние электроны для формирования октетной оболочки. Такие электроны называют
неподеленные, необобществленные или n-электроны.
Донорно-акцепторная связь или координационная – разновидность ковалентной связи,
которая отличается способом образования.
Донор – атом, который должен иметь пару неполеленных электронов, а акцептором может быть любой атом (в том числе и протон), у которого не хватает до образования октета двух электронов.
Например, образование иона аммония протекает по донорно-акцепторному механизму. Ковалентная связь образуется за счет того, что атом азота (донор электронов) отдает неподеленную пару электронов на образование ковалентной связи протону (акцептору электронов):
Врезультате образования связи атом кислорода (акцептор) приобретает отрицательный заряд,
аатом азота (донор) – положительный. Такой вид связи обозначают следующим образом:
Вновь образовавшаяся связь Н–N ничем не отличается от остальных связей Н–N, которые имелись у аммиака. Такая связь называется еще координационной.
Семи полярная связь – частный случай донорно-акдепторной связи. Она образуется между атомами, один из которых имеет неподеленную пару электронов, а другой содержит на внешнем энергетическом уровне шесть электронов (секстет), то есть имеет вакантную атомную орбиталь.
Рассмотрим образование семиполярной связи в молекуле оксида триметиламина:
Соединения с семиполярной связью не проводят электрический ток, несмотря на наличие наряду с ковалентной связью и ионного взаимодействия.
ВОДОРОДНАЯ СВЯЗЬ
10
