- •Основные виды коррозионных разрушений
- •Зависимость скорости коррозии от структуры стали 1—мартенсит; 2 — троостит; 3 — сорбит;
- •Зависимость скорости коррозии твёрдых растворов медь – золото в концентрированной азотной кислоте от
- •Зависимость скорости коррозии от рН среды
- •Зависимость скорости коррозии железа от концентрации кислорода
- •Рисунок 6 – Зависимость скорости коррозии в воде от температуры (а) и зависимость
- •Схема газовой коррозии
- •Основные виды разрушения оксидной плёнки
- •Строение окалины железа
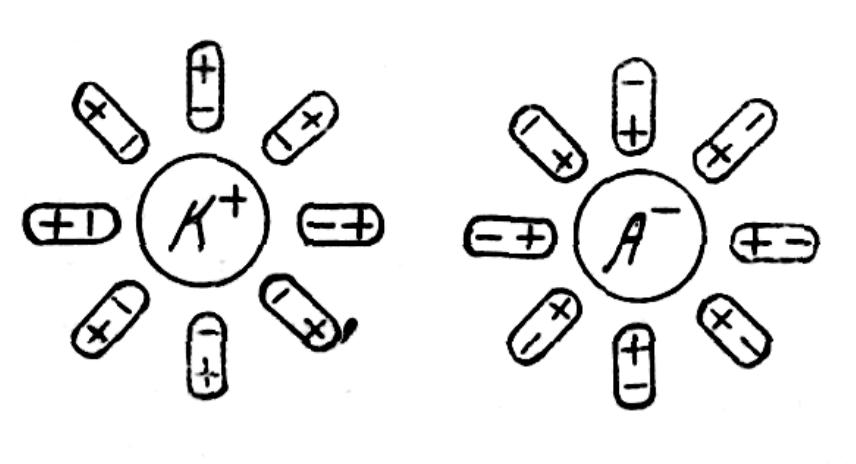
- •Схема образования гидратированных ионов
- •Схема двойного электрического слоя
- •Стандартные электродные потенциалы
- •Схема электрохимической коррозии стали в растворе кислоты
- •Схема изменения потенциалов катода и анода после замыкания цепи φа0; φк0 – начальные
- •Потенциал водородного и кислородного электродов в зависимости от рН среды
- •Коррозионная диаграмма Эванса φа; φк – начальное положение потенциалов анода и катода (бесконечное
- •А – область сухой атмосферной коррозии; Б – область влажной атмосферной коррозии; В
- •1 – чистый воздух; 2 – воздух содержит 0,01% SO2
- •Схема развития язвы (питтинга)
- •Схема щелевой коррозии
- •Образование ножевой коррозии
- •Заклёпочные соединения
- •Зависимость скорости коррозии железа от концентрации кислоты
- •Анодная потенциостатическая кривая
- •Анодная потенциостатическая кривая для хрома, железа и никеля
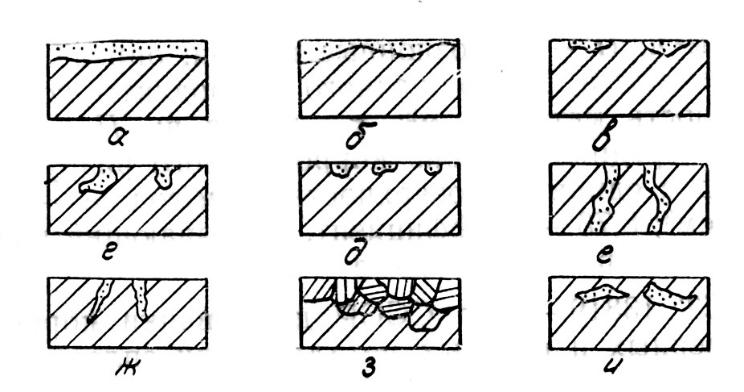
Основные виды коррозионных разрушений
а – сплошная равномерная коррозия; б – сплошная неравномерная коррозия; в – коррозия пятнами; коррозия язвами; г – коррозия точками; е – сквозная коррозия; ж – ножевая коррозия; з – межкристаллитная коррозия; и – подслойная коррозия
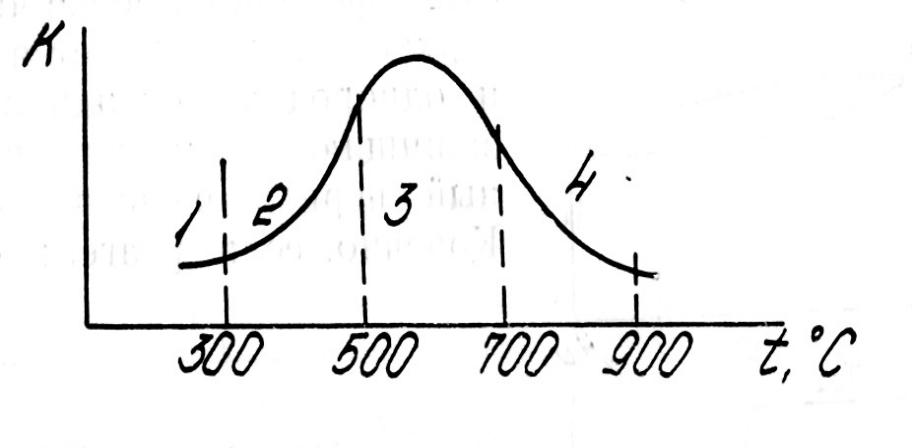
Зависимость скорости коррозии от структуры стали 1—мартенсит; 2 — троостит; 3 — сорбит; 4 — перлит
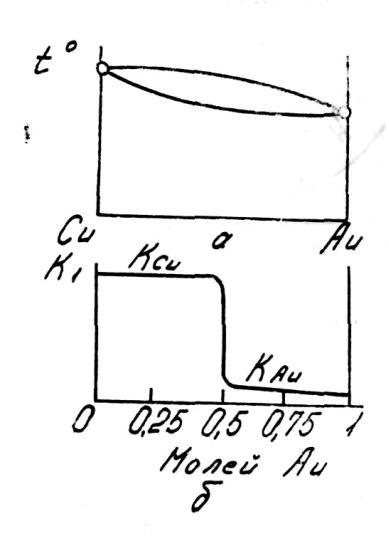
Зависимость скорости коррозии твёрдых растворов медь – золото в концентрированной азотной кислоте от состава сплава
б – изменение коррозионной стойкости в зависимости от состава сплава
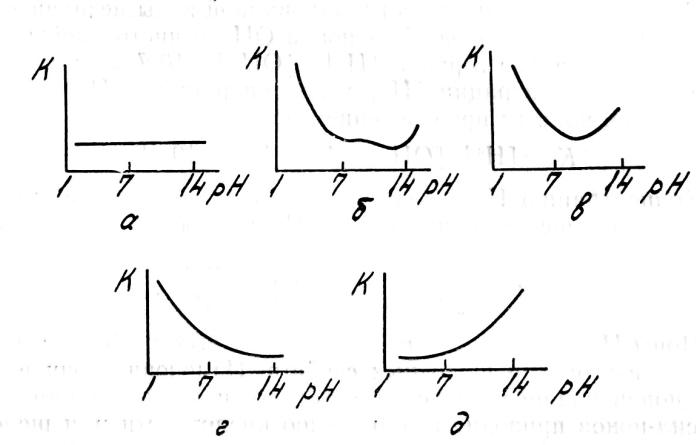
Зависимость скорости коррозии от рН среды
а– благородные металлы Ag, Au, Pt; б – малостойкие в кислых средах и стойкие
вщелочных Fe, Cu, Mn, Mg; в – устойчивые в нейтральных средах и сильно корродирующие в кислых и щелочных Al, Pb, Sn, Zn; г – малостойкие в кислых средах и стойкие в щелочных Ni, Co, Cr; д – стойкие в кислых средах и неустойчивые в щелочных W, Mo, Ta.
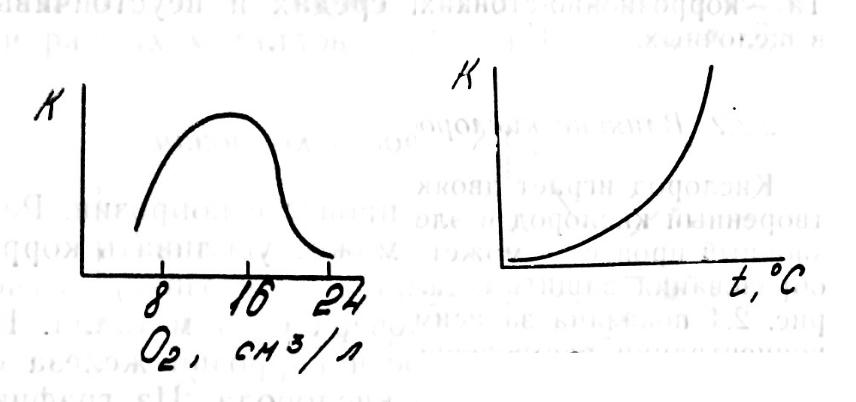
Зависимость скорости коррозии железа от концентрации кислорода
(а) и температуры (б)
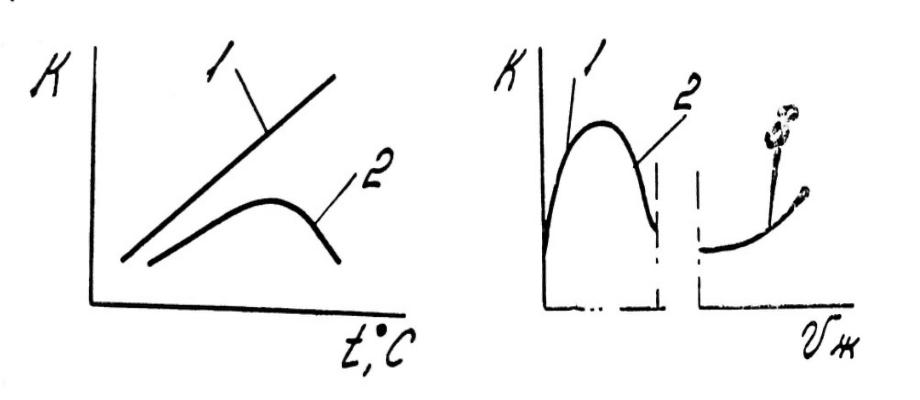
Рисунок 6 – Зависимость скорости коррозии в воде от температуры (а) и зависимость скорости коррозии от скорости движения жидкости (б)
а: 1 – закрытая система; 2 – открытая система
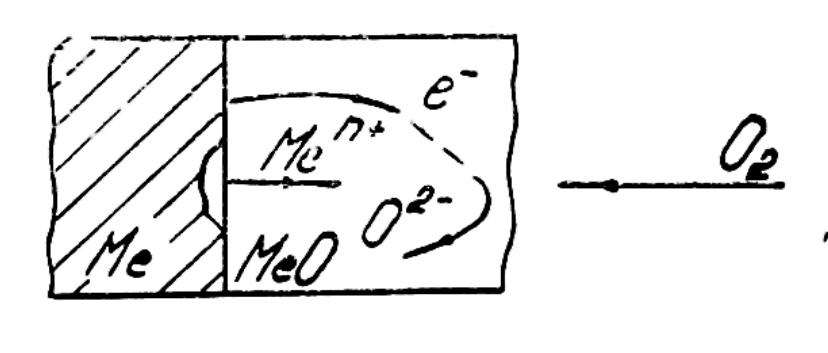
Схема газовой коррозии
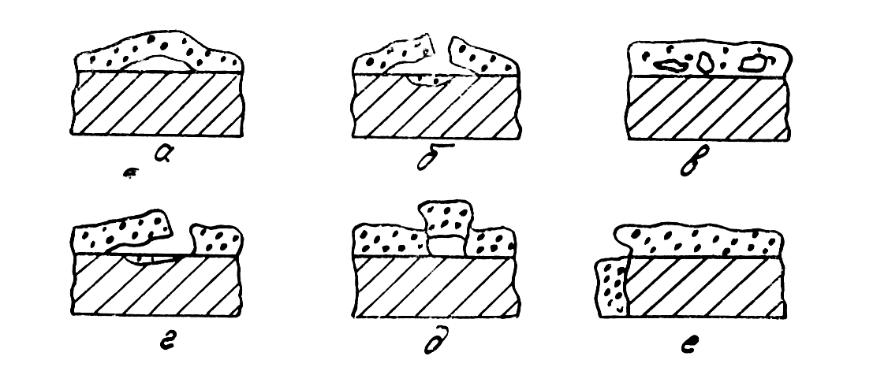
Основные виды разрушения оксидной плёнки
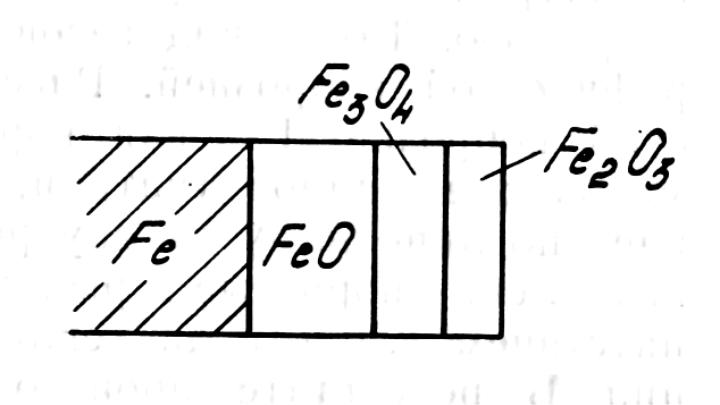
Строение окалины железа