
лабораторная работа / ADIABATA
.DOC
САРАТОВСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ
ЛАБОРАТОРНАЯ РАБОТА №7
Измерение показателя адиабаты
Выполнил: студент 1-го курса группы ПВС-12 Козлов С.С.
Проверил:
Саратов, 1999
Цель работы
В ходе эксперимента вычислить показатель адиабаты и погрешность при его нахождении.
Методика эксперимента
Экспериментальная установка состоит из большого стеклянного баллона 1 объёмом V (V = 10л.) с воздухом, соединённого с манометром 2 и насосом 3. С помощью клапана 5 в насадке 4 баллона может сообщаться с атмосферой и с помощью клапана 6 – с насосом. Разность уровней жидкости в коленах манометра показывает превышение давления P в баллоне над атмосферным.
5 6 4 1 2 3






Метод Клемана-Дезорма определения показателя адиабаты основан на исследовании некоторой массы воздуха, мысленно выделенной в баллоне, последовательно проходящей через три состояния, причём из 1-го во 2-ое состояние воздух переходит путём адиабатического расширения и из 2-го в 3-е путём изохорического нагревания.
С помощью насоса в баллон накачивают некоторую массу воздуха. В следствии произведённой работы (при накачивании) воздух в баллоне нагреется. До начала опыта необходимо подождать несколько минут, чтобы в результате теплообмена температура в баллоне сравнялась с температурой окружающей среды. При этом давление в баллоне несколько снизится, т.к. давление пропорционально температуре (P=nkT).
Рассмотрение процесса начнём с того момента, когда температура и давление в баллоне установились. Выделенная часть воздуха в баллоне в начале процесса будет характеризоваться P1 (выше атмосферного), V1, T1 (температура окружающей среды), что соответствует точке I на диаграмме состояний.
П роизведём
адиабатическое расширение воздуха в
баллоне, соединив объём баллона с
атмосферой. Часть воздуха выйдет из
баллона, а выделенная масса воздуха
расширится. Это расширение можно считать
почти адиабатическим, если оно происходит
быстро и теплообмен с окружающей средой
произойти не успевает. Такой процесс
приближённо можно считать равновесным
и изобразить на диаграмме.
роизведём
адиабатическое расширение воздуха в
баллоне, соединив объём баллона с
атмосферой. Часть воздуха выйдет из
баллона, а выделенная масса воздуха
расширится. Это расширение можно считать
почти адиабатическим, если оно происходит
быстро и теплообмен с окружающей средой
произойти не успевает. Такой процесс
приближённо можно считать равновесным
и изобразить на диаграмме.
На диаграмме процесс расширения изображён отрезком адиабаты I-II. Давление в баллоне сравнивается с атмосферным, а температура понижается. Параметры выделенной части воздуха принимают значения: P2 (атмосферное), V2, T2 (ниже температуры окружающей среды). Параметры воздуха в начале и в конце опыта связаны уравнением адиабаты:
![]() (1).
(1).
После адиабатического нагревания в течение 2-3-ёх минут произойдёт теплообмен между окружающей средой и воздухом в баллоне. Температура в баллоне поднимается до температуры окружающей среды, а давление повысится. Процесс изобразится отрезком изохоры II-III. Параметры газа примут значения P3, V2, T1 (окружающей среды).
Сравнивая конечное состояние выделенной части воздуха III с исходным I, можно заметить, что они находятся при одной и той же температуре T1, такие состояния связаны уравнением изотермы:
![]() (2).
(2).
Для определения показателя адиабаты возведём уравнение (2) в степень и разделим почленно на уравнение (1):
 или
или
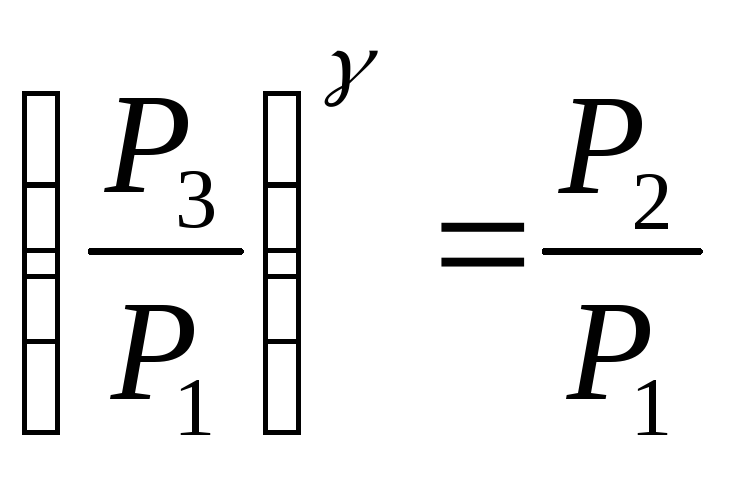 (3).
(3).
Логарифмируя уравнение (3), получим:
![]() (4).
(4).
Эту формулу упростим, исходя из условий эксперимента. Выразим давление воздуха в баллоне через разность уровней жидкости в коленах манометра h. Обозначим атмосферное давление H, добавочное давление в состоянии I буквой h1 и добавочное давление в состоянии II буквой h2. Тогда P1=H+h1, P2=H, P3=H+h2, где h1 и h2 << H.
Подставим эти значения в уравнение (4):
![]() (5).
(5).
Подставим эти формулы в (5), для показателя адиабаты имеем:
![]() (6).
(6).
Порядок выполнения работы
-
Накачал с помощью насоса воздух в баллон до давления 0,8 – 0,9 от предельного по шкале манометра. Выждал около 5 минут, чтобы падение давления поэтапно прекратилось. Клапан 5 должен быть закрыт. Отсчитал разность уровней h1.
Для измерения величины h2 использовал 2 способа:
|
2)
|
1-ый способ. Произвёл адиабатическое расширение. Для этого на 2-3 секунды нажал клапан 5. Выждал 1-2 минуты, затем снял первую разность уровней h2. Измерение 2) повторил 10 раз и для каждого измерения вычислил по формуле (6 – методика эксперимента).
|
-
2-ой способ. Нажал клапан 5 и держал открытым время ti (1-5 секунд). Отпустил клапан 5 и выждал 1-2 минуты, определил полученную разность h2i. Измерения ti и h2i провёл 5 раз при разных значениях ti и неизменном значении h1.
|
Уровни |
№ эксперимента |
|||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
|
h1 |
110 |
100 |
105 |
115 |
104 |
94 |
100 |
95 |
98 |
115 |
|
h2 |
20 |
21 |
19 |
22 |
19 |
17 |
20 |
17 |
19 |
19 |
|
|
1,22 |
1,27 |
1,22 |
1,24 |
1,22 |
1,22 |
1,25 |
1,22 |
1,24 |
1,20 |
![]()
|
|
№ эксперимента |
|||||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
|
h1x |
6,40 |
-3,60 |
1,40 |
11,40 |
0,40 |
-9,60 |
-3,60 |
-8,60 |
-5,60 |
11,40 |
|
h2x |
0,7 |
1,7 |
-0,3 |
2,7 |
-0,3 |
-2,3 |
0,7 |
-2,3 |
-0,3 |
-0,3 |
V2 = V0 = 10л. = 0,01м^3 – объём баллона
T1 = T0 = 300K – температура воздуха
P2 = P0 = 10^5Па – давление в лаборатории
Определение количество молей газа в баллоне:
Определение внутренней энергии газа:
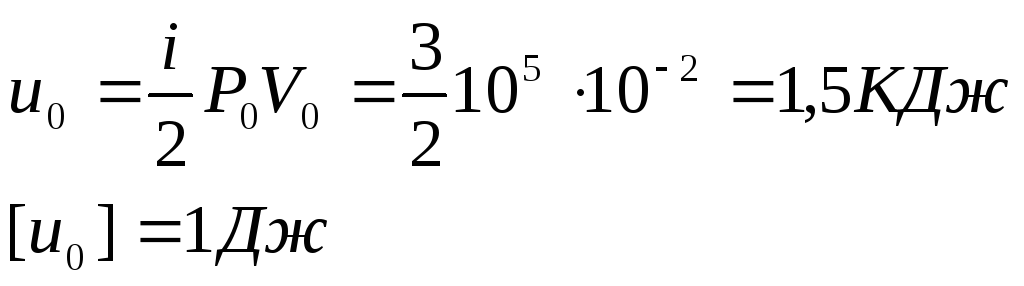
где i – количество измерений, в которых могут перемещаться молекулы газа.
По данным исходному состоянию и значению вычислил:
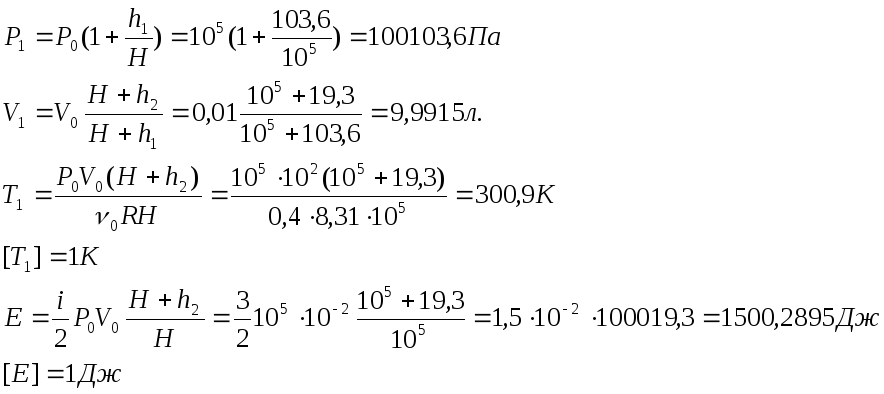
Расчёт погрешностей
П огрешность
вычисления показателя адиабаты
насчитывается по формуле расчёта
погрешности косвенных измерений:
огрешность
вычисления показателя адиабаты
насчитывается по формуле расчёта
погрешности косвенных измерений:
Где h1 и h2 определяются по методике расчёта погрешностей прямых измерений:

где N-число измерений, Cn-коэффициент Стьюдента для N (N = 10) измерений (C10 = 2,3).

Вывод
Средний
показатель адиабаты
![]() ,
что близко к реальному значению.
Допущенная погрешность
0,43.
,
что близко к реальному значению.
Допущенная погрешность
0,43.


