
травматология 2 / Yu_G_Shaposhnikov_red_Travmatologia_i_ortoped
.pdfнередко и видимой на глаз воспалительной опухолью — поднадкостничной или параоссальной флегмоной. Пальпация и перкуссия этого отдела резко болезненны. Движения в близлежащих суставах значительно ограничены из-за развивающейся контрактуры.
С е п т и к о - т о к с и ч е с к а я ф о р м а . Является или продолже нием первых двух форм, или же может быть дебютом заболевания. В последнем варианте травматолог почти никогда не участвует в диагностическом процессе, ибо именно при этой форме локальные проявления нивелируются за счет выраженных общих сдвигов. За болевание начинается остро, внезапно. Клиника соответствует сеп тическому шоку и развивается в первые часы болезни. Отмечается высокая температура тела, достигающая 39—41°С, появляются му чительные головные боли, сменяющиеся бредовым состоянием, не редко рвота. Если к этому времени больной успел обратить внимание на боли в скелете, то диагностика может пойти по правильному руслу. В противном случае состояние больного трактуется тифозным, и он направляется в инфекционную больницу. Вместе с тем в самой картине септического шока могут быть различные нюансы, связан ные или с этапами его развития, или этиологией (грамотрицательные или грамположительные микроорганизмы, вызвавшие воспаление). Разнообразная клиническая картина укладывается в понимание «по лиорганной патологии». Резко снижается сердечная деятельность, падает артериальное давление, учащается число сердечных сокра щений со слабостью наполнения и напряжения пульса. Границы сердца расширяются, тоны приглушены, а на ЭКГ выявляются дистрофические изменения миокарда. Особое значение придают ис следованию легких как органа-мишени, в котором раньше всего развиваются вторичные септические изменения: ослабление дыха тельных шумов, хрипы, притупление перкуторного звука, а на рентгенограммах выявляется различная гамма изменений — от интерстициального и альвеолярного отека до локальных воспалитель ных изменений (инфильтраты, абсцессы, плевриты и др.). Резко страдает выделительная функция почек — отмечается олигурия, вплоть до анурии. Пальпируются увеличенная печень и селезенка. Нередки петехиальные высыпания на коже.
Диагностика и дифференциальный диагноз. Диагностика острого гематогенного остеомиелита основывается на анализе клинических данных и обязательном применении лабораторно-инструментальных методов.
Следует выделить главное в клинической картине — локализо ванную болезненность, подкрепленную общеклиническими сдвига ми. Мы категорически возражаем против общепринятого метода клинической диагностики у больных с подозрением на острый ге матогенный остеомиелит — динамического наблюдения. Нам неод нократно приходилось сталкиваться с внезапным септическим шоком у больных, находящихся под динамическим наблюдением. Поэтому в диагностической ситуации, когда подразумевается возможность остеомиелита, он должен быть немедленно подтвержден или отвер гнут дополнительными методами исследования. Их можно подраз-
559
делить на обычные (лабораторные) и специальные (инструменталь ные).
Лабораторные методы исследования крови подтверждают наличие воспалительного процесса увеличением числа лейкоцитов, сдвигом лейкоцитарной формулы влево, увеличением СОЭ. При биохими ческом изучении крови отмечается снижение белка разной степени, в зависимости от формы процесса с преобладанием снижения уровня мелкодисперсных фракций. Неоднозначны изменения углеводного обмена: значительное снижение глюкозы в крови при генерализо ванных формах и увеличение при локальных. Значительно повы шается активность свертывающей системы.
Инструментальные методы исследования подразделяют на неинвазивные и инвазивные. На первый взгляд, такие методы неинвазивной диагностики, как реовазография, артериальная осциллогра фия, ультразвуковая эхолокация, цветная контактная термометрия, тепловидение и др., чрезвычайно заманчивы. Однако им присущи и серьезные недостатки, главным из которых является только кос венное доказательство наличия болезни, указывающее лишь на имеющееся воспаление, но не раскрывающее ни его природы, ни степени выраженности. Поэтому, нисколько не умаляя их значения, необходимо из методов неинвазивной диагностики предпочесть рент генологический, хотя и он имеет определенные недостатки, ибо известно, что первые убедительные симптомы появляются не ранее 5—6-го дня заболевания. Вместе с тем высказанное С. А. Рейнбергом (1964) мнение о важности мягкотканной диагностики острого гема тогенного остеомиелита используется еще явно недостаточно. Суть ее сводится к детальному прочтению состояния параоссальных мяг ких тканей, отражающих картину начального процесса: отек и увеличение тени мягких тканей.
Изучение рентгенограмм для выявления начальных признаков заболевания, связанных с появлением «воспалительного остеопороза», следовало бы начинать с их денситометрии [Ормантаев К. С, Султанбаев Т. Ж., 1979]. Велика информативность в этот самый важный для диагностики период ЯМР. С момента появления периоссальных наслоений диагноз становится утвердительным, но в той же мере и запоздалым из-за деструктивных изменений (рис. 11.2).
Разновидностью лучевой является радионуклидная диагности ка — сканирование, — связанная с накоплением и выявлением в очаге поражения того или иного радиофармацевтического пре парата.
Инвазивные методы диагностики, по нашему мнению, имеют несомненные преимущества. Они прежде всего общедоступны, более информативны и убедительны. Основой инвазивного метода является пункция мягких тканей кости в зоне наибольшей болезненности. Пункцию проводят под общей анестезией обычными иглами Дюфо, Кассирского и др. Поступление гноя по игле тотчас решает диаг ностическую задачу. Если же по игле поступает кровь, то, присо единив аппарат Вальдмана, можно измерить ВКД, которое в норме
560

Рис. 11.2. Рентгенограмма. Острый гематогенный остео миелит нижней трети правой большеберцовой кости. Де струкция костной ткани с периостальными наслоениями.
равно 120 мм вод. ст., а в зависимости от остроты воспаления повышается до 200—300 и 400 мм вод. ст. Введением в иглу датчика от электротермометра регистрируется внутрикостная температура, которая с нормальных цифр 37,2°С повышается до 38—39°С и более. Эти экспресс-тесты подтверждают диагноз ос теомиелита. Дополнительно взятая из иглы кровь на посев и цитология мазка позволяют получить сведения о возбудителе и характере воспаления, что имеет значение для выбора методов консервативного лечения. Через иглу, находящуюся в очаге воспаления, можно вы полнить остеомедуллографию и по задержке контрастного вещества судить о границах по ражения.
Из перечисленных методов основное зна чение мы придаем измерению температуры, ВКД и бактериологического исследования пунктата. Этот комплекс исследований мы назы ваем «скрининг-тестом», который позволяет резко поднять уровень своевременной диагно стики острого гематогенного остеомиелита.
Круг заболеваний для целей дифференци альной диагностики необходимо подразделить на протекающие преимущественно с общими изменениями и преимущественно с локальными
проявлениями. К числу первых необходимо отнести упоминавшуюся выше тифо-паратифозную инфекцию, которую ошибочно диагности руют при наличии острого гематогенного остеомиелита. Некоторые старые авторы называли остеомиелит «костным тифом». К ошибке при водит игнорирование тщательного исследования всех костей скелета, наиболее часто являющееся причиной септического статуса.
Опухоли костей (остеогенная саркома, опухоль Юинга) нередко протекают с повышением температуры тела, общей слабостью. Од нако главным в их диагностике является сильнейший болевой сим птом, не прекращающийся в течение суток. Сомнения в диагнозе решаются рентгенологическим исследованием, открывающим типич ные проявления. При неясности диагноза проводят биопсию кости.
Туберкулез костей весьма редко является причиной диагности ческих ошибок. Для него характерны медленное течение, довольно типичный анамнез, отсутствие выраженного лихорадочного статуса, очаговый (преимущественно эпифизарный) характер процесса. На рентгенограмме нет периостальных наслоений.
19—1241 |
561 |
|
Ревматизм является объектом для дифференциальной диагности ки в ситуациях, при которых он сопровождается перифокальными изменениями в суставах. Однако более медленное начало заболе вания, интактность метафизарного отдела кости при пальпации, отсутствие значительных воспалительных изменений в крови по зволяют установить правильный диагноз.
Впоследние годы все заметнее становится значимость острого лейкоза в дифференциальной диагностике острого гематогенного остеомиелита. Лейкозные инфильтраты, распирая кость, повышают ВКД. Оно иногда столь высоко, что инфильтрат расплавляется и через каналы остеонов выходит за пределы кости, создавая полное впечатление субпериостальной флегмоны. Деструктивный характер поражения кости иногда трудно отличить от остеомиелита. Реша ющее значение мы придаем пункции кости, при которой выявляются нормальная температура и высокое ВКД. При этом посев остается стерильным. При подобном сочетании рекомендуем исследование костного пунктата грудины.
Вситуациях с преимущественно локальными проявлениями не обходимо дифференцировать со многими патологическими процес сами. Однако прежде всего необходимо думать о разных процессах при поражении сегмента конечности, состоящего из двух костей или же между сегментами скелета. В нашей практике отмечались напрасные остеоперфорации проксимального отдела бедра при ис тинном поражении подвздошной кости. Встречается это тогда, когда зона резкой болезненности чрезвычайно расширена.
Травма кости или сустава, сопровождающаяся общей слабостью, повышенной температурой тела, всегда требует проведения диффе ренциальной диагностики и поиска очага поражения.
Нередко значительные трудности возникают при дифференци альной диагностике между флегмоной и остеомиелитом. При ма лейшем подозрении на последний необходима пункция кости, ко торая должна проводиться вне флегмоны (с противоположной сто роны). Подобный методический подход должен быть и при прове дении дифференциальной диагностики с рожистым воспалением.
Нередко трудности дифференциальной диагностики связаны с некоторыми суставными заболеваниями — транзиторным и аллер гическим синовитами. Локальность их течения, отсутствие общих сдвигов, а также диагностическая пункция сустава обычно разре шают сомнения.
Лечение. Лечение комплексное, основы которого заложил еще Т. П. Краснобаев (1925). Оно состоит из следующих патогенетиче ских звеньев: воздействия на макроорганизм, микроорганизм и ме стный очаг. Подчеркнем крайнюю важность экстренности в прове дении этого комплекса. Сроки оказания экстренной помощи должны исчисляться не в часах, а в минутах, ибо при условно локальной форме подобная экстренность предупреждает возможность появления ярких септических осложнений. Наряду с этим от быстрого прове дения лечебных мероприятий зависит и морфофункциональный ис ход заболевания. По нашим данным, диагностика острого гемато-
562
генного остеомиелита в первые 12 ч заболевания и экстренная помощь способствуют выздоровлению больных в 93,4% случаев.
Воздействие на макроорганизм преследует цель снятия инток сикации, нивелировку острых нарушений жизненно важных ор ганов, поднять защитные возможности больного и подготовить его к предстоящей операции. Одним из первых пособий должно быть снижение температуры тела, опасной именно у детей переходом в состояние токсемического шока. Борьба с температурой заклю чается в применении физических методов охлаждения и в про ведении медикаментозного лечения, направленного на расширение периферических сосудов (папаверин, но-шпа) и непосредственно ведущих к ее снижению (4% раствор амидопирина в дозе 0,1 мл/кг, 50% раствор анальгина в дозе 0,1 мл на год жизни ребенка). Коррекцию нарушений гомеостаза проводят путем внут ривенных инфузий с целью ликвидации гиповолемии и нормали зации водно-электролитного баланса и КОС. Стартовыми раство рами для проведения инфузионной терапии являются глюкоза и низкоили среднемолекулярные полимеры, оказывающие детоксикационное действие (гемодез, реополиглюкин) и белковые пре параты (альбумин, нативная плазма, свежезаготовленная кровь или прямые ее переливания). Необходимая часть расчетного объема жидкости восполняется растворами электролитов. Нормализация метаболического или смешанного ацидоза, развивающегося в ос тром периоде остеомиелита, осуществляется с помощью введения 4% раствора гидрокарбоната натрия или трисамина. Тяжелая ин токсикация, проявляющаяся рвотой и поносом в далеко зашедшем процессе, сопровождается гипокалиемией и требует проведения коррекции ее путем введения хлорида калия и др.
В основе дезинтоксикационной терапии наряду с общепринятыми получили распространение и специальные методы, и среди них выдвигается на первый план гемосорбция — экстракорпоральное очищение крови, где в качестве сорбентов используют специальные активированные угли. Обменную гемотрансфузию проводят у наи более тяжелых больных. Замещается примерно 1,5—2 ОЦК инди видуально подобранной свежестабилизированной крови. В течение ряда лет для целей детоксикации используют форсированный диурез. Суть метода состоит в увеличении предварительно водной нагрузки 5% раствором глюкозы, раствором Рингера—Локка (с гемодилюциеи до 30%) с последующим введением лазикса и маннитола. Метод положительно зарекомендовал себя, но требует постоянного конт роля. В последние годы с целью детоксикации проводят плазмаферез. К методам детоксикации необходимо отнести и назначение инги биторов протеолиза, ибо гидролазному насыщению крови в насто ящее время придается главное значение в патогенезе интоксикации. С этой целью в возрастных дозировках назначают трасилол, контрикал.
Улучшение состояния микроциркуляторного русла направлено на ликвидацию ДВС-синдрома. С этой целью вводят гепарин из расчета 100—150 ЕД/кг внутривенно через 6 ч. Назначают его не
19* |
563 |
ранее чем через 12 ч после операции. Для уменьшения проницае мости стенки капилляра назначают аскорбиновую кислоту, препа раты кальция, рутин.
Важным разделом общей терапии является забота об укреплении общей резистентности индивидуума, которое лучше всего проводить на фоне десенсибилизирующей терапии. В ряду средств общего воздействия необходимо отметить переливание свежезаготовленной крови, эритроцитной массы, плазмы, альбумина. Повышение иммунорезистентности проводят назначением иммуностимуляторов — левамизола, тималина, нуклеината натрия. Для стимуляции мета болических процессов используют метилурацил, пентоксил, оротат калия. Специфическая иммунотерапия включает введение гиперим мунной антистафилококковой плазмы, гипериммунного антистафи лококкового гамма-глобулина и стафилококковой вакцины.
И, наконец, нельзя понимать общей терапии острого гематоген ного остеомиелита без заботы об обеспечении и покрытии энерге тических затрат. При парентеральном питании потребность больного в калориях обеспечивают за счет введения смесей в следующих соотношениях основных ингредиентов: углеводы — 60%, жиры — 30%, белки — 10%. По мере восстановления аппетита больного переводят на естественное питание.
Воздействие на макроорганизм проводят целенаправленной ан тибактериальной терапией. Учитывая, что даже до развертывания всей симптоматики сепсиса острый гематогенный остеомиелит не обходимо считать потенциально септическим состоянием, антибак териальную терапию необходимо проводить в оптимальном режиме. Практически всем больным необходимо пунктировать подключич ную вену, через которую проводится не только инфузионная, но и антибактериальная терапия. К общей антибактериальной внутри венной терапии обязательно добавляется местная внутрикостная (в очаг поражения). При торпидном течении процесса местное лечение дополняют пункционным внутриартериальным (в бедрен ную артерию). Наряду с этим всем больным для поддержания достаточной концентрации антибиотики регулярно вводят внутри мышечно в обычных дозировках.
Принимая во внимание, что в первые часы поступления иден тифицировать флору не представляется возможным, лечение начи нают с внутривенного введения натриевой соли пенициллина в массивных суточных дозировках. Внутрикостно капельно тотчас на значают антибиотики широкого спектра действия. Через 2 сут после получения результатов бактериального исследования антибиотики внутрикостно назначают в зависимости от чувствительности (гентамицин, клафоран, цефалоспорины и др.).
В тех ситуациях, когда не удается оборвать течение процесса при достаточном дренировании очага, дополнительно в бедренную артерию вводят пункционно 5 000 000—10 000 000 ЕД пенициллина в 20 мл 0,25% раствора новокаина. Все внутрикостно вводимые растворы, учитывая гипертермию кости, охлаждают до 20°С.
Местное лечение неоднократно пересматривалось. В конце про-
564

шлого столетия оно бы ло активно хирургиче ским и заключалось во вскрытии флегмоны с обязательной широкой трепанацией кости, про водившейся в остром пе риоде. Нередко подо бные операции заканчи вались патологическими переломами, ампутаци ями конечностей и летальнымии исходами. Впервые сберегатель ный принцип в лечении острого гематогенного остеомиелита внедрил Т. П. Краснобаев. По его мнению, детская кость, имеющая широ кие каналы остеонов, способна самостоятель но дренировать костно мозговую полость, без ее насильственной тре панации. Операция бы ла им ограничена лишь периостотомией. Опыт показал несомненную правоту Т. П. Краснобаева: повсеместным внед рением его принципов удалось снизить леталь ность и улучшить фун кциональные результа ты лечения. Однако с
Рис. 11.3. Рентгенограмма. Внутрикостное введение антибиотиков в дистальный метафиз большеберцовой кости.
появлением антибактериальных препаратов и новых взглядов на патогенез в настоящее время местное лечение вновь претерпело изменения. Основным в лечении является снижение высокого ВКД, предупреждающее генерализацию процесса, и поэтому периостотомию обязательно дополняют так называемыми микротрепанациями, достаточными для дренирования, но не нарушающими структуру кости (рис. 11.3). Ранняя декомпрессия в очаге остеомиелита ока зывается достаточно эффективной, и поэтому мы считаем излишним множественные остеоперфорации, промывание всей костномозговой полости с насильственным разрушением активных очагов кроветво рения, столь функционально необходимых именно в остром периоде заболевания.
Методика локальной терапии состоит в следующем. Проводят
565
разрез кожи и подкожной жировой клетчатки над зоной наибольшей болезненности. Разъединяют по ходу волокна мышцы. При наличии поднадкостничной флегмоны ее вскрывают, а при отсутствии рас секают надкостницу. Фрезами диаметром до 0,3—0,8 см в зависи мости от величины кости наносят два—три перфорационных отвер стия. В центре или рядом оставляют иглу для внутрикостного вве дения антибиотиков. Накладывают заднюю гипсовую шину. В тех ситуациях, когда диагностируется тотальное поражение кости, про водят подобное лечение в двух метафизарных зонах.
Впослеоперационном периоде проводят ежедневные перевязки
сосмотром, а при необходимости — и ревизию раны для обеспечения хорошего дренирования. Осматривают все кости скелета для выяв ления возможных очагов отсева. При подозрении на метастазы проводят пункцию кости с измерением температуры и давления.
При гладком послеоперационном периоде в течение 7—10 дней нормализуется температура тела, улучшается общее состояние. Это является показанием для удаления иглы. У тех же больных, у которых температура тела остается повышенной, общее состояние страдает, можно в течение 3 дней вводить в бедренную артерию антибиотики. Эти меры оказываются очень эффективными. В крайне редких наблюдениях при неэффективности внутриартериального ле чения проводят ревизию зоны деструкции и соединение ранее на ложенных трепанаций в одно трепанационное отверстие.
По мере стихания острых явлений воспаления больным разре шают в течение дня дозированные движения в суставе для предуп реждения тугоподвижности. Проводят физиотерапевтическое лече ние: электрофорез антибиотиков, УФО, УВЧ-терапию.
Через 3—4 нед проводят контрольное рентгенологическое иссле дование и при отсутствии прогрессирования процесса разрешают вставать в гипсовой шине на костыли с легкой нагрузкой на ногу. Стационарное лечение продолжается в течение 1—1,5 мес.
Через 2—3 мес после выписки у детей при гладком послеопе рационном течении функция конечности полностью восстанавлива ется. В дальнейшем проводят общеукрепляющее лечение: ЛФК, массаж, водные процедуры. Рекомендуется избегать нагрузки на кость. При возможности проводят санаторное лечение, особенно при наличии остаточных явлений в суставах.
.
11.1.1. Деформации костей и суставов после гематогенного остеомиелита у детей
Деформации опорно-двигательного аппарата, возникшие как следствие перенесенного гематогенного остеомиелита, составляют значительную и трудно поддающуюся ле чению группу заболеваний ортопедического профиля. Совокупность характерных особенностей возникновения деформаций и патологических изменений в пораженных тканях позволяет выделить их в отдельную нозологическую форму ортопедической патологии.
Количество наблюдаемых деформаций связано с частотой поражения гематогенным остеомиелитом и трудностями диагностики и лечения этого заболевания, несвоевремен ностью и неадекватностью ортопедического лечения.
566
Гематогенный остеомиелит у детей является проблемой не только медицинской, но и социальной. Наиболее часто гематогенный остеомиелит поражает новорожденных и детей 1-го года жизни. Причины этого кроются в особой уязвимости организма ребенка в названные возрастные периоды из-за повышенной восприимчивости к инфекционным заболеваниям. Для новорожденных характерна высокая частота инфекций: 1 — 2 % груд ных детей инфицируются еще в эмбриональном периоде, а 10% новорожденных — в возрасте до 2 мес. Существуют многочисленные факторы риска и пути инфицирования развивающегося плода. Так, трансплацентарный путь инфицирования возможен и носит выраженный диссеминированный характер. Новорожденные инфицируются во время прохождения родовых путей, от матерей, больничного персонала и посетителей, а также инфицируются с небиологических объектов внешней среды. У здоровых новорожденных, родившихся в срок, колонизация может быть выявлена на 2—3-й день жизни. Полость носа и область пупка колонизируются Staphylococcus aureus, Staphylococcus epidermidis, Streptococcus haemoliticus, а желудочно-кишечный тракт — Escherichia coli, лактобактериями и анаэробами, у недоношенных и детей, родившихся с малой массой тела, риск инфицирования увеличивается.
Отмечено превалирование тех или иных возбудителей инфекционных заболеваний в разные возрастные периоды. Так, до 60-х годов в стационарах США этиологическим Диктором большинства эпидемий в учреждениях для новорожденных и детей младшего возраста, в том числе и эпидемий гематогенного остеомиелита, были Staphylococcus aureus, стрептококки группы В, а в конце 60-х — начале 70-х годов — грамотрицательные бактерии. Позднее основными возбудителями бактериемии у новорожденных и детей младшего возраста вновь стали грамположительные кокки, особенно Staphylococcus aureus и коагулазоотрицательные стафилококки. Следует особо отметить, что эти ин фекции не были связаны с какими-либо конкретными штаммами, поступающими из общего резервуара, напротив, в этих случаях возбудителями были многочисленные штаммы, обитающие на коже больных и персонала, а также инструментарии.
В 1960 г. Wolinsky и соавт., обследовавшие грудных детей и медицинских работников, колонизированных определенными фаготипами Staphylococcus aureus, показали, что пе редача инсрекции происходит в результате прямого контакта, а не воздушно-капельным путем, как это считалось раньше. Обычно инфекция передается через руки. Таким путем распространяются из общего резервуара (т. е. руки) ряд микроорганизмов: Staphylococcus aureus, Klebsiella, Proteus mirabillis, Escherichia coli и Salmonella.
Потенциальным резервуаром внутрибольничной инфекции во всех стационарах яв ляются контаминированные растворы.
Качественное изменение состава гнойной микрофлоры, по мнению многих авторов за рубежом и в нашей стране, связано с широким применением антибиотиков. В США и развитых странах Европы эти изменения произошли раньше, чем в нашей стране, где пик стафилококковой инфекции пришелся на середину — конец 60-х годов. Особое место в силу тяжести течения и последствий среди гнойных хирургических заболеваний занимает гематогенный остеомиелит, который в 75% случаев встречался в детском воз расте. Остеомиелит в названный период времени характеризовался увеличением коли чества септических форм до 42,9%, летальности от 0,8 до 11,5% и переходом процесса в хроническую стадию в 40—50% случаев.
Наиболее яркая клиническая картина гематогенного остеомиелита и выраженные проявления последствий его свойственны стафилококковой инсрекции, что объясняется набором токсинов и ферментов этого микроорганизма.
Формы проявлений последствий гематогенного остеомиелита обусловлены харак терными для разных возрастных групп особенностями кровообращения в метаэпифизах длинных трубчатых костей .(рис. 11.4).
Так, у детей 1 -го года жизни существуют трансфизарные сосуды, по которым через зону роста сообщаются метафизарный и эпифизарный бассейны кровоснабжения. По этим сосудам из первичного очага воспаления, который всегда локализуется в метафизе, процесс распространяется в эпифиз. В исходе заболевания у больных этой возрастной группы разрушаются эпифизы длинных трубчатых костей и зоны роста.
В младшем и среднем детском возрасте метафизарный и эпифизарный бассейны разобщены бессосудистой зоной роста, поэтому гнойно-воспалительный процесс имеет тенденцию к метадиафизарной локализации, при которой происходит секвестрация раз личных по величине участков кости. В исходе заболевания у этих больных возникают патологические переломы, сформируются ложные суставы и дефекты длинных трубча тых костей.
567
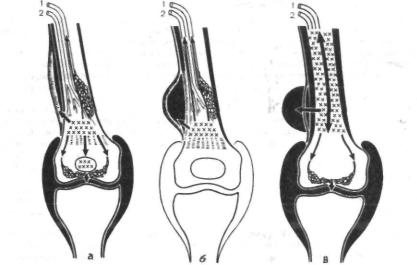
Рис. 11.4. Схема распространения остеомиелитического процесса в длинных трубчатых костях.
а — у новорожденных и детей первого года жизни; б — в детском возрасте; в — у подростков: 1 — вена; 2 — артерия.
В подростковом возрасте и у взрослых больных вновь появляется тенденция к рас пространению процесса в эпифиз. У больных этой возрастной группы процесс из метафиза распространяется на субхондральную зону эпифиза, вызывая секвестрацию сус тавного хряща. Процесс распространяется на суставную поверхность сочленованной ко сти и сопровождается выраженной картиной артрита. В исходе заболевания происходит синостозирование сочленованных костей, формируется анкилоз.
Последствия гематогенного остеомиелита новорожденных и детей 1-го года жиз ни. Характерными последствиями гематогенного остеомиелита новорожденных и детей 1-го года жизни (так называемого эпифизарного остеомиелита) являются патологиче ские вывихи бедра, деформации длинных трубчатых костей метаэпифизарной локали зации, укорочения конечностей.
Среди этих деформаций особое место занимает патологический вывих бедра. На основании клинико-рентгенологической картины и возможных механизмов возникно вения патологического вывиха — дистензионном и деструктивном — можно выделить четыре основных типа (рис. 11.5).
I тип — дистензионный самовправившийся вывих. Он возникает при растяжении капсулы сустава в остром периоде заболевания. Рентгенологически отмечаются латеропозиция проксимального конца бедренной кости, высокое стояние большого вертела. При своевременно начатом и адекватном лечении острого гнойно-воспалительного про цесса происходит самовправление. В ряде случаев формируются деформации прокси мального конца бедренной кости. У некоторых больных происходит «коллапс» головки бедренной кости, что связано с ранней нагрузкой конечности, отсутствием иммобили зации в остром периоде заболевания.
II тип — дистензионный вывих («состоявшийся»). Этот вывих возникает при руб цевании полости сустава в результате разрешения гнойно-воспалительного процесса, после чего самовправление становится невозможным. Рентгенологически головка бед ренной кости определяется вне впадины, отмечается выраженная патологическая антеторсия проксимального конца бедренной кости (рис. 11.6).
III тип — деструктивный патологический вывих. Характеризуется разрушением
568
