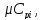- •Контрольное задание по теплотехнике
- •1.Требования к выполнению контрольной работы
- •2.Задание на контрольную работу
- •3. Что требуется выполнить
- •4.Контрольные вопросы
- •5. Пояснения к расчётам
- •Определение состава газовой смеси в массовых долях
- •Определение изменения внутренней энергии Δu, энтальпии Δh
- •Литература
5. Пояснения к расчётам
В качестве рабочих тел могут использоваться смеси, состоящие из нескольких газов. Если смесь состоит из идеальных газов, то для неё справедливы все соотношения, полученные для однородного идеального газа. Например, уравнение состояния идеального газа для 1кг смеси
P·v=Rсм·T;
для m>1 кг
P·V=m·Rсм·T,
где Rсм=R0/µсм– газовая постоянная смеси, Дж/(кг·град);
R0=8314 Дж/(кмоль·град) – универсальная газовая постоянная;
v – удельный объём смеси, м3/кг;
µсм – «кажущаяся» молекулярная масса смеси, кг/кмоль.
Для определения Rсм иµсм необходимо знать состав смеси, который может быть задан массовыми или объёмными долями.
Определение состава газовой смеси в массовых долях
Массовая доля
 ,
,
где
 - массаi-го газа
в смеси, кг;
- массаi-го газа
в смеси, кг;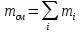 - масса смеси, кг.
- масса смеси, кг.
Определение удельной газовой постоянной смеси Rсм
и состава смеси в объёмных долях
Если смесь задана массовыми долями, то

или
 ,
,
где
 – характеристическая газовая постояннаяi-го компонента,
Дж/(кг·град);
– характеристическая газовая постояннаяi-го компонента,
Дж/(кг·град);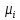 - молекулярная массаi-го
компонента, кг/кмоль.
- молекулярная массаi-го
компонента, кг/кмоль.
Объёмная доля, выраженная через массовую долю
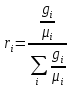 .
.
Определение «кажущейся» молекулярной массы смеси
через массовые и объёмные доли

или
 .
.
Определение плотности и удельного объёма смеси
при нормальных физических условиях
Нормальные физические условия:
P0 =760 мм рт.ст.=101300 Па,t0= 0°C= 273K.
Тогда
 ,
м3/кг,
,
м3/кг,
 ,
кг/м3.
,
кг/м3.
Определение параметров состояния смеси P, v, T
в характерных точках цикла и показателей политропы
Недостающие (не заданные) параметры состояния в характерных точках цикла (1, 2, 3, 4, 5) определяются из уравнения состояния
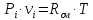
и по известным (заданным) соотношениям для характерных процессов цикла
 ;
;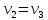 ;
; .
.
Показатель политропы:
для процесса 1-2
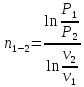 ,
,
для процесса 4-5
 .
.
Определение процессных теплоёмкостей Cv и Cp газовой смеси
и показателя адиабаты k
Теплоёмкости смеси при постоянном объёме и давлении в кДж/(кг·град)
 ;
;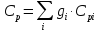 ,
,
где
 и
и - теплоёмкости каждого компонента в
составе смеси. Находятся с учётом
количества атомов в молекуле и молекулярной
массы по формулам (руководствуясь
таблицей 8):
- теплоёмкости каждого компонента в
составе смеси. Находятся с учётом
количества атомов в молекуле и молекулярной
массы по формулам (руководствуясь
таблицей 8):
 ,
, .
.
Таблица 8. Мольные теплоёмкости газов в соответствии
с молекулярно-кинетической теорией строения газов
|
Газы |
|
|
|
Одноатомные |
12,5 |
20,8 |
|
Двухатомные |
20,8 |
29,1 |
|
Трёх- и многоатомные |
29,1 |
37,4 |
Показатель адиабаты
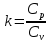 .
.
Процессные теплоёмкости для:
процесса 1-2
 ,
,
процесса 2-3
 ,
,
процесса 3-4
 ,
,
процесса 4-5
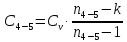 ,
,
процесса 5-1
 .
.
Примечание: для изотермических процессов теплоёмкость равна ∞.
Определение изменения внутренней энергии Δu, энтальпии Δh
и энтропии Δs в процессах, составляющих цикл
Изменение внутренней энергии в любом процессе
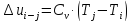 ,
кДж/кг.
,
кДж/кг.
Изменение энтальпии в любом процессе
 ,
кДж/кг.
,
кДж/кг.
Изменение энтропии в любом процессе (кроме изотермического)
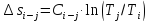 ,
кДж/кг.
,
кДж/кг.
Изменение энтропии в изотермическом процессе
 ,
кДж/кг.
,
кДж/кг.
Определение количества работы изменения объёма l,
совершаемой в каждом из процессов, и теплоты q,
подводимой (отводимой) в каждом из процессов, составляющих цикл
Для процесса 1-2:
 ,
кДж/кг;
,
кДж/кг;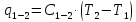 ,
кДж/кг.
,
кДж/кг.
Для процесса 2-3:
 ,
кДж/кг;
,
кДж/кг; ,
кДж/кг.
,
кДж/кг.
Для процесса 3-4:
 ,
кДж/кг;
,
кДж/кг;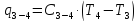 ,
кДж/кг.
,
кДж/кг.
Для процесса 4-5:
 ,
кДж/кг;
,
кДж/кг; ,
кДж/кг.
,
кДж/кг.
Для процесса 5-1:
 ,
кДж/кг;
,
кДж/кг; ,
кДж/кг.
,
кДж/кг.
Примечание: для изотермических
процессов теплота и работа рассчитываются
по формуле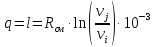 ,
кДж/кг.
,
кДж/кг.
Количество теплоты q1, подводимое в цикле, – это сумма количеств теплоты тех процессов, в которых теплота участвует со знаком «+»;
количество теплоты q2, отводимое в цикле, – это сумма количеств теплоты тех процессов, в которых теплота участвует со знаком «-»;
полезная работа lц – это алгебраическая сумма количеств работы во всех процессах цикла;
термический КПД цикла
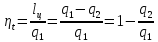 ,
,
термический КПД цикла Карно
 .
.
Примечание: при построении цикла
в диаграммеs-Tрекомендуется значение энтропии смеси
в состоянии 1 условно принять равным
нулю (s1=0). Тогда
состояние 2 на диаграмме находится по
значениям температурыT2и величины (с учётом знака изменения этропии).
Расчёт промежуточных точек в процессе
1-2 производится по произвольно выбранной
температуреTx
в интервале (T1-T2)
и изменению энтропии
(с учётом знака изменения этропии).
Расчёт промежуточных точек в процессе
1-2 производится по произвольно выбранной
температуреTx
в интервале (T1-T2)
и изменению энтропии .
Аналогично строятся остальные процессы
цикла.
.
Аналогично строятся остальные процессы
цикла.