
- •Реакция почвенного раствора как экологический фактор местообитания. Экологическое значение содержания кальция в
- •Почвенные растворы- источник минерального корневого (почвенного) питания растений .
- •Важнейшие катионы:
- •Концентрация почвенных растворов невысока
- •Реакция почвенного раствора Реакция
- •Кислотно-основные свойства почвы — это одна из важных характеристик ее плодородия. В природе
- •Хвойные леса и мох сфагнум способствуют усилению
- •Кислая реакция почв губительна. Они имеют плохие физические характеристики.
- •Распределение типов почв в зависимости от реакции почвенного раствора:
- •Экологическое значение содержания кальция в почве
- •Кальций – необходимый элемент питания
- •Кальций уравновешивает соотношение других
- •Богаты -глинистые земли; бедны – легкие.
- •Литература
- •Спасибо

Реакция почвенного раствора как экологический фактор местообитания. Экологическое значение содержания кальция в
почве
почве
Выполнил: студентка 2 курса биологического факультета
очной формы обучения группа 2 Г Мухаметзянова Р.И.
Мухаметзянова Р.И.

Почвенные растворы- источник минерального корневого (почвенного) питания растений .
Человек регулирует состав почвенного раствора, чтобы сделать его оптимальным для выращиваемых растений.
Минеральные, органические и органоминеральные вещества могут иметь форму истинно растворенных или коллоидно- растворимых соединений.

Важнейшие катионы:
Na+, K+, NH4+, H+, Ca2+, Mg2+, Al3+, Fe2+, Fe3+. Среди анионов преобладают НСО3-, СО32-, NO2-,
N03-, Сl-, SО42-, НРО42-, Н2РО4-.
Железо, алюминий и многие микроэлементы (Си, Со, Ni и др.) в почвенных растворах содержатся в форме комплексных органоминеральных соединений.

Концентрация почвенных растворов невысока
и колеблется в разных почвах от 10 мг до нескольких гр вещества на 1 литр раствора. В засоленных почвах содержание растворенных веществ может достигать нескольких десятков или даже сотен граммов в 1 литре.
В почвенном растворе находятся свободные кислоты и основания, что определяет его реакцию — кислотность, или напротив,
щелочность.
щелочность.

Реакция почвенного раствора Реакция
определяется концентрацией свободных водородных (Н+) и гидроксильных
(ОН-) ионов и измеряется водородным показателем рН — отрицательным логарифмом концентрации ионов водорода.
Почвы могут иметь нейтральную реакцию (рН=7), кислую (рН<7)
или щелочную (рН>7). Кислые почвы имеют рН 4,5-5, карбонатные и засоленные почвы — 8- 9 и выше. В процессе своей жизнедеятельности растения, потребляя из почвы анионы и катионы, выделяют в почву эквивалентное количество ионов Н+, ОН-, НСО3-, СО32-. Это
может привести к сдвигу реакции почвенного раствора в кислую или щелочную сторону.
Столь же существенное влияние на кислотность почвы оказывают микроорганизмы. .
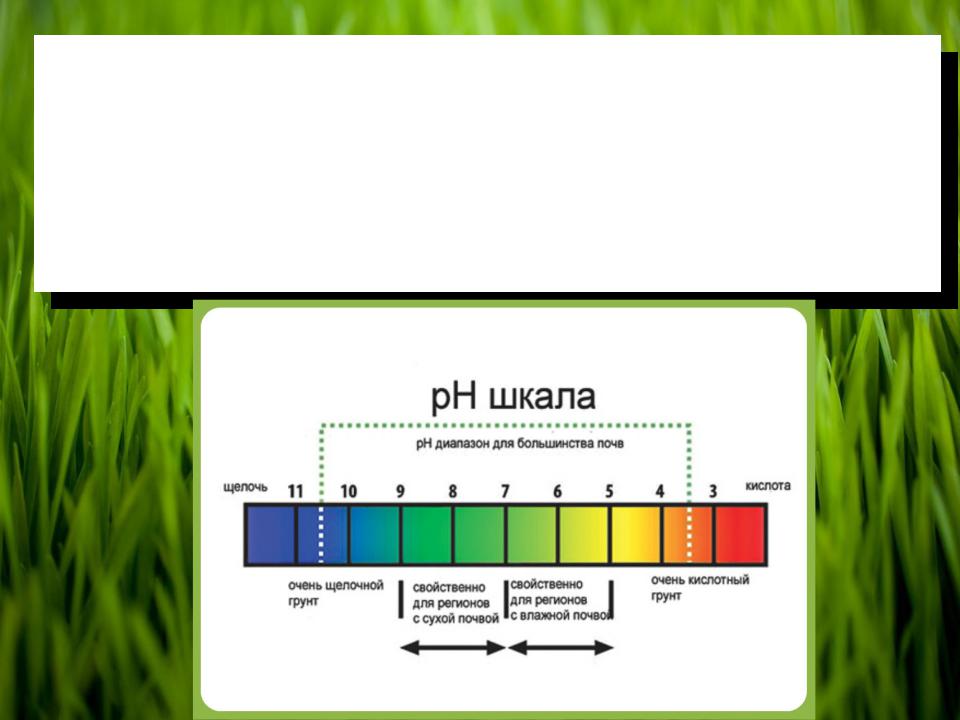
Кислотно-основные свойства почвы — это одна из важных характеристик ее плодородия. В природе распространение кислых почв связано с определенными условиями почвообразования. В одних случаях этот процесс приводит к потере
оснований (Са, Мg) и подкислению почвы (подзолистый процесс), в других — к обогащению почв основаниями (дерновый процесс). .

Хвойные леса и мох сфагнум способствуют усилению
кислотности. Напротив, лиственные леса и травянистая растительность лугов благоприятствуют накоплению оснований и поэтому почву не подкисляют.
Сельскохозяйственная деятельность человека вызывает изменение почвенной реакции. Вынос из почвы с урожаем оснований (Сa и Мg) приводит к усилению кислотности почвы. Длительная механическая обработка почвы также может привести
. .

Кислая реакция почв губительна. Они имеют плохие физические характеристики.
Сильнощелочная реакция почвы также губительна для большей части растений. При рН около 9-10 почвы имеет большую вязкость, липкость, водонепроницаемость.

Распределение типов почв в зависимости от реакции почвенного раствора:

