
- •Амины: классификация, номенклатура; химическая идентификация, спектральные характеристики. Представители: анилин, n–метиланилин, n,n–диметиланилин, толуидины, фенетидины, дифениламин.
- •Амины: реакции первичных, вторичных и третичных алифатических и ароматических аминов с азотистой кислотой; карбиламинная реакция (изонитрильная проба).
- •Ароматические амины: влияние аминогруппы на реакционную способность ароматического ядра; реакции галогенирования, сульфирования, нитрования. Защита аминогруппы.
- •Диазосоединения: номенклатура; реакция диазотирования (вопр. 29), механизм и условия проведения; строение солей диазония; влияние рН среды на устойчивость солей диазония.
- •Диазосоединения: реакции солей диазония с выделением азота, синтетические возможности реакций.
- •Диазосоединения: реакции без выделения азота; реакция азосочетания, ее механизм, диазо– и азосоставляющие; использование реакции азосочетания для идентификации фенолов и ароматических аминов.
- •Азосоединения: азокрасители (метиловый оранжевый), индикаторные свойства; основы теории цветности.
- •Альдегиды и кетоны: факторы, определяющие реакционную способность; реакции присоединения воды и спиртов, механизм, роль кислотного катализа в образовании ацеталей и полуацеталей.
- •Альдегиды и кетоны: механизм аn; присоединение гидросульфита натрия, циановодорода, магнийорганических соединений, значение этих реакций.
- •Альдегиды и кетоны: реакции присоединения-отщепления – образование иминов, оксимов, гидразонов, семикарбазонов, использование этих реакций для идентификации оксосоединений.
- •Альдегиды и кетоны: реакции восстановления – гидридами и комплексными гидридами, восстановление по Кижнеру–Вольфу и Клемменсену; реакции окисления альдегидов катионами серебра (I) и меди (II).
- •Карбоновые кислоты: кислотные свойства, строение карбоксилат-аниона; сравнительная характеристика кислотных свойств алифатических и ароматических моно- и дикарбоновых кислот; образование солей.
- •Карбоновые кислоты: реакции нуклеофильного замещения, механизм; образование функциональных производных.
- •Сложные эфиры: номенклатура, кислотный и щелочной гидролиз, аммонолиз; идентификация.
- •Дикарбоновые кислоты: специфические свойства. Представители: щавелевая, малоновая, янтарная, глутаровая, фталевая кислоты.
- •Фталевая кислота, фталевый ангидрид, фталимид; синтез фенолфталеина, его индикаторные свойства.
- •Аминокислоты: номенклатура, химические свойства как гетерофункциональных соединений; специфические реакции –, β–, –аминокислот; лактамы, дикетопиперазины, отношение к гидролизу.
- •Пептиды и белки: первичная структура, строение (электронное, пространственное) пептидной группы, частичный и полный гидролиз.
- •Кето-енольная таутомерия β – дикарбонильных соединений (ацетилацетон, ацетоуксусный эфир, щавелевоуксусная кислота). Реакции кетонной и енольной форм ацетоуксусного эфира.
- •Ацетоуксусный эфир: строение, таутомерия; синтез карбоновых кислот и кетонов.
- •Сульфаниловая кислота: строение, биполярная структура; реакция диазотирования (вопр. 29); сульфаниламид (стрептоцид), общий принцип строения сульфаниламидных лекарственных препаратов.
-
Сульфаниловая кислота: строение, биполярная структура; реакция диазотирования (вопр. 29); сульфаниламид (стрептоцид), общий принцип строения сульфаниламидных лекарственных препаратов.
Аминосульфоновые кислоты. Из этой группы аминокислот наибольшее практическое значение имеет п-аминобензолсульфоновая (сульфаниловая) кислота, представляющая собой внутреннюю соль (хотя записывается обычно в виде неионизированного соединения):

Она обладает одновременно и кислотными, и основными свойствами, т. е. является амфотерной:

Реакции с азотистой кислотой – сульфаниловая кислота реагирует амино-группой.
Амины разных типов с азотистой кислотой реагируют неодинаково. Некоторые продукты этих реакций, например соли диазония, имеют широкое практическое применение.
Первичные ароматические амины. В результате реакции первичных ароматических аминов с азотистой кислотой при низких температурах в присутствии сильных минеральных кислот образуются соли арилдиазония, а сама реакция называется реакцией диазотирования:

Сульфаниламиды. Амид сульфаниловой кислоты — сульфаниламид (R=Н), известный под названием стрептоцид, является родоначальником огромного семейства химиотерапевтических антибактериальных средств.
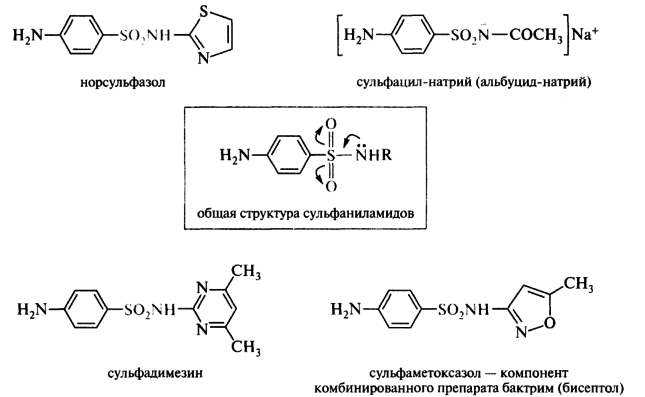
За более чем полувековой период существования сульфаниламидных препаратов было синтезировано свыше 10 тыс. производных, отличающихся главным образом природой заместителя R в сульфонамидной группе. Реже модификации структуры затрагивали аминогруппу, связанную с бензольным кольцом. Несколько десятков сульфаниламидов применяются в медицине, и в большинстве из них заместитель R представлен различными гетероциклическими структурами.
Сульфаниламиды плохо растворимы в воде, их растворимость повышается в щелочных средах благодаря наличию в молекуле NH-кислотного центра, обусловленного р,π-сопряжением в сульфанамидном фрагменте. Некоторые сульфаниламиды применяются в виде натриевых солей, например сульфацил-натрий.
Сульфаниламиды относятся к лекарственным средствам, механизм действия которых достаточно изучен на молекулярном уровне. Полагают, что сульфаниламиды конкурируют с п-аминобензойной кислотой (благодаря подобию геометрических параметров их молекул) на стадии биосинтеза фолиевой кислоты и других веществ, необходимых для жизни и развития многих форм микроорганизмов. Иными словами, являются антиметаболитами ПАБК, и принцип их действия заключается в блокировании биохимических процессов связывания ПАБК, в результате чего нарушается рост и размножение микроорганизмов. Таким образом, сульфаниламиды действуют только на те виды микробов, которые самостоятельно производят фолиевую кислоту, и не действуют на микроорганизмы, утилизирующие кислоту в готовом виде.
