
- •Теоретические основы металлокомплексного катализа
- •Строение и свойства комплексов переходных металлов
- •Ключевые реакции в гомогенном металлокомплексном катализе
- •Правило 16/18-электронов
- •Координирование (присоединение, диссоциация и замещение лигандов)
- •Окислительное присоединение и восстановительное элиминирование (redox-реакции).
- •Внедрение (по связи металл-лиганд)
- •Внешняя нуклеофильная и электрофильная атака
- •Механизмы реакций, катализируемых комплексами переходных металлов
- •Гидрирование
- •Изомеризация олефинов
- •Олигомеризация и полимеризация
- •Диспропорционирование (метатезис)
- •Окисление
- •Радикально-цепное окисление (гомолитический механизм)
- •Гетеролитический механизм окисления
- •Эпоксидирование олефинов органическими гидроперекисями
- •Окисление этилена до ацетальдегида
- •Присоединение протонодонорных веществ к олефинам и ацетиленам
- •Синтезы на основе окиси углерода
- •Карбонилирование метанола с получением уксусной кислоты
- •Карбоксилирование непредельных соединений
- •Гидроформилирование алкенов с получением альдегидов
- •Промышленные процессы металлокомплексного катализа
- •Особенности технологии процессов металлокомплексного катализа
- •Оксосинтез
- •Карбонилирование метанола
- •Cелективное окисление этилена в ацетальдегид (wacker-process)
- •Окисление циклогексана (производство циклогексанола и циклогексанона)
- •Эпоксидирование олефинов (халкон-процесс)
- •Олигомеризация этилена (shop-process)
-
Оксосинтез
Процесс оксосинтеза (гидроформилирования олефинов) протекает по суммарной реакции:
R-CH=CH2 + CO + H2 R-CH2-CH2-CH=O + R-CH(CH3)-CH=O (4.1)
и направлен на получения линейных альдегидов, служащих сырьем для получения линейных первичных спиртов по реакции гидрирования.
В настоящее время в промышленности используют четыре типа катализаторов на основе комплексов Со и Rh, различающихся лигандным окружением:
1. HCo(CO)4 - тетра-карбонил кобальт гидрид
2. HCo(CO)3PAlk3 - триалкилфосфин-три-карбонил кобальт гидрид
3. HRh(CO)(PPh3)3 - три-(трифенилфосфин)-карбонил родий гидрид
4. HRh(CO)(TPPTS)3 - три-(трифенилфосфинтрисульфат)-карбонил родий гидрид (ТРРТS = P(PhSO3Na)3).
Механизм катализа.
Каталитический цикл для кобальтовых катализаторов был рассмотрен выше (п. 3.3.7.3). Для родиевых катализаторов он выглядит так:
 (4.2)
(4.2)
Сравнение катализаторов оксосинтеза.
Сравнение условий и показателей процессов, катализируемых немодифицированным и модифицировнным карбонилом кобальта, и трифенилфосфиновым комплексом родия приведены в Таблице 4.2.
Таблица 4.2.
Показатели различных процессов гидроформилирования пропилена.
|
Показатели процесса
|
HCo(CO)4 |
HCo(CO)3PR3 |
HRh(CO)(PPh3)3 |
|
Температура, оС |
140-180 |
180-200 |
80-125 |
|
Давление, атм. |
200-300 |
50-100 |
7-25 |
|
Концентрация катализатора, % масс. от олефина |
0,1-1,0 |
0,5-1,0 |
0,01-0,001 |
|
Отношение н-/изо-продукт |
80/20 |
до 90/10 |
до 95/5 |
|
Состав продуктов, %: |
|
|
|
|
альдегиды |
80 |
- |
96 |
|
спирты |
10 |
80 |
- |
|
алканы |
1 |
15 |
1 |
|
Селективность образования продуктов С4, % |
82-85 |
> 85 |
> 90 |
|
Другие продукты |
9 |
5 |
2 |
Катализатор HCo(CO)4 является самым неустойчивым из всех перечисленных; при низких давлениях СО он разлагается до металлического кобальта, поэтому требует давления около 20-30 МПа в реакторе. Модифицированный триалкилфосфином кобальтовый катализатор HCo(CO)3PAlk3 значительно стабильнее, поэтому требует меньших давлений, но менее активен, поэтому температура процесса выше.
Родиевые катализаторы стабильны при низких давлениях, а также гораздо активнее кобальтовых (примерно в 1000 раз) и селективнее (как по соотношению н- и изо-продуктов, так и по образованию альдегидов). Условия проведения процесса на катализаторе HRh(CO)(PPh3)3 гораздо более мягкие. Но цена на родий выше цены на кобальт примерно в те же 1000 раз.
Важный показатель эффективности катализатора – соотношение нормальных и изомерных продуктов, поскольку целевыми являются продукты линейного строения. Согласно представлениям о механизме катализа и о влиянии природы комплекса на селективность реакции, соотношение н/изо-продуктов растет в ряду HCo(CO)4 < HCo(CO)3PAlk3 < HRh(CO)(PPh3)3.
Кроме того, кобальтовые катализаторы, в отличии от родиевых, обладают высокой каталитической активностью в реакции последовательного гидрирования образующихся альдегидов:
(4.3)

Это объясняется тем, что СоI, более жесткий центр, чем RhI и склонен к образованию жесткого лиганда RCH2O-, из которого затем получается спирт (4.3).
Сырье и продукты оксосинтеза.
1. Пропионовый альдегид, н- и изо-масляные альдегиды получают гидроформилированием этилена и пропилена, соответственно. Их используют далее для получения соответствующих кислот окислением, и соответствующих спиртов гидрированием.
Пропионовый и н-масляный альдегиды конденсируют с CH2O (при основном катализе) до трехатомных спиртов.
н-Масляный альдегид подвергают основнокаталитической конденсации до 2-этилгексеналя в производстве 2-этилгексанола.
2. Высокомолекулярные альдегиды получают гидроформилированием соответствующих -олефинов. Долее их гидрируют до соответствующих спиртов (С7-9 для пластификаторов и С10-18 для ПАВ).
Реакционные узлы в процессах оксосинтеза.
Реакция гидроформилирования является высоко экзотермической – тепловой эффект составляет 320-450 кДж/моль. Поэтому необходимо организовывать высокоэффективный теплоотвод в реакторе. Как правило, в качестве реактора используется пустотелая колонна с встроенными теплообменниками для отвода тепла.
Процессы гидроформилирования проводят в непрерывном режиме. В низ колоны подается смесь жидких компонентов реакционной массы с растворенным в ней катализатором и газообразная смесь СО + Н2 в мольном соотношении 1:1 с 2-3-х кратным избытком от стехиометрического соотношения с олефином. Смесь газов барботирует через жидкость, обеспечивая необходимый гидродинамический режим в реакторе. Непрореагировавшая газовая смесь отделяется по выходе из реактора от жидкой реакционной массы и рециркулируется.
В зависимости от используемого катализатора применяют различные схемы его регенерации и рецикла. Для рецикла неустойчивого HCo(CO)4 разработано три варианта технологии, описанные ниже.
Триадная схема.
В данной технологии используется склонность комплекса HCo(CO)4 к разложению до металлического кобальта при низких давлениях:
![]() (4.4)
(4.4)
Схема реакторного узла приведена на рисунке 4.2. Олефин, растворитель с катализатором из катализера (1) и смесь СО+Н2 подается в низ реактора (2). На выходе из реактора избыточные газы отделяются и направляются в рецикл, а жидкая реакционная смесь подается в декатализер (3), заполненный пористым адсорбентом (например, пемзой). На входе в декатализер давление смеси сбрасывается. При этом в декатализере происходит разложение каталитического комплекса по реакции (4.4) и металлический кобальт оседает на поверхности адсорбента. После полного насыщения адсорбента потоки переключают в обратном направлении и декатализер начинает работать в режиме катализера (1), где при высоком давлении СО и Н2 протекает реакция образования каталитически активного комплекса кобальта по реакции:
![]() (4.5)
(4.5)

Рис. 4.2. Триадная схема реакционно-регенеративного узла гидроформилирования.
Рецикл гидридных комплексов кобальта в виде натриевых солей.

Рис. 4.3. Схема реакционно-регенеративного узла гидроформилирования с рециклом катализатора в виде натриевого производного комплекса кобальта.
По данной технологии (Рис. 4.3.) конечная реакционная масса из реактора (1) подается в экстрактивную колонну (2) где контактирует с водным раствором карбоната натрия. При этом происходит обмен обладающего кислотными свойствами иона водорода в комплексе гидрокарбонила кобальта на катион натрия:
![]() (4.6)
(4.6)
Солевая форма карбонила кобальта переходит в водную фазу. Далее в сепараторе (3) происходит разделение газовой фазы от жидкой и разделение органической фазы от водной. Органическая фаза дополнительно промывается водой в колонне (2’) для более полного извлечения катализатора, и водный поток смешивается с водной фазой из сепаратора.
Объединенный водный раствор подается в регенератор (4), куда поступает также водный раствор серной кислоты (сверху) и водород. В регенераторе протекает реакция образования активной формы катализатора по реакции:
![]() (4.7)
(4.7)
Образующийся гидрокарбонил кобальта обладает высокой летучестью, поэтому выходит с верха регенератора вместе с потоком избыточного водорода и попадает в поглотительную колонну (5), где растворяется в потоке растворителя и олефина. Полученная смесь из колонны (5) направляется в реактор.
Рецикл кобальта в виде сульфата (испарительно-солевая схема).
При данном способе рециркуляции катализатора используют окислительно-восстановительные свойства кобальта.
Реакционная смесь на выходе из реактора (2) (Рис. 4.4) отделяется от газового потока (СО и Н2) и, после сброса давления, направляется в оксидатор (3), в который подают воздух и водный раствор серной кислоты. Оксидатор - полая барботажная колонна. Там протекает окисление кобальта до степени 2+ и образование его сульфата:
![]() (4.8)
(4.8)
После оксидатора смесь попадает в ректификационную колонну (4), где отгоняются продукты реакции гидроформилирования, а водный раствор сульфата кобальта из куба колонны поступает в карбонилообразователь (1). В карбонилообразователь также подают растворитель и газовую смесь СО и Н2. Под давлением окиси углерода и водорода в аппарате (1) протекает окислительно-восстановительная реакция образования гидрокарбонила кобальта(I):
![]() (4.9)
(4.9)
После карбонилообразователя смесь попадает в сепаратор (5), откуда, после разделения водной и органической фаз, водный раствор серной кислоты направляется в оксидатор, а органический раствор HCo(CO)4 - в реактор оксосинтеза.

Рис. 4.4. Испарительно-солевая схема реакционно-регенеративного узла гидроформилирования.
Рецикл стабильных катализаторов оксосинтеза (HCo(CO)3PAlk3, HRh(CO)(PPh3)3 , HRh(CO)(TPPTS)3) не требует специальных стадий превращения их в другие химические соединения и последующей регенерации, что значительно упрощает технологию. Продукты реакции отделяют от катализаторов либо отгонкой, либо экстракцией, и катализатор возвращают в реактор.
Испарительная схема.
Данная технология применяется при использовании в качестве катализатора устойчивых комплексов HCo(CO)3PAlk3 и HRh(CO)(PPh3)3. Схема реакционного узла отличается от приведенной на рисунке 4.4 отсутствием аппаратов 1, 3, 5.
Двухфазная технология.
Катализатор HRh(CO)(TPPTS)3 является новым катализатором оксосинтеза и отличается от предыдущих высокой водорастворимостью. Технология гидроформилирования пропилена с применением этого катализатора разработана компаниями Rurchemie и Rhone-Poulenc. Схема процесса представлена на Рисунке 4.5. Оксосинтез протекает в адиабатическом реакторе (1), представляющем собой барботажный реактор с мешалкой. После реактора в сепараторе (2) отделяется газ (СО, водород) от жидкой реакционной массы, которая затем в сепараторе (3) разделяется на водную и органическую фазы (так как масляный альдегид плохо растворим в воде). От органической фазы в колонне (4) газообразным потоком СО/Н2 отдувают растворенный пропилен и отправляют на рецикл. А водный слой с растворенным в нем катализатором через охлаждающий теплообменник (5) направляют снова в реактор. Туда же подают небольшой поток воды, для компенсации ее потерь во время рецикла.
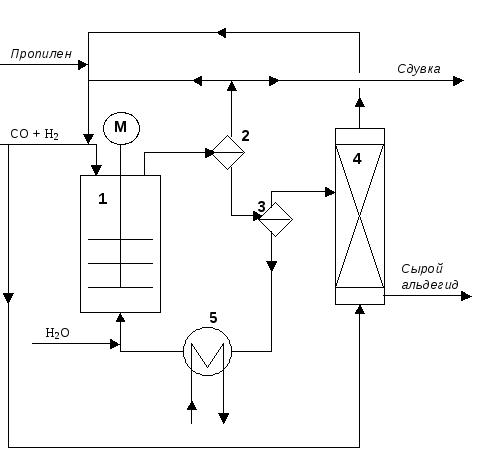
Рис.4.5. Схема реакционного узла двухфазной технологии гидроформилирования пропилена.
