
ТОХФ / 4 группа (ТОСиХК) / Химия и технология органических красителей / Лекции - Желтов - 2006 / Лекция 15
.pdf
15. Макрогетероциклические красители |
1(15) |
15. Макрогетероциклические красители
Хромофорная система макрогетероциклических красителей характеризуется наличием замкнутой системы сопряженных двойных связей в составе шестнадцатичленного или четырнадцатичленного макроцикла, который включает от восьми до четырех гетероатомов.
Таким образом, макрогетероциклические красители следует рассматривать как производные двух молекулярных систем гетероциклогексадецина и гетероцикло- тетрадецина.
13 X |
|
16 |
|
X 1 |
14 |
|
|
1 |
|
|
|
|
|
||||||
|
Y |
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
N |
|
N |
|
N |
|
|
|
Гекса аза - |
||||
|
|
|
N |
N |
|
|
|
|
|
||||||||||
|
|
|
|
11 |
|
|
|
|
4 |
||||||||||
|
|
|
|
|
|
N |
цикло тетрадецин |
||||||||||||
|
|
|
|
Y |
|
|
|
|
|
|
|
N |
|
N |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
9 X |
|
|
|
|
X 5 |
8 |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Гетероциклогексадецин Гетероциклотетрадецин
В зависимости от химической структуры макроцикла макрогетероциклические красители делятся на следующие группы.
Фталоцианиновые красители - производные октаазациклогексадецина, X=Y= N.
Сопряженные и несопряженные аналоги фталоцианина - производные гетероцик-
логексадецина, содержащие меньшее число атомов азота или включающие атомы азота и серы, например, гексаазадитиациклогексадецина, X = N ; Y = S.
Порфирины - производные тетраазациклогексадецина, X = CH; Y = N.
Гексаазациклотетрадециновые красители.
15.1. Фталоцианиновые красители
15.1.1. Особенности строения и цвет
Молекулы практически ценных фталоцианиновых красителей построены из четырех остатков бензо[с]пиррола (изоиндола), связанных тригональными атомами азота в тетрабензотетразапорфиновое кольцо, называемое фталоцианином (Ф).
|
|
N |
N |
|
N |
|
|
|
N |
N |
N |
||
|
|
NH |
HN |
|
||
c |
NH |
|
Ф , C32H18N8 |
|||
N |
NH |
HN |
||||
|
||||||
бензо[c]пиррол |
N |
N |
N |
N |
||
|
N |
|
||||
|
|
тетразапорфин |
|
тетрабензотетразапорфин |
||
|
|
(порфиразин) |
|
|||
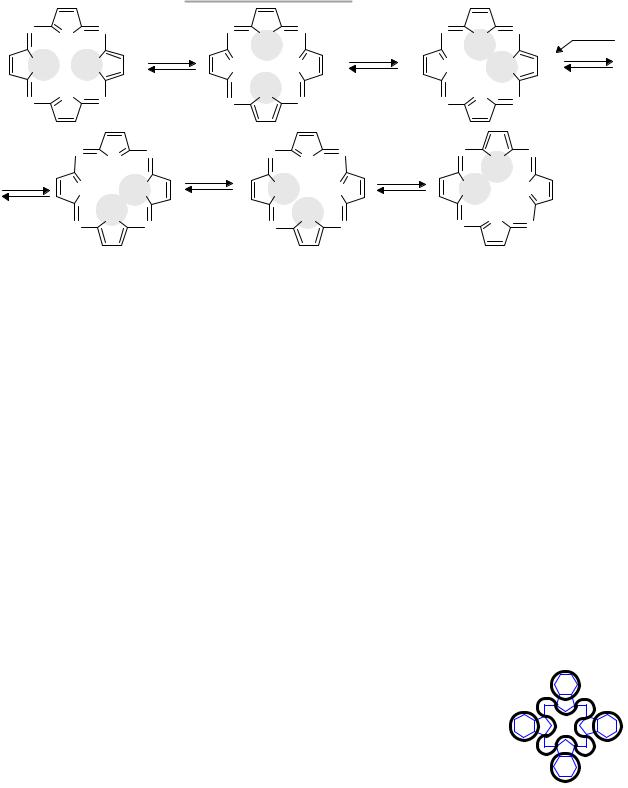
Общепринятая запись формулы фталоцианина не отражает равноценность изоиндольных фрагментов в молекуле. Тетразапорфин и его тетрабензопроизводное фталоцианин могут существовать в шести (6) таутомерных формах, каждая из которых описывается двумя (2) мезомерными структурами.
15. Макрогетероциклические красители |
2(15) |
В двух таутомерных формах иминные атомы водорода находятся у противолежащих N-атомов в макроцикле. По аналогии с географическими обозначениями стран света обозначим эти таутомерные формы как з-в (запад восток) и с-ю (север-юг) и т.д.
|
|
Зеркальное отражение - мезомерная |
форма |
|
||
N |
N |
N |
|
N |
N |
всего |
N |
N 4 формулы |
|||||
N |
|
|
|
N |
|
|
NH HN |
|
|
H |
|
H |
|
|
N |
N |
|
N |
HN |
|
N |
|
|
H |
|
N |
|
N з-в |
N |
N |
N с-ю |
N с-в |
||
N |
|
N |
||||
N |
N |
|
N |
N |
N |
N |
|
N |
|
|
N |
|
N |
N |
|
|
|
N |
NH |
H |
HN |
|
NH |
N |
|||
|
H |
|
|
H |
|
N |
N |
N |
|
N |
N |
N |
|
N |
ю-в |
N |
N |
|||
|
|
|
|
ю-з |
с-з |
|
В четырех других таутомерных формах, одна из которых (с-в) приведена в равновесии, атомы водорода располагаются у соседних N-атомов внутреннего окна макроцикла. Остальныетритаутомерные формы (ю-в, ю-з, с-з) представленные ввтором ряду.
Благодаря таким сложным таутомерным превращениям, во фталоцианине изоиндольные остатки и оба центральных иминных протона должны рассматриваться как вполне эквивалентные.
Тетразапорфин и фталоцианин относятся к типичным ароматическим соединениям. В их плоских молекулах число -электронов в сопряженной системе отвечает правилу Хюккеля m( )= 4n + 2. Действительно,
тетраазапорфин содержит 26 -электрона (n=6), которые предоставляют 11 двойных связей (22 е) и 2 пары неподеленных электронов у иминных атомов азота (4 е); фталоцианин содержит 42 -электрона (n=10), которые предоставляют 19 двойных
связей (38 е) и 2 пары неподеленных электронов у иминных атомов азота (4 е).
Ароматический характер фталоцианина подтверждает и выравненность связей в молекуле. Длина 16-ти C-N связей в макроцикле одинакова и составляет 1,34A, что очень близко к 1,38A - длине C-C связи в бензольном кольце. В то же время длины 8-ми C-C связей между бензольными кольцами и гетероциклом составляют 1,49A, то есть являются существенно простыми (обычная С-С связь – 1,54A).
Таким образом, сопряжение между -системами бензольных колец и макроциклом в известной мере ослаблено и в молекуле фталоцианина сосуществуют 5 квазиавтономных ароматических систем. Действительно при переходе от фиолетового-синего тетраазопорфина к красновато-голубому фталоцианину углубление окраски не столь значительно, как это можно было ожидать при аннелировании ароматического цикла четырьмя бензольными ядрами.

15. Макрогетероциклические красители |
3(15) |
Таким образом, основной причиной глубокой окраски фталоцианина следует считать наличие мощной макроциклической сопряженной системы, в которой степень делокализации -электронов еще более усиливается благодаря конденсированным бензольным кольцам.
В плоском тетраазопорфиновом кольце внутренние атомы азота сближены, а иминные протоны достаточно подвижны и могут замещаться катионами металлов. При нагревании фталоцианина в высококипящем органическом растворителе (дихлорбензол, тетралин) с солями металлов легко образуются соли или внутрикомплексные соединения.
Соли Na+, Ca2+, Mg2+ не очень стабильны. При обработке их кислотами происходит деметаллизация, в результате которой регенерируется свободный, "безметалль-
ный" фталоцианин.
C32H16N8Ca + H2SO4 CaSO4 + C32H18N8
Комплексные соединения с Cu2+, Ni2+, Co2+ чрезвычайно устойчивы. Так медьфталоцианин (Cu-Ф) выдерживает нагревание до 500 С без разложения, возгоняется в вакууме при 580 С, не разрушается в расплавленных щелочах и горячих кислотах.
N |
|
Cu-Ф |
|
N |
-полоса |
||
N |
|
||
N Cu N |
|
-полоса |
|
|
Ф |
||
N |
N |
||
|
|||
N |
|
 нм
нм
400 500 600 700
В видимой области электронного спектра поглощения фталоцианина присутствуют две интенсивные полосы, имеющие колебательную структуру. Они обусловливают ярко-голубую окраску этого соединения.
макс ,нм ( ) |
-полоса |
-полоса |
|
Фталоцианин (Ф) |
667 |
(125 000) |
702 (137 000) |
Медьфталоцианин (Сu-Ф) |
654 |
( 31 000) |
685 (219 000) |
Поскольку при комплексообразовании координационные связи с металлом образуют N-атомы четной альтернантной системы, комплексообразование не сопровождается заметным изменением цвета. Однако в спектре медьфталоцианина максимумы поглощения немного смещаются гипсохромно, но при этом интенсивность -полосы резко возрастает, а менее коротковолновая -полоса снижает свою интенсивность в четыре раза.
Металлокомплексы фталоцианина могут существовать в нескольких кристаллических структурах (полиморфных модификациях), которые отличаются физическими свойствами и в колористическом отношении.

15. Макрогетероциклические красители |
4(15) |
Для медьфталоцианина известны четыре полиморфные модификации, которые получили названия: неустойчивая , устойчивая , и модификации. Схематически строение кристаллов в -модификации и в устойчивой -модификации можно изобразить следующим образом.
Полиморфные модификации
11,9A |
медьфталоцианина |
9,8A |
3,8A |
|
4,8A |
26,5O |
|
44,8O |
-модификация |
|
Устойчивая -модификация |
В кристаллах плоские и близкие к квадрату молекулы фталоцианина меди располагаются параллельно друг другу на определенном расстоянии, образуя вертикальные «стопки». В зависимости от вида кристаллической модификации молекулы в «стопке» размещаются под определенным углом к вертикальной оси, причем в соседних «стопках» молекулы наклонены в разные стороны и образуют как бы двускатную крышу.
Существуют различия и во взаимном расположении «стопок» в кристалле. Модификации различаются и расстоянием между осями соседних «стопок». В соседних «стопках» молекулы медьфталоцианина располагаются на одинаковом уровне или могут быть смещены по вертикали на определенную величину.
Все четыре кристаллических модификации фталоцианина меди имеют голубой цвет, но отличаются оттенками и яркостью. Эти характеристики в определенной степени определяются результирующим эффектом процессов избирательного поглоще-
ния, отражения и рассеяния света агрегатами молекул в структуре кристаллической решетки.
Неустойчивая -модификация, имеет красноватый оттенок.
Устойчивая -модификация, имеет зеленоватый оттенок.
-Модификация, имеет ещё более выраженный зеленый оттенок.
-Модификация, имеет чисто-голубой цвет, но наименее яркая.
Наибольшей красящей силой и интенсивностью окраски обладает неустойчивая-модификация. Однако при действии органических растворителей или нагревании выше 200 С она переходит в -модификацию. Поэтому в лакокрасочных композициях вынуждены применять только устойчивую - или -модификации медьфталоцианина.
В процессе синтеза медьфталоцианин обычно образуется в -модификации, ко-
торую посредством переосаждения из концентрированной серной кислоты водой можно видоизменить. Но если продукт содержит некоторое количество монохлорзамещенного медьфталоцианина, его -модификация не может быть превращена в наиболее яркую -неустойчивую модификацию. Эти особенности полиморфизма медьфталоцианина следует учитывать при выборе методики получения фталоцианина.

15. Макрогетероциклические красители |
5(15) |
15.1.2. Способы получения фталоцианинов
Фталоцианины образуются при нагревании
–производных фталевой кислоты с веществами, выделяющими аммиак; или
–орто-фталодинитрила, который уже имеет N-атомы, необходимые для создания макрогетероцикла.
Проведение этой реакции с солью меди или другого металла приводит к образованию соответствующего металлфталоцианина. Реакцию ведут в расплаве реагентов или в среде органического растворителя. Добавка As2O5, борной кислоты H3BO3 или молибдата аммония (NH4)2 Mo2O7 катализирует процесс.
Фталоцианины в промышленности получают мочевинным и нитрильным спосо-
бами в расплаве реагентов или в высококипящем растворителе.
Мочевинный способ заключается в нагревании смеси фталевого ангидрида, мочевины и CuCl в присутствии H3BO3 до получения расплава и начала энергичной экзотермической реакции. При достижении 280-300 С смесь подвергают 2-х часовой выдержке. При этой температуре образование медьфталоцианина завершается, затем расплав охлаждают, измельчают, и технический продукт направляют на получение выпускной формы пигмента.
Реакция происходит по следующей схеме, необходимый для превращения аммиак образуется при термическом разложении мочевины.
O |
O |
|
CONH2 |
|
|
NH3 |
NH |
3 |
280°C |
||
O |
NH |
|
|
|
|
|
|
|
-2 H2O |
||
- H O |
- H2O |
CONH |
2 |
||
2 |
Фталимид O |
|
|
|
|
O |
|
Фталамид |
|
|
|
C N |
|
|
N |
|
|
|
|
Cu+ ( 2 CuCl ) |
|||
C N: |
|
|
N |
|
|
|
|
- CuCl2 |
|
||
Фталодинитрил |
|
|
+ |
|
|
Ион имино-изо-индоленина |
|
|
|||
Заключительная стадия процесса протекает как темплейтная (шаблонная) циклизация биполярных ионов имино-изо-индоленина, которые координируются вокруг катиона металла и затем рекомбинируют с образованием медьфталоцианина.
N + |
N |
N |
N |
N |
|
+ |
|
N |
|
N |
Cu |
N |
N |
Cu N |
+ |
N |
+ N |
N |
N |
N |
|
N |

15. Макрогетероциклические красители |
6(15) |
Нитрильный способ состоит в том, что смесь фталодинитрила, CuCl и NaCl нагревают до 140-145 С до получения однородного расплава, после чего температура самопроизвольно повышается до 260-280 С и в течение 30 минут завершается образование медьфталоцианина.
Использовние фталодинитрила позволяет сократить продолжительность реакции и получить более чистый металлокомплекс с более высоким выходом. Однако фталодинитрил очень токсичен и гораздо дороже фталевого ангидрида. Его получают пропусканием паров фталевого ангидрида и аммиака над бокситом или W2O3 при 420 С.
Получение фталоцианина меди методом "запекания" экономично, но в реакции вместе с основным продуктом образуется до 30% монохлорфталоцианина меди в результате участия в реакции при темепературе выше 250 С хлорной меди CuCl2.
4 С6H4(CN)2 + 2 CuCl C32H16N8-Cu + CuCl2
4 C6H4(CN)2 + CuCl2 C32H15ClN8-Cu + HCl
Из такого продукта нельзя получить колористически ценную -неустойчивую модификацию пигмента. Поэтому медьфталоцианин, предназначенный для этой цели, получают мочевинным способом в среде органического растворителя.
Мочевинный способ в среде растворителя. Смесь фталевого ангидрида, мо-
чевины, CuCl и As2O5 (мольное соотношение 4:11:1:0,1) нагревают в трихлорбензоле в течение 3-4 часов при температуре не выше 200°С, отводя выделяющееся тепло. Затем загустевшую реакционную массу разбавляют трихлорбензолом, охлаждают и после фильтрации и промывок медьфталоцианина получают индивидуальный металлокомплекс в -модификации.
Нитрильный способ в среде растворителя обычно применяют при производ-
стве безметального фталоцианина, из которого получают другие металлокомплексы
(Co-Ф, Al-Ф).
Фталодинитрил нагревают при 150 С в смеси изо-гептилового и гексилового спиртов (C7; C6) в присутствии алкоголятов натрия этих спиртов в течение 5 часов.
4 С6H4(CN)2 + 2 RCH2ONa + RCH2OH 2 RCH2OH + RCHO + C32H16N8-Na2
Образующийся динатрий фталоцианин отфильтровывают, обрабатывают метанолом и после отмывки водой едкого натра и спирта получают индивидуальный безметальный фталоцианин.
C32H16N8-Na2 + 2 CH3OH 2 CH3-ONa + C32H18N8
Из этого соединения приготавливают ценные полиграфические краски с оттенком зеленее, чем медьфталоцианина.
15.1.3. Фталоцианиновые пигменты
Пигменты, получаемые из медьфталоцианина, нерастворимы в большинстве органических растворителей, обладают выдающейся светостойкостью, термической и химической устойчивостью, яркостью и чистотой цвета. Благодаря этому они широко применяются в текстильной и полиграфической печати, для приготовления автомобильных эмалей, для крашения пластмасс и резины.

15. Макрогетероциклические красители |
7(15) |
Исходный фталоцианин меди, поступающий из реактора, характеризуется жесткой кристаллической решеткой и не может служить в качестве товарного пигмента. Различные кристаллические модификации медьфталоцианина с необходимыми цветовыми и пигментными свойствами получают в зависимости от способа обработки технического продукта.
Пигмент голубой фталоцианиновый У представляет собой в основном устой-
чивую -модификацию. Получают переосаждением продукта "запекания" (по мочевинному или нитрильному способу) из раствора в 90%-ой H2SO4 горячей водой с последующей промывкой методом декантации.
Пигмент голубой фталоцианиновый ЗУ, более чистый и яркий пигмент с зеле-
ным оттенком (устойчивая -модификация) также получают из продукта, содержащего примесь монохлорзамещенного. Для этого его растворяют в 100%-ой H2SO4, понижают концентрацию кислоты до 70% добавлением воды, отфильтровывают выпавший сульфат медьфталоцианина, а затем его переосаждают из концентрированной серной кислоты водой обычным способом.
Пигмент ярко-голубой фталоцианиновый К (неустойчивая -модификация)
получают из медьфталоцианина, приготовленного мочевинным способом в трихлорбензоле. Технический продукт, не содержащий хлорзамещенного фталоцианина, растворяют при 60 С в 96%-ой H2SO4, к охлажденному раствору при перемешивании добавляют касторовое масло (при параллельно происходящем сульфировании оно превращается в ПАВ) и смесь выливают горячую воду. В заключении высокодисперсный пигмент промывают декантацией, фильтруют и сушат.
Пигмент голубой фталоцианиновый Б4ЗУ ( -модификация) получают дис-
пергированием Пигмента ярко-голубого фталоцианинового К в ксилоле (диэтиленгли-
коле) в присутствии NaCl в шаровой мельнице. Эта модификация, обладающая чистым зеленоватым оттенком, применяется в полиграфии и в лакокрасочных составах, содержащих органические растворители
Пигмент зеленый фталоцианиновый получают исчерпывающим хлорированием медьфталоцианина в течение 20 часов при 180-190 С в расплаве AlCl3 и NaCl. Продукт, содержащий 14-16 атомов хлора переосаждают из серной кислоты водой.
15.1.4. Водорастворимые фталоцианиновые красители
Эта группа производных медьфталоцианина предназначена для крашения вискозы в массе, гладкого крашения природных волокон и бумаги из водных ванн.
Прямой бирюзовый светопрочный – динатриевая соль дисульфокислоты медьфталоцианина. Получают сульфированием пигмента 25%-ым олеумом при 50 С и последующим высаливанием из водного раствора.
|
25%-ый олеум, 50оС |
H O ; NaCl |
|
||
Cu-Ф |
|
|
Cu-Ф(SO3H)2 |
2 |
Cu-Ф(SO3Na)2 |
|
|
|
|||
Краситель может применяться и для получения Ba-соли, осажденной на гидроксиде алюминия, которая выпускается под названием Лак бирюзовый.

15. Макрогетероциклические красители |
8(15) |
Однако для получения водорастворимых фталоцианиновых красителей различных технических классов удобнее использовать в качестве промежуточного продукта
реакционноспособный тетрасульфонилхлорид медьфталоцианина.
Cu-Ф HSO3Cl ; SOCl2 ; 130OC Cu-Ф(SO2Cl)4
Cu-Ф(SO2Cl)4
При обработке медьфталоцианина хлорсульфоновой кислотой при 130 С в присутствии SOCl2 в течение 2 ч образуется тетрасульфонилхлорид. Его выделяют выливанием реакционной на холодный водный раствор NaCl, затем промывают на фильтре водой от минеральных кислот и высушивают.
Прямой бирюзовый светопрочный К получают аминированием тетрасуль-
фонилхлорида медьфталоцианина рассчитанным количеством водного аммиака с одновременным гидролизом оставшихся сульфохлоридных групп в сульфокислотные.
|
|
|
SO Cl |
|
SO- NH |
+ |
||
|
2 NH4OH |
|
2 |
2 H O |
|
3 |
4 |
|
Cu-Ф(SO2Cl)4 |
Cu-Ф(SO2NH2)2 |
Cu-Ф |
(SO2NH2)2 |
|||||
|
2 |
|||||||
|
|
SO Cl |
|
|
SO- NH + |
|||
|
|
|
|
|||||
|
|
2 |
|
3 |
4 |
|||
Этот краситель дает на хлопке более чистые по оттенку и более светопрочные окраски, чем предыдущий прямой краситель.
Хромовый бирюзовый для шелка содержит хелатный центр, обусловливающий способность красителя к комплексобразованию с солями хрома.
Cu-Ф-(SO2Cl)4 + H2N |
|
OH |
|
NaO3S |
|
|
|
OH |
|
|
|||||
|
H2O ; Na2CO3 Cu Ф |
|
|
|
|
||||||||||
|
|
COOH |
|
|
SO2 |
HN |
|
|
|
COOH |
|
||||
|
|
||||||||||||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
NaO3S |
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
||||||||||
|
SO3Na |
|
|
|
|
|
|
|
|
SO Na |
|
|
|||
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|||
Его получают араминированием тетрасульфохлорида медьфталоцианина двумя молями 3-амино-5-сульфосалициловой кислотой с последующим гидролизом оставшихся сульфонилхлоридных групп в содовом растворе.
Активные красители голубого и ярко-зеленого цвета также получают, исходя из тетрасульфонилхлорида медьфталоцианина. При этом с помощью тетрасульфонилхлорида медьфталоцианина ацилируют соединение – носитель активного центра:
амин, содержащий -сульфатоэтилсульфонильную группу или
арилендиамин, в котором вторая аминогруппа, способна ацилироваться цианурхлоридом или его замещенными.
Первым способом получают Ремазоль бирюзовый Г - винилсульфоновый активный краситель, исходя из 4-( - сульфатоэтилсульфонил)анилина.
|
|
|
|
SO2CH2CH2OSO3Na |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Na2CO3 ; pH 8 ; 25°C |
|
|
|
|
|
SO2CH2CH2OSO3Na |
|
||||
2 |
|
|
|
+ Cu-Ф-(SO2Cl)4 |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
(NaO S) - Cu-Ф - |
|
|
|
|
|
|
|
|
||||
H N |
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
SO NH |
|
|||||||||||
|
|
|
|
|
|||||||||||
2 |
|
|
|
|
3 |
2 |
|
|
2 |
|
|
|
|
|
2 |

15. Макрогетероциклические красители |
9(15) |
Вторым способом синтезируют Цибакрон бирюзовый ГФП монохлортриазиновый краситель, используя в качестве промежуточного арилендиамина 1,3-фенилендиамин-
4-сульфокислоту.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(SO3Na)2 |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2N |
|
|
|
NH2 |
|
|
|
|
|
|
Cu-Ф |
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
Cu-Ф-(SO2Cl)4 |
+ |
2 |
|
|
|
|
|
SO3Na |
|
|
|
|
|
|
|
|
O2S HN |
|
|
NH2 |
|
||||||||||||||||||
|
|
|
|
|
|
|
Cl |
|
|
(SO3Na)2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
SO3Na |
2 |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
Cl |
|
|
|
|
|
|
Cu-Ф |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
N |
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
N |
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
Cl |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
NH4OH |
|
|
O S |
|
HN |
|
|
|
|
|
NH |
|
|
|
|
N |
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
N |
|
|
Cl |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
SO3Na |
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|||
Соединяя голубой фталоцианиновый краситель с желтым аминоазокрасителем посредством триазинового кольца, получают зеленые активные красители с гибридной хромофорной системой.
15.1.5. Нерастворимые в воде фталоцианиновые красители
Жирорастворимый и растворимый в органических растворителях фталоцианиновый краситель получают обычным методом из трет-бутилфталодинитрила.
|
|
|
CN |
|
|
|
|
|
|
|
|
|
CuCl, мочевина, As O |
, ТХБ ; 200OC |
|
||
|
|
|
|
|||||
|
|
|
2 |
5 |
|
Cu-Ф-[-C(CH3)3 |
]4 |
|
|
|
|
|
|
|
|
||
(CH3)3C |
|
|
CN |
|
|
|||
|
|
|
|
|
|
|||
Наличие объемных трет-бутильных групп разрыхляет кристаллическую структуру красителя и вследствие ослабления межмолекулярного взаимодействия он легко сольватируется растворителем, переходя в раствор.
Кубовый голубой фталоцианиновый представляет из себя моносульфокислоту кобальтфталоцианина.
HN


 N
N
N
Na2S2O4 : NaOH 



 SO3Na
SO3Na
Co-Ф-SO3Na 

 N Co N
N Co N

N
HN |
N Лейкосоединение |
|
Кубового голубого фталоцианинового |
Это соединение практически нерастворимо в воде, но при восстановлении Na2S2O4 в щелочной среде дает растворимое лейкосоединение оливкового цвета. Благодаря плоской структуре молекулы и наличию гетероатомов, способных образовывать водородные связи с целлюлозой, лейкосоединение обладает сродством к хлопча-

15. Макрогетероциклические красители |
10(15) |
тобумажному волокну и после окисления дает светостойкие окраски, устойчивые к стирке, но мало устойчивые к действию хлора.
15.1.5. Фталоцианогены
Фталоцианогенами (фталогенами) называют водорастворимые соединения, образующие на волокне нерастворимый фталоцианиновый краситель.
В отечественной красящей композиции, называемой Фталоцианоген 4ЗМ, в качестве исходного реагента используют 1-амино-3-иминоизоиндоленин.
O |
NH2CONH2 |
, NH4 |
NO3 , |
|
NH2 |
_ |
|
|
|
|
|
|
NH2 |
||||||||
|
|
|
|
|
|
|
|
|
1 |
||||||||||||
|
|
O |
в PhNO2 , 180OC |
|
|
|
|
+NH |
NO3 |
|
NaOH |
|
|
|
N |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- NaNO3, -H2O |
|
|
3 |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
O |
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
NH |
|
|||||||||||||
|
|
|
|
|
|
|
1-амино-3-имино-изоиндоленин |
NH |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
Его получают нагреванием в нитробензоле при 170-190 С смеси фталевого ангидрида, мочевины и нитрата аммония. Образующуюся азотнокислую соль превращают в свободное основание действием щелочи.
В состав водной пасты, предназначенной для крашения хлопка, входит 1-амино- 3-иминоизоиндоленин, медная соль Трилона А (ЭДТУ кислоты), мочевина и неионо-
генное ПАВ. После нанесения состава на ткань её подвергают тепловой обработке при 135-140 С в течение 5 мин. В структуре волокна происходит реакция образования фталоцианина меди и образование окраски.
NH2 |
+ |
2+ |
|
135-140°С |
|||
N |
Cu |
||
N |
Cu-Ф |
||
- NH3 |
N- |
|
|
NH |
|
||
|
ион имино-изо-индоленина |
||
В аналогичных иностранных рецептурах применяют другие соли металлов и высококипящие органические растворители (ДМФА, этиленгликоль), что удорожает крашение фталоцианогеном.
15.1.6. Цианалы
Цианалами или алцианами называют растворимые производные фталоцианино-
вых красителей, которые содержат четвертичные аммониевые ( N+–R) или третич-
ные сульфониевые (=S+–R) группы. Для придания растворимости в воде и придания сродства к волокну достаточно ввести в краситель две такие группы.
Метод получения цианалов основан на реакции N- или S-алкилировании третичных аминов или алкантиолов хлорметильными производными медьфталоцианина. На примере четвертичной пиридиниевой соли рассмотрим, как осуществляют синтез и применяют цианалы в крашении.
Хлорметилирование фталоцианина по реакции Блана позволяет получать даже октазамещенное, но обычно ограничиваются меньшей степенью замещения.
