
ТОХФ / 4 группа (ТОСиХК) / Химия и технология органических красителей / Лекции - Желтов - 2006 / Лекция 10
.pdf
10. Индигоиды |
1 (10) |
10. Индигоидные красители
Название этого химического класса красителей происходит от Индиго - одного из природных красителей, который был известен человеку с глубокой древности и до сих пор не утратил своего значения в крашении текстильных материалов.
В молекулах индигоидных красителей присутствует тот же структурный элемент, что и в Индиго.
O |
H |
|
O |
где |
.. |
.. .. .. |
|
N |
|
A |
X ; A = NH ; Se ; S ; O , |
||
.. |
.. |
|
|
|
R |
.. .. .. |
|
|
X |
или |
R |
||
N |
|
|
A = C |
C |
||
H |
O |
Индиго |
O |
|
|
|
В большинстве индигоидных красителей X, A и карбонильная группа включены в циклическую систему и являются производными гетероциклических или ароматических соединений. Практически ценные индигоиды являются производными
индола (X=NH), бензотиофена (X=S), нафталина, аценафтена (A= H2C–CH2).
3 |
3 |
H2C CH2 |
2 |
|
2 |
1NH |
1S |
|
Поэтому индигоидные красители включают большое количество разнообразных, но структурно родственных соединений.
O |
S |
|
O |
Br |
O |
|
|
|
|
S |
|
||
S |
O |
|
NH |
NH |
NH |
Br |
|
|
|
O |
O |
|
|
Тиоиндиго красный С |
|
Индирубин |
Циба фиолетовый 3B |
|||
O |
Br |
|
O |
Br |
O |
|
|
|
|
|
|||
S |
NH |
|
NH |
|
S |
|
Br |
O |
|
|
|||
|
O |
|
|
O |
|
|
|
|
|
|
|
||
Тиоиндиго алый R |
Ализарин индиго синий 3R |
Тиоиндиго алый Ж |
|
|||
Из приведенных примеров видно, что индигоидные красители могут быть как симметричными молекулами (Индиго, Тиоиндиго красный С), которые построены из одинаковых гетероциклических остатков, так иметь и несимметричное строение.
При этом несимметричные индигоиды могут состоять:
из одинаковых гетероциклов, но связанных в разных положениях (Индирубин), то есть быть позиционными изомерами, или
из разных циклических систем (Циба фиолетовый B, Ализарин индиго синий R,
Тиоиндиго алый Ж)- гетероциклических или гетероциклической и ароматической.
Условные названия индигоидных красителей принято составлять путем перечисления гетероциклических и ароматических систем, которые образуют краситель, с добавлением слова «индиго». Кроме того, цифрами обозначаются положения, в которых остатки исходных соединений связаны друг с другом двойной связью.
10. Индигоиды |
2 (10) |
Отметим, что в названии красителя указываются название “родительского” цик-
ла, а не производного, остатки которого фактически входят в молекулу красителя (индол, а не индоксил, бензотиофен, а не гидроксибензотиофен, аценафтен, а не аценафтенхинон).
Тогда в соответствии с этими правилам вышеприведенные красители называют-
ся:
Индиго |
2,2’-бис(индол)индиго |
Индигорубин |
2,3’-бис(индол)индиго |
Циба фиолетовый 3B |
2-индол-2’-бензотиофениндиго |
Тиоиндиго красный С |
2,2’-бис(бензотиофен)индиго |
Ализарин индиго синий R |
2-индол-2’-нафталининдиго |
Тиоиндиго алый Ж |
2-бензотиофен-2’-аценафтениндиго |
В зависимости от природы гетероциклических остатков, из которых построены молекулы практически ценных индигоидных красителей, они делятся на следующие четыре группы:
бис(индол)индигоиды; бис(бензотиофен)индигоиды; индол бензотиофен индигоиды; бензотиофен арен- и индол арен индигоиды.
Методы их синтеза и свойства будут рассмотрены позднее.
10.1. Строение и хромофорная система Индиго
Наиболее поразительной чертой Индиго и его производных является неожидан-
но глубокая окраска при сравнительно простом химическом строении молекул ин-
дигоидов. В самом деле, замечательно, что такая небольшая молекула как Индиго может быть синей. Синие азо- и антрахиноновые красители обычно содержат несколько ЭД и ЭА заместителей во взаимносопряженных положениях развитой системы сопряженных двойных связей, обеспечивая тем самым максимальное углубление цвета.
Многочисленные исследования показали, что феномен глубокой окраски объясня-
ется:
особенным строением хромофорной системы индигоидов,
высокой полярностью молекул этих красителей,
значительным влиянием межмолекулярных взаимодействий, способствующих углублению цвета.
существованием молекул в энергетически выгодной транс-конформации,
Вклад этих факторов при формировании окраски различных групп индигоидных красителей не одинаков и зависит:
от природы гетероатомов, входящих в состав хромофорной системы, и от дополнительных структурных элементов, которые влияют на чувствительность
молекул красителей к изменению среды и агрегатного состояния. Рассмотрим влияние этих факторов подробнее.
10. Индигоиды |
3 (10) |

10. Индигоиды |
4 (10) |
10.1.1. Строение хромофора
Рентгеноструктурный анализ показал, что молекула Индиго почти плоская, существует как в твердом состоянии, так и в растворах в транс-конформации. В молекуле длины центральной С=С связи и C=O связей карбонильных групп несколько больше, чем у типичных двойных связей этого типа.
1,24A O |
1,37A |
|
||
H |
|
|||
|
|
N |
|
|
1,38-1,39A |
N |
O |
1,35A |
|
H |
||||
|
|
|||
Типичные длины связей в A
Олефиновая С = С |
1.34 |
Карбонильная С = O |
1.22 |
Пиррольная C – N |
1.42 |
Бензольная С – С |
1.37 |
Напротив, связь C-N в Индиго существенно короче простой пиррольной, однако длины С-С связей в конденсированных кольцах бензола примерно такие же, как в бензоле. Эти данные свидетельствуют о значительном вкладе в основное состояние молекулы Индиго, традиционно описываемой структурой “a”, таких резонансных форм, как внутриионизированные структуры “б” и “в”, которые имеют большую энергию.
O- H |
O |
H |
O |
H |
|
|
N |
|
N |
|
N |
.. |
+ |
.. |
.. |
+ |
.. |
N |
|
N |
|
N |
O - |
H |
O |
H |
O |
H |
|
|
б |
|
а |
|
в |
E 
 б или в
б или в
E'
 a + б + в
a + б + в
E
a
В возбужденном состоянии эти две важнейшие резонансные формы - биполярные структуры “б” и “в” с разделенными зарядами и существенно простыми С-О связями и существенно двойными C-N связями становятся главными. При этом два бензольных кольца полностью сохраняют ароматический характер.
На основании этих данных можно предположить, что между основным и возбужденным состоянием молекулы Индиго имеется заметно меньшее различие в энергииE′, чем можно было бы ожидать для классической структуры “a”. Так объясняется сравнительно небольшая энергия фотовозбуждения Индиго и его глубокая окраска.
Следовательно, цвет Индиго и его производных обусловлен взаимодействием двух электронодонорных NH-групп с двумя электроноакцепторными карбонильными группами через этиленовый мостик, общий для обеих систем, а два бензольных кольца не являются существенной частью хромофора.
Квантово-химический расчет подтверждает такую модель и энергетику основного и возбужденного состояний Индиго, но согласно расчетам Индиго должен иметь не синий, а более высокий, красный цвет.
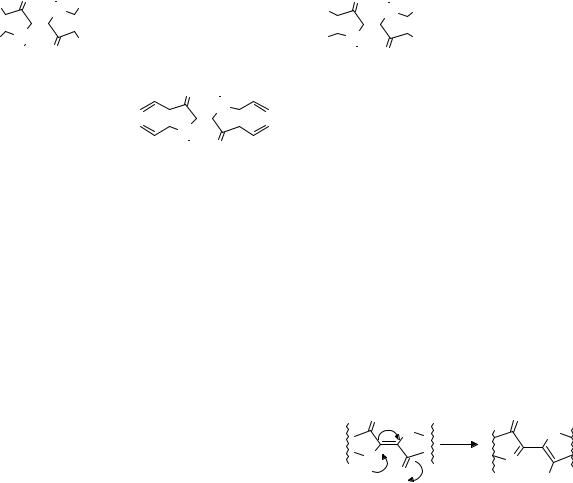
Это кажущиеся противоречие можно объяснить, если сопоставить спектральные характеристики двух модельных соединений (1) и (2) и Индиго в парах.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
10. Индигоиды |
5 (10) |
|||||||||||
Me |
O |
H |
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
H |
||||||||
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
Me |
|
|
|
N |
|
Me |
|||||||
Me |
|
|
|
|
|
|
|
H |
|
макс 480 нм |
|
|
|
|
|
|
|
||||||||||||
H |
|
|
|
|
|
|
|
Me |
(1) |
|
|
|
|
|
|
|
|
|
|
|
(2) макс 528 нм |
||||||||
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Me N |
|
|
|
|
|
Me |
|||||||||
H |
|
Me |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
H |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||||||
оранжево-красный |
|
|
|
|
|
|
|
|
|
|
|
|
|
красный |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
макс 540 нм (пары) |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пурпурный |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
O |
|
|
|
|
|
|
|
||||||
В молекулах модельных красителей отсутствуют бензольные кольца, но в них имеется главный элемент хромофора индигоидов – две перекрещивающиеся мероциа-
ниновые системы.
Сразу же обращает на себя внимание, что наращивание общего размера -систе- мы в ряду этих соединений (замена простой связи между карбонилом и NH-группой в соединении (1), на -связь в соединении (2), и замыкание циклической системы с помощью бензольного кольца в Индиго) сопровождается относительно небольшим углублением цвета от оранжево-красного до пурпурного. При этом величина батохромного сдвига полосы поглощения в видимой области ( макс) составляет всего 60 нм, то есть оказывается весьма скромной.
Из приведенных данных следует, что
первичный хромофорный элемент Индиго дей-
ствительно состоит из двух перекрещивающихся мероцианиновых структур, связанных общим этиленовым мостиком, в котором и совершается электронный переход, определяющий красный цвет красителя,
O .. |
h |
O .. |
X |
X |
|
X |
|
+ |
|
X |
|
.. |
|
|
O |
|
:O:- |
|
|
.. |
Аш (H) - хромофор индигоидов
Клессингер, Лютке (1968 г)
бензольные кольца в формировании окраски Индиго играют второстепенную, вспомогательную роль,
синий цвет Индиго в твердом состоянии и растворе обусловлен ассоциацией молекул красителя и конформационными причинами.
Эффект поперечного связывания или “кросс-сопряжения” чрезвычайно силен, и поэтому, подчеркивая особый характер всех индигоидных систем, Клессингер и Лютке предложили называть присущие им хромофоры “Аш-хромофорами” - по форме основного структурного фрагмента, напоминающего латинскую букву H.
10.1.2. Межмолекулярные взаимодействия
На основании данных рентгеноструктурного анализа было установлено, что Индиго в твердом состоянии образует устойчивый ассоциат с помощью межмолеку-
лярных водородных связей.
Водородные связи возникают между водородом иминогруппы одной молекулы и кислородом карбонильной группы другой молекулы. В таком ассоциате каждая молекула связана с четырьмя другими молекулами Индиго.

10. Индигоиды |
6 (10) |
O |
H |
|
N |
N |
|
H |
O |
O |
H |
|
N |
N |
|
H |
O |
Полимерность Индиго является причиной его плохой растворимости и неожиданно высокой температуры плавления (390-392°С). Факт ассоциации молекул Индиго в твердом состоянии подтверждается и изменением окраски этого красителя в растворах. Цвет Индиго за-
метно повышается при растворении, поскольку в ре-
зультате сольватации молекул разрушаются межмолекулярные водородные связи.
При этом повышение окраски и величина гипсохромного сдвига растет с уменьшением полярности органического растворителя, то есть наблюдается положительная сольватохромия. Сольватохромией называют зависимости окраски вещества от природы и полярности растворителя.
Растворитель → |
|
Уменьшение полярности среды |
|
||
В KBr |
Этанол |
CCl4 |
В парах |
||
|
|||||
Индиго, макс, нм |
660 |
606 |
588 |
540 |
N,N’-диметилиндиго, макс, нм |
672 |
656 |
640 |
633 |
Цвет Индиго зависит также и от его агрегатного состояния, он изменяется от красного в паровой фазе до фиолетово-синего в аморфном состоянии и до синего в кристаллах.
Агрегатное состояние красителя |
В парах |
Аморфное |
Кристаллическое |
|||
O.....H |
Индиго |
|
|
|
||
|
|
N |
540 |
575 |
656 ( 116) |
|
N |
|
|
макс, нм |
|||
..... |
|
|
|
|||
H |
|
|
|
|||
|
O |
|
|
|
|
|
O H3C |
N,N’-диметилиндиго |
|
|
|
||
|
|
N |
633 |
666 |
672 ( 39) |
|
N |
|
|
макс, нм |
|||
|
|
|
|
|
||
|
|
|
|
|
|
|
CH |
O |
|
|
|
|
|
|
|
3 |
|
|
|
|
В отличие от Индиго, N,N’-Диметилиндиго, Тиоиндиго и другие индигоиды, у которых нет водорода связанного с гетероатомом , не обладают такой чувствительностью к изменению среды. Из этого можно сделать вывод, что синяя окраска и соль-
ватохромия Индиго вызвана образованием межмолекулярных водородных связей.
Однако и в мономолекулярном состоянии в индигоидах - производных индола, повидимому, сохраняются внутримолекулярные водородные связи.
10.1.3. Конформационный эффект
Индигоидные красители имеют фиксированную ориентацию карбонильных групп и поэтому могут существовать в двух стериоизомерных формах, которые различаются энергией основного состояния и окраской.
Так в случае Тиоиндиго красного С помимо более устойчивой транс-формы, имеющей пурпурный цвет, может быть получена и цис-форма, обладающая более вы-
соким оранжевато-красный цветом.

|
10. Индигоиды |
|
|
7 (10) |
O |
|
|
O |
O |
S |
транс-форма |
цис-форма |
|
|
S |
макс 546 нм |
макс 490 нм |
S |
S |
O |
пурпурный |
оранжево-красный |
|
|
|
Тиоиндиго красный С |
(CHCl3) |
|
-h |
h |
O |
O |
O |
|
|
S |
|
|
|
|
+ |
+ |
S |
|
|
S |
S |
|
|
O
Этот переход в цис-форму совершается в результате поглощения красителем энергии света, переводящего молекулу в возбужденное состояние, в котором происходит поворот одной половины молекулы вокруг простой С-С связи с последующей дезактивацией. Обратный переход в транс-форму совершается при выдерживании образца в темноте.
Однако явление фотохромии не наблюдается в случае Индиго и индолиндигоидов, в которых транс-форма стабилизируется внутримолекулярной водородной связью. Этот пример убедительно показывает, что транс-конформация также вносит определенный вклад в углублении цвета Индиго, хромофор которого обусловливает лишь пурпурную окраску этой молекулы.
10.2. Закономерности цвета в производных Индиго
10.2.1. Природа гетероатома
Красители, структурно близкие Индиго, получаются при замене NH-групп другим гетероатомом, обладающим неподеленной парой электронов.
O |
|
O |
X |
O |
X |
|
X |
||
.. |
+ |
.. |
.. |
.. |
|
+ |
|||
X |
б |
X |
O а |
X |
O |
|
O в |
||
Введение гетероатома несущего неподеленную пару электронов на более диффузных, чем у азота 3p -орбитали (сера) и 4p -орбитали (селен) или атома с большей электроотрицательностью (кислород), сопровождается ослаблением электронодонорного эффекта этого заместителя.
-X- |
макс, нм (цвет) |
Растворитель |
|
|
|
|
|
NCH3 |
650 (Голубой) |
Ксилол |
|
NH |
605 |
(Синий) |
C2H2Cl2 |
Se |
570 |
(Фиолетовый) |
CHCl3 |
S |
546 |
(Красный) |
CHCl3 |
O |
420 |
(Желтый) |
CHCl3 |
В рзультате такой модификации Аш-хромофора в ряду Селеноиндиго, Тиоиндиго, Оксоиндиго понижается перекрещивающееся p, -взаимодействие с электроноакцепторными C=O группами, вклад поляризованных структур в основное состояние молекул уменьшается и цвет соответствующих производных Индиго повышается.

10. Индигоиды |
8 (10) |
Разбавленные кислоты и щелочи не влияют на цвет индигоидных красителей. Однако сильные кислоты и основания вызывают их ионизацию. Так в концентрированной серной кислоте индигоиды углубляют окраску. Протонирование идет по карбонильной группе, и это увеличивает ЭА эффект этого заместителя, результатом чего является батохромный сдвиг.
|
O |
96%-H2SO4 |
+OH |
|
|
||
|
S |
|
S |
макс |
641нм |
||
|
S |
|
|
S |
|
||
|
бордо |
|
+ |
голубой |
|
||
O |
O |
|
O |
OH |
|
||
H |
t-BuONa в t-BuOH |
H |
|
|
|||
|
N |
N:- |
N |
макс |
773 нм |
||
N |
|
- |
H+ |
|
|||
H |
O |
|
.. |
O |
зеленый |
|
|
синий |
|
|
|
||||
Напротив, в присутствии трет-бутилата натрия происходит монодепротонирование Индиго по иминогруппе. Уменьшение электроотрицательности отрицательно заряженного (N–) азота усиливает электронодонорность этой группы и ионизированный Индиго приобретает зеленый цвет.
10.2.2. Несимметричные индигоиды
Цвет несимметричных индигоидных красителей 2,2’-ряда зависит от обеих со-
ставных частей молекулы и определяется вкладом предельных структур, возни-
кающих в возбужденном состоянии.
Так, например, цвет индолбензотиофениндигоида Кубового фиолетового соответствует цвету эквимольной смеси двух симметричных красителей, Индиго и Тиоиндиго красного С. Это свидетельствует о примерно одинаковых вкладах предельных структур “б” и “в” в фотовозбужденное состояние.
O |
NH |
|
O |
|
O |
|
|
S |
|
S |
|
|
|
|
|
||
NH |
O |
|
NH |
|
S |
Индиго |
|
O |
|
O |
|
|
O |
Кубовый фиолетовый |
O- Тиоиндиго красный С |
||
|
|
||||
|
в |
+ |
S |
S |
б |
|
|
+ |
|||
|
|
NH |
O - |
NH |
|
|
|
|
O |
|
|
Цвет Кубового фиолетового 4 (C.I.) свидетельствует о преобладании предельной структуры, характерной для Индиго красного С, поскольку его пурпурный цвет ближе к красному, чем к синевато-голубому - цвету несимметричного красителя Гелиндон си-
ний B.

O
S 


 S
S 

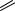 O
O
Тиоиндиго красный С
O
S
б 

 +
+

S  O -
O -
|
10. Индигоиды |
O |
Cl |
|
S |
|
S |
|
O |
|
Кубовый фиолетовый 4 |
Cl |
O- |
S 

 +
+

 S
S
O
9 (10)
O |
Cl |
|
S |
S |
O |
Cl |
Гелиндон синий B
Cl
в

10. Индигоиды |
10 (10) |
Цвет несимметричных индигоидных красителей 2,3’-ряда определяется в основ-
ном природой остатка, связанного в положении 2, и обычно более или менее близок к цвету симметричного 2,2’-красителя, образованного из двух таких остатков.
Например, Кубовый коричневый 2R ближе к цвету красителя Тиоиндиго красно- коричневый Ж, чем к оранжевому тетрахлоризоинидиго.
|
|
Cl |
|
|
Cl |
O |
O |
|
|
|
O |
|
|
HN |
Cl |
||
S |
|
Cl |
|
||
|
|
NH |
|||
S |
S |
NH |
Cl |
|
|
|
O оранжевый |
||||
|
|
|
|||
O |
|
O |
|
|
|
Тиоинидиго красно-коричневый Ж |
Кубовый коричневый 2R |
|
|
Cl |
|
Тетрахлоризоиндиго |
|||||
10.2.3 Влияние заместителей
Как было показано выше, бензольные кольца играют в формировании цвета Индиго и его производных лишь второстепенную роль. Однако электронный эффект и особенно положение заместителей в кольцах оказывают заметное влияние на цвет этих красителей, что показывают данные электронных спектров соответствующих замещенных Индиго (X = NH) и Тиоиндиго (X = S).
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Положение полосы в ЭС, макс, нм |
|
|
||||
|
Гетеросистема |
|
Положение за- |
|
Индиго (C2H2Cl4) |
Тиоиндиго (ДМФА) |
||||||||||||||||||||
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
местителей |
|
5,5’- |
|
6,6’- |
5,5’- |
|
6,6’- |
||
4' |
|
|
|
|
|
1X |
|
7 |
|
NO2 |
|
580 |
|
635 |
513 |
|
567 |
|||||||||
|
|
|
3' |
|
|
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
|
|
|||||
5' |
|
|
|
|
|
H |
|
|
605 |
|
543 |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
.. |
2' .. |
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
2 |
|
|
|
|
|
|
|
|
Cl |
|
620 |
|
590 |
556 |
|
539 |
|||||||
6' |
|
|
X |
|
|
|
|
3 |
|
|
5 |
|
|
|
||||||||||||
7' |
|
1' |
|
O |
4 |
OC2H5 |
|
645 |
|
570 |
584 |
|
473 |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
Введение ЭД заместителей в 5,5’(пара)-положения или 7,7’(орто)-положения к электронодонорной NH- или S-группе вызывает батохромный сдвиг полосы поглощения в видимой области спектра и увеличивает её интенсивность, а присутствие ЭА заместителей в этих положениях приводит к гипсохромному сдвигу.
Напротив, введение ЭД заместителей в 6,6’(пара)-положения или 4,4’(орто)-по- ложениях к электроноакцепторной C=O группе вызывает гипсохромный сдвиг полосы поглощения, а присутствие ЭА заместителей в этих положениях приводит к батохромному сдвигу. Теория валентных связей (ВС) объясняет эффект замещения следующим образом.
ЭД заместители в положениях 5 или 7 сопряжены с NH-группой в гетероцикле и будут стабилизировать возбужденное состояние.
O |
H |
O- |
H |
|
|
|
N |
|
N |
|
|
|
.. |
|
+ |
.. Углубление окраски |
|
N |
.. |
N |
|||
|
|||||
D |
|
D |
|||
H |
O |
H |
O |
|
Они увеличивают электронную плотность у атома азота (N ) с дефицитом электронов. Это облегчает электронный переход в хромофоре и приводит к углублению окраски.
