
- •Метаболизм
- •Обратная связь за счет участия в цепи превращений аллостерического (регулятор-ного) фермента.
- •У высших организмов регуляция метаболических превращений осуществляется гормонами.
- •Третий механизм регуляции метаболизма основан на изменении концентрации ферментов в зависимости от потребности в обеспечиваемых ими превращениях.
- •Катаболические превращения
Метаболизм
Совокупность ферментативных реакций, протекающих в живых клетках, называется метаболизмом. Метаболические процессы решают четыре основных задачи:
-
Снабжение организма свободной химической энергией за счет преобразования энер-гии солнечного света или за счет превращения богатых энергией веществ, поступа-ющих с пищей.
-
Превращение пищевых веществ в строительные блоки, используемые клетками для синтеза макромолекул и других биогенных веществ.
-
Биосинтез белков, полисахаридов, нуклеиновых кислот и других клеточных элемен-тов из этих строительных блоков.
-
Синтез новых веществ, отсутствующих в пище, разложение лишних веществ, посту-пающих в клетку, а также разложение выполнивших свою роль биомолекул.
-
Метаболические процессы сопровождаются выделением тепла, поддерживающего оптимальный температурный интервал для протекания биохимических превраще-ний, хотя есть и специальный механизм окислительного превращения субстратов, предназначенный только для поддержания температуры тела.
Из этого следует, что метаболические превращения включают обмен веществ и био-энергетические процессы.
Высокая скорость и избирательность ферментативных реакций подразумевают, что метаболизм основан на высокоорганизованной и согласованной работе взаимосвязан-ных мультиферментных систем. Простые, единичные превращения веществ в биоло-гических системах редки. Чаще всего речь идет о линейных или циклических путях превращений, протекающих при согласованном катализе многих ферментов (мульти-ферментных систем), и дирижерами при этом являются аллостерические ферменты, называемые также регуляторными ферментами:
![]()
Часто метаболические превращения организованы как циклические процессы, и они отличаются от этой схемы тем, что конечный и начальный продукты в такой цепочке представляют собой одно и то же вещество, например:
![]()
В обеих схемах Е1 означает регуляторный фермент. Продукты последовательных пре-вращений называются метаболитами. Метаболизм включает две основных составляю-щих - катаболизм и анаболизм. В катаболических превращениях происходит деграда-ция пищевых и запасных веществ до более простых молекул. Катаболизм – это основа биоэнергетики, так как превращение сложных молекул в более простые чаще всего со-провождается выигрышем в энергии. В биохимии эта энергия аккумулируется в опре-деленных веществах, главным образом в аденозинтрифосфате (АТФ) и никотинамид-адениндинуклеотиде(фосфате) в восстановленной форме (NADH или NADPH), образу-ющихся в ходе катаболических процессов. У аэробных организмов энергия окисления NADPH также может использоваться для биосинтеза АТФ. Богатые химической энер-гией вещества лежат в основе анаболических превращений, когда из простых веществ с затратой энергии получаются более сложные.
Метаболизм слагается из сотен различных ферментативных реакций, но центральные пути превращений углеводов, аминокислот, жирных кислот и биогенных фосфатов немногочисленны и, что самое главное, едины для всего живого:
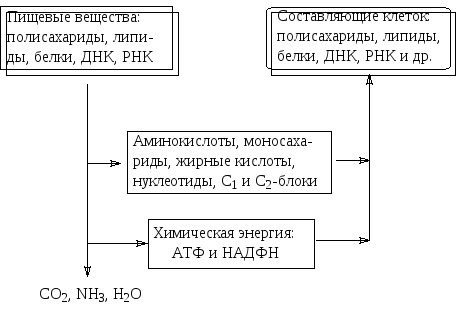
Левая нисходящая ветвь на этой схеме представлена катаболическими процессами, правая - анаболическими. Катаболические пути сходятся: из всего разнообразия вовле-ченных в них веществ образуется сравнительно немного одинаковых молекул. Так, например, все разнообразие белков при гидролизе приведет к двадцати аминокислотам, а катаболические превращения сахаров, жирных кислот и некоторых аминокислот приводят к образованию одного вещества - ацетилкофермента А, для которого принято сокращенное обозначение СоАS-COCH3 или СоАS-Ас.
Анаболические пути расходятся: небольшое число аминокислот, сахаров, жирных кислот, нуклеотидов и С1-С2-блоков являются исходными продуктами для всего разно-образия структурных элементов живой природы.
Все ферментативные процессы обратимы, но несмотря на это пути синтеза и деграда-ции биомолекул в многостадийных превращениях различаются на одной или несколь-ких стадиях. Вторичной причиной тому служат термодинамические ограничения. Так, например при полной обратимости в цепи превращений
![]()
для более или менее разумной скорости протекания реакций потребовались бы доста-точно высокие значения стационарных концентраций метаболитов, а рост концентра-ции конечного продукта привел бы и к росту концентрации исходного продукта (ана-логия с кладкой стены из кирпичей, то есть если нет подвоза кирпичей, то надо прекра-тить кладку стены, оставив запас). Более существенна необходимость раздельной регу-ляции анаболических и катаболических процессов, иначе блокировка одного из этапов катаболического превращения привела бы к остановке и соответствующего анаболи-ческого процесса. Различие может состоять во включении обходных путей, иных про-межуточных стадий, а также к появлению новых ферментов на одном или нескольких этапах обратимых превращений. Важно также, что катаболические и анаболические пути должны быть разделены по локализации, то есть разделены пространственно. Это необходимо для того, чтобы исключить холостые циклы. Так, например, в процессе катаболизма глюкозы с участием АТР образуется 1,6-дифосфоглюкоза, а при глюко-неогенезе это вещество гидролизуется (АТР при этом не образуется). При совмещении этих путей в одном месте происходило бы непроизводительное расходование АТФ – этого важнейшего участника биоэнергетических процессов. В качестве примера про-странственного разделения можно привести окислительные превращения с выигрышем энергии, которые идут в клеточных органеллах митохондриях, тогда как восстанови-тельные энергозатратные анаболические процессы образования тех же самых веществ локализованы в жидкой среде клетки – цитозоле.
Генерируемая в катаболических превращениях энергия представляет собой свободную энергию, то есть энергию, которая может совершать работу при постоянных температу-ре и давлении. Так, сжигание органических веществ сопровождается выделением теп-ловой энергии, но она может совершать работу только в условиях перепада температур.
Во всем объеме клеток температура мало различается и энергия химических превра-щений реализуется через образование особых веществ, их называют макроэргически-ми, главным из которых является аденозинтрифосфат (АТР, АТФ). Это вещество содержит две ангидридные связи, гидролиз которых сопровождается выделением около 7,3 ккал/моль (30,5 кДж/моль):
![]()
![]()
где АТР означает аденозинтрифосфат, ADP - аденозиндифосфат, AMP - адено-зинмонофосфат, а Pi и PРi это принятые в биохимии обозначения анионной формы фос-форной и пирофосфорной кислот (i – inorganic), в общем случае для фосфорной кисло-ты в клетке это смесь одно- и двухосновных анионов. Гидролиз аденозинмонофосфата на аденозин и фосфат дает только 3,4 ккал/моль (в кДж – это 14,2), а макроэргическими считаются связи, у которых G0’ превышает 30 кДж/моль. Пирофосфаты важнейшие, но не единственные макроэргические фосфаты в биохимии. Кроме них можно назвать еще смешанные ангидриды карбоновых кислот и фосфорной кислоты (около -49 кДж/моль), гуанидинофосфаты (около -43 кДж/моль) и енолфосфаты (около -62 кДж/моль)
Заложенная в АТР (АТФ) химическая энергия может совершать работу четырех основ-ных видов:
-
Метаболические превращения. При этом молекулы предшественники фосфорили-руются аденозинтрифосфатом в присутствии соответствующих ферментов с образо-ванием активных фосфатов, которые и включаются в обменные процессы.
-
АТР служит источником энергии для движения.
-
АТР поставляет энергию для переноса веществ через клеточные мембраны против градиента концентраций.
-
АТР используется в процессах, связанных с передачей наследственной (генети-ческой) информации.
Легче всего роль пирофосфатной связи демонстрируется на реакциях конденсации. Предположим, что в клетке должна пройти эндотермическая реакция
ХОН + HYXY + H2O,
для которой свободная энергия Гиббса равна 12,5 кДж/моль. С участием АТР (сопря-женная реакция) эта схема приобретает такой вид
Реакция 1: ХОН + А-R-Р-Р-Р А-R-Р-Р-О-Х + Рi
Реакция 2: A-R-P-P-O-X + HYXY + A-R-P-POH
В сумме: ХОН + АМР-Р-Р + HY АМР-РО-Х + [(Н2О) + АМР-Р + Рi]
То есть на реакцию образования XY накладывается реакция гидролиза АТР на АDP и фосфорную кислоту (Pi) с эффектом -30,5 кДж/моль. Тогда по свободной энергии полу-чаем в сумме экзотермический эффект:
12,5 – 30,5 = -18 кДж/моль.
Вторым важнейшим источником химической энергии является восстановительный потенциал, универсальным носителем которого в живой природе стали NADPH и NADH, образующиеся в результате переноса гидридиона (Н-) или двух электронов и одного протона на NADP+ и NAD+, например:
![]()
![]()
где SH2 - субстрат дегидрирования. Химически этот процесс представляет собой переход пиридиниевого фрагмента молекулы NAD+ в дигидропиридиновый:

Восстановленные формы NADH и NADPH включаются в другие окислительно-восстановительные процессы и снова превращаются в NAD+ и NADP+.
Химические свойства и редокспотенциалы NADН и NADPН почти неразличимы (‑0,32 В), но лишняя фосфатная группа в последнем делает его несовместимым с апо-ферментами для пары NAD+/NADH, что позволяет, например, разделять метаболичес-кие пути за счет участия этих двух коферментов (косубстратов).
Метаболические пути регулируются по трем механизмам:
