
1.4. Кристалізація металів
Процес переходу металу з рідкого стану в твердий називається кристалізацією. Він відбувається в два етапи. Спочатку, при зменшенні температури розплавленого металу утворюється зародки, а потім ці зародки розростаються до утворення зерен. Зародки – це перші елементарні комірки, які утворюються в розплавленому металі в центрах кристалізації. Центрами кристалізації є домішки, стінки посудини та випадково розташовані атоми у вигляді геометрично правильних фігур, ідентичних до елементарних комірок, які характерні даному металу. Оскільки атоми в розплавленому металі швидко рухаються і їх величезна кількість, то завжди є імовірність утворення таких фігур в значній кількості. Отже, в розплавленому металі є величезна кількість центрів кристалізації. При певній температурі, яка характерна для кожного металу (температура плавлення), біля центрів кристалізації утворюються зародки довільно орієнтовані у просторі. Розростаючись, вони утворюють зерна (рис. 1.5). Отже, метал складається з великої кількості зерен, тобто є полікристалічним тілом. Якби він кристалізувався з одного центра, то був би монокристалом.
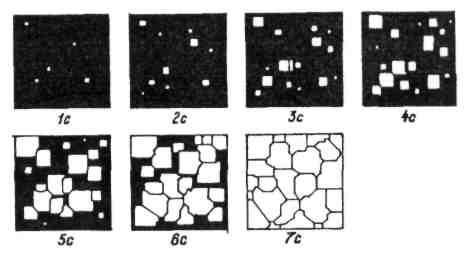
Рис. 1.5
З вище сказаного випливає, що змінюючи число центрів кристалізації можна змінити величину зерна. Наприклад, додавши в розплавлений метал порошкоподібного модифікатора можна зменшити величину зерна. Число зародків, а значить і величину зерна, можна змінити також шляхом переохолодження розплаву. Переохолодження металу – це охолодження з більшою швидкістю ніж тією, яка супроводжується рівноважними процесами. Воно характеризується степінню переохолодження. Степінь переохолодження – це різниця між теоретичною температурою кристалізації (рівноважний процес) і практичною. Чим більша степінь переохолодження, тим меншими будуть зерна в металі.
Швидкість процесу кристалізації, величина зерен, їх форма значною мірою залежить від режиму охолодження розплавленого металу і перш за все від ступеня переохолодження розплаву (рис. 1.6).
Рис. 1.6
Взаємозв’язок між швидкістю кристалізації, числом центрів кристалізації і ступенем переохолодження розплаву визначає величину зерна, а значить і властивості металу.
Перехід металу з розплавленого стану в твердий відбувається при постійній температурі. Це пояснюється тим, що утворення елементарних комірок відбувається з виділенням тепла (схована теплота кристалізації).
При подальшому охолодженні кристалічні комірки в окремих металах можуть змінюватись. Атоми розташовуються в новому порядку, який енергетично вигідніший, ніж в попередньому. Це явище називається поліморфним або алотропічним перетворенням. Наприклад, залізо має α, γ, δ перетворення. До температури 911°С буде α-залізо з ОЦК решіткою. Від 911°С до 1392°С буде γ-залізо з коміркою ГЦК, а від 1392°С і до плавлення буде δ-залізо з ОЦК коміркою.
Оскільки в зерні елементарні комірки об’єднуються в решітку, то спостерігається різна густина упаковки атомів в різних напрямках. Це приводить до анізотропії всіх його властивостей (неоднаковість властивостей в різних напрямках). Оскільки зерен в металі багато і вони розорієнтовані, це приводить до усереднення всіх властивостей, тобто метал є ізотропним.
Таким чином, метал є полікристалічним тілом. Він має велику кількість зерен, кристалічні решітки яких розорієнтовані в просторі. Атоми металу розташовуються у вузлах кристалічної решітки, яка складається з елементарних комірок, характерних для даного металу. Комірки являють собою геометрично правильну фігуру.
У реальних умовах правильне розташування атомів у решітці порушується. Це викликається різними причинами. Так, до порушень (дефектів) приводять домішки, вакансії тощо.
Усі дефекти можна розділити на три види: точкові, лінійні та поверхневі.
Точкові дефекти мають незначні розміри у трьох вимірах (x, y, z). Причин їх виникнення дві. Одна з них – це виникнення в металі вакансій (рис. 1.7, а). Відомо, що атоми коливаються біля вузлів решіток. З підвищенням температури амплітуда цих коливань збільшується. Більшість атомів кристалічної решітки мають однакову (середню) енергію і коливаються при даній температурі з однаковою амплітудою. Проте, окремі атоми можуть випадково отримати надлишок енергії від сусідніх атомів, якої достатньо, щоб атом покинув своє місце. Таким чином, утворюється вакансія. Кулонівські сили взаємного притягання стягують сусідні атоми і утворюють дефект. Найбільш часто це трапляється в поверхневих шарах металу. Утворена вакансія може швидко заповнитись атомом, який створив вакансію в іншому місці металу і т. д. Тобто вакансія може переміщуватись в глибину металу. Атом, який покинув вузол решітки, в свою чергу утворює точковий дефект, або навпаки заповнює вакансію.
Точковий дефект може створити також домішковий атом, який відрізняється від основних атомів своїми розмірами (рис. 1.7, б, в).
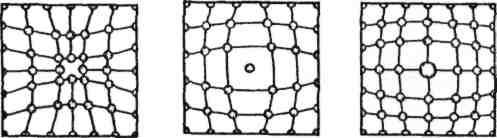
а) б) в)
Рис. 1.7
Лінійні дефекти мають незначні розміри в двох вимірах і значні в одному, тобто є протяжними. Вони можуть бути крайові (рис. 1.8, а) та гвинтові (рис. 1.8, б).
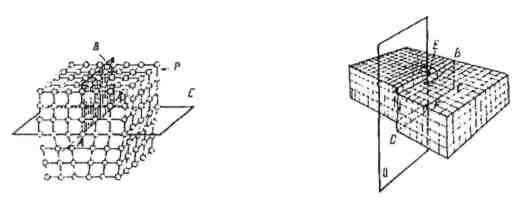
а) б)
Рис. 1.8
Крайові утворюються в результаті зсуву на одну міжатомну відстань однієї частини решітки відносно іншої вздовж якоїсь площини. Тоді число рядів атомів у верхній частині решітки на одиницю більше, ніж у нижній. Отже, у верхній частині решітки з’явиться ніби зайва атомна площина (екстраплощина). Край цієї площини створює лінійний дефект. Гвинтовий дефект утворюється в результаті кристалізації металу шарами, які заходять один під одний. При цьому відбувається закручування атомних шарів по гвинтовій лінії. Поверхневі дефекти знаходяться на границях між зернами, оскільки на границях зерен атоми розташовуються неправильно. Крім того, по границям зерен зосереджуються дислокації і вакансії, а також концентруються домішки, що ще більше порушує порядок розташування атомів.
Дефекти в кристалах суттєво впливають на властивості металів. Підрахунки показують, що ідеальні кристали мають високу теоретичну міцність (у 10...1000 разів більшу, ніж у реальних кристалах). Однак міцність змінюється в залежності від концентрації дефектів.
Таблиця 1.2. Деякі властивості металів
|
Елемент |
Номер елемента в періодичній системі |
Кристалічна решітка |
Атомний радіус, Ао |
Густина (при 20оС) г/см3 |
Температура |
Коефіцієнт розширення (при 20 оС) α·106 |
Твердість НВ | |||
|
плавлення, оС |
кипіння, оС | |||||||||
|
Be Mg Al Ti V Cr
Mn Fe Co Ni Cu Zn
Zr Nb Mo Ag Sn W
Au Hg Pb U |
4 12 13 22 23 24
25 26 27 28 29 30
40 41 42 47 50 74
79 80 82 92 |
Г12 Г12 К12 Г12, К8 К8 К8
складна К8, К12 Г12, К12 К12 К12 Г6
Г12, К8 К8 К8 К12 алмазу К4 К8
К12 Г6 К12 складна |
1,13 1,60 1,43 1,45 1,36 1,28
1,31 1,27 1,26 1,24 1,28 1,37
1,60 1,47 1,40 1,44 1,58 1,41
1,44 1,55 1,75 1,55 |
1,82 1,74 2,70 4,50 5,96 7,14
7,46 7,86 8,9 8,90 8,92 7,14
6,52 8,5 10,2 10,5 7,29 19,3
19,3 13,51 11,3 19,0 |
1284 651 660 1660 1700 1850
1244 1539 1480 1455 1083 419
1860 2450 2625 960 232 3410
1063 - 38,9 327 1133 |
2970 1110 2500 3260 3000 2470
2150 2880 3135 3080 2300 907
3580 3700 4800 1950 2430 5500
2600 357 1750 3927 |
12,2 25,7 23,1 7,14 8,3 6,2
22,1 11,5 12,5 13,5 16,5 32,5
6,23 7,2 4,9 18,9 46,6 4,3
14,2 – 28,1 23 |
140 30 20 80 260 100
200 70 50 60 35 35
100 80 150 25 5 300
19 – 4 240 | ||
Література
Гуляев А. П. Металловедение. – М.: Металлургия, 1987. – 456 с.
Лахтин Ю. М., Леонтьева В. П. Материаловедение. – М.:Машиностроение, 1990. – 528 с.
Материаловедение / Под ред. А.Г. Рохштада – М.: Металлургия, 1989. – 454 с.
Металловедение / Под ред. Б. Н. Арзамасова. – М.: Машиностроение, 1986. – 383 с.
Попович В. та ін. Технологія конструкційних матеріалів і матеріалознавство. – Львів: Світ. – 2006. – 611 с.
Питання для самостійної роботи
Чому метали є полікристалічними тілами?
Було б погано чи добре, якби метали були аморфними чи монокристалічними?
Збільшення дефектів (точкових, лінійних, поверхневих) покращує чи погіршує властивості металів?
Як змінити величину зерен у металі?
