- •Химическая кинетика
- •Основные понятия химической кинетики
- •Факторы, влияющие на скорость химических реакций.
- •Примеры
- •Закон действующих масс (к. Гульдберг, п.Вааге, 1867г.)
- •Решение:
- •Примеры решения задач:
- •Задачи с использованием закона действия масс
- •Решение
- •Решение
- •Решение
- •Задачи с использованием закона Вант-Гоффа
- •Задачи с использованием закона объёмных отношений
- •Способы смещения равновесия
- •Примеры решения задач:
Решение:
a) Поскольку в данной реакции все вещества находятся в газообразном состоянии, то данная система будет являться гомогенной и в формулу закона для прямой реакции будут входить концентрации всех компонентов:
=[N2]![]() [H2]3
[H2]3
для обратной реакции:
=[NH3]2
b) Поскольку в данной реакции вещества находятся в газообразном и кристаллическом состоянии, то данная система будет являться гетерогенной и в формулу закона для прямой реакции будут входить концентрации только газообразных веществ ([C] не учитывается, т. к. углерод находится в кристаллическом состоянии, а концентрации кристаллических веществ равны единице.):
=[О2]
для обратной реакции:
=[CO]2
3)Температура. Многочисленные опыты показывают, что при повышении температуры скорость большинства химических реакций существенно увеличивается, причем для реакций в гомогенных системах при нагревании на каждые десять градусов скорость реакции возрастает в 2—4 раза (правило Вант-Гоффа).
Это
правило связано с понятием температурного
коэффициента
скорости реакции
![]() и определяется соотношением
и определяется соотношением
![]()
При увеличении температуры от t1 до t2 изменение скорости реакции можно рассчитать по формуле:

(где
t2
и t1
- скорости реакции при температурах t2
и t1
соответственно;
![]() -
температурный коэффициент скорости
данной реакции, показывающий, во сколько
раз изменяется скорость реакции при
изменении температуры на 100
С).
-
температурный коэффициент скорости
данной реакции, показывающий, во сколько
раз изменяется скорость реакции при
изменении температуры на 100
С).
С одной стороны, увеличение температуры приводит к увеличению скорости движения молекул и, как следствие, к более частым столкновениям. Но этот фактор не вызывает увеличение скорости даже в 2а раза, т. к. не все столкновения оказываются эффективными. Реакция начнётся только в том случае, если энергия молекул превысит некоторую величину, достаточную для преодоления барьера отталкивания. В этом случае происходит сближение взаимодействующих частиц, при котором становиться возможным образование химической связи. При этом возникает активированный комплекс- единое образование из столкнувшихся молекул, находящихся в состоянии перераспределения электронной плотности. Такие молекулы называются активными, а энергия, которой должны обладать эти сталкивающиеся молекулы, чтобы их столкновение привело к химическому превращению, называют энергией активации. Отсюда следует, что при увеличении температуры увеличивается доля активных, т. е. способных к взаимодействию молекул, и скорость реакции увеличивается. Этот факт может быть доказан с помощью графика:
-
Ч


 исло
частиц с данной энергией
исло
частиц с данной энергией







Т1
 Т2
Е Т2>Т1
Т2
Е Т2>Т1
Кинетическая энергия
Правило Вант-Гоффа применимо только в узком интервале температур. Более точным является уравнение Аррениуса:
k = A ∙ e √Ea/RT
где
A - постоянная, зависящая от природы реагирующих веществ;
R - универсальная газовая постоянная [8,314 Дж/(моль ∙ К) = 0,082 л ∙ ═атм/(моль ∙ К)];
Ea - энергия активации.
Показательно, что для экзотермической реакции( идущей с выделением теплоты ) энергия активации перекрывается тепловым эффектом реакции.
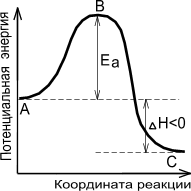
Энергетическая диаграмма химической реакции.
|
|
|
|
Экзотермическая реакция |
Эндотермическая реакция |
А - реагенты, В - активированный комплекс (переходное состояние), С - продукты.
Чем больше энергия активации Ea, тем сильнее возрастает скорость реакции при увеличении температуры.
4)Поверхность соприкосновения реагирующих веществ. Для гетерогенных систем (когда вещества находятся в разных агрегатных состояниях), чем больше поверхность соприкосновения, тем быстрее протекает реакция. Поверхность твердых веществ может быть увеличена путем их измельчения, а для растворимых веществ - путем их растворения.
5)Катализ - процесс, заключающийся в изменении скорости химических реакций в присутствии веществ, называемых катализаторами. Катализаторы - вещества, изменяющие скорость химической реакции, которые могут участвовать в реакции, входить в состав промежуточных продуктов, но не входят в состав конечных продуктов реакции и после окончания реакции остаются неизменными. Каталитические реакции - реакции, протекающие в присутствии катализаторов. Положительным называют катализ, при котором скорость реакции возрастает, отрицательным (ингибированием) - при котором она убывает. Примером положительного катализа может служить процесс окисления аммиака на платине при получении азотной кислоты. Примером отрицательного - снижение скорости коррозии при введении в жидкость, в которой эксплуатируется металл, нитрита натрия, хромата и дихромата калия. Катализаторы, замедляющие химическую реакцию, называются ингибиторами. В зависимости от того, находится катализатор в той же фазе, что и реагирующие вещества, или образует самостоятельную фазу, говорят о гомогенном или гетерогенном катализе. Примером гомогенного катализа является разложение пероксида водорода в присутствии ионов йода. Реакция протекает в две стадии:
Н2 О2 + I2 = H2 O + I2O
Н2 O2 + I2O = Н2 O + O2 + I2
При гомогенном катализе действие катализатора связано с тем, что он вступает во взаимодействие с реагирующими веществами с образованием промежуточных соединений, это приводит к снижению энергии активации. При гетерогенном катализе ускорение процесса обычно происходит на поверхности твердого тела - катализатора, поэтому активность катализатора зависит от величины и свойств его поверхности. На практике катализатор обычно наносят на твердый пористый носитель. Механизм гетерогенного катализа сложнее, чем у гомогенного.
Механизм гетерогенного катализа включает пять стадий, причем все они обратимы. 1. Диффузия реагирующих веществ к поверхности твердого вещества. 2. Физическая адсорбция на активных центрах поверхности твердого вещества реагирующих молекул и затем хемосорбция их. 3. Химическая реакция между реагирующими молекулами. 4. Десорбция продуктов с поверхности катализатора. 5. Диффузия продукта с поверхности катализатора в общий поток.
Примером гетерогенного катализа является окисление SO2 в SO3 на катализаторе V2 O5 при производстве серной кислоты (контактный метод).
Промоторы (или активаторы) - вещества, повышающие активность катализатора. При этом промоторы могут сами и не обладать каталитическими свойствами.
Каталитические яды - посторонние примеси в реакционной смеси, приводящие к частичной или полной потере активности катализатора. Так, следы мышьяка, фосфора вызывают быструю потерю катализатором V2 O5 активности (контактный метод производства H2 SO4 ).
Многие важнейшие химические производства, такие, как получение серной кислоты, аммиака, азотной кислоты, синтетического каучука, ряда полимеров и др., проводятся в присутствии катализаторов. Биохимические реакции в растительных и животных организмах ускоряются биохимическими катализаторами - ферментами.