
Oxorona_atmosfernogo_povitria / Хараев.Инженерная защита атмосферы
.pdf
Решение.
Исходная эмаль МЛ-12 состоит на 35 % из сухого остатка, а также из летучей части, содержащей 10% бутилового спирта и 90 % уайт-спирита [7]. Растворитель №649 состоит из 50% ксилола, 30% этилцеллозольва, 20% изобутилового спирта [7 , 12].
Валовый выброс ЗВ при отсутствии очистки равен их валовому выделению.
По уравнению (1.15) при окраске:
а) бутиловый спирт
Мб.сп.ок = Zкр · (1- сух · 10-2) · φкр · βок · 10-4 + 0 =
= 49 · (1 - 35 · 10-2)10 · 23 · 10-4 + 0 = 0,733 т/г;
б) уайт спирит
Му.сп.ок = Zкр · (1- сух · 10-2) · φкр · βок · 10-4 + 0 =
= 49 · (1 - 35 · 10-2)90 · 23 · 10-4 + 0 = 6,593 т/г;
в) ксилол
Мкс.ок = 0 + Zраст · φраст · βок · 10-4 = 0 + 17 · 50 · 23 10-4 = 1,955 т/г;
г) этилцеллозольв
Мэт.ок = 0 + Zраст · φраст · βок · 10-4 =0 + 17 · 30 · 23 · 10-4 = 1,173 т/г;
д) изобутиловый спирт
Миз.сп.ок = 0 + Zраст · φраст · βок · 10-4 =0 + 17 · 20 · 23 · 10-4 = 0,782 т/г;
при сушке:
а) бутиловый спирт
60
Мб.сп.суш = Zкр · (1- сух · 10-2) ·φкр · βсуш · 10-4 + 0 =
= 49 · (1 - 35 · 10-2)10 ·77 · 10-4 + 0 = 2,452 т/г;
б) уайт спирит
Му.сп.суш = Zкр · (1- сух · 10-2) · φкр · βсуш ·10-4 + 0 =
= 49 · (1 - 35 · 10-2)90 · 77 · 10-4 + 0 = 22,072 т/г;
в) ксилол
Мкс.суш = 0 + Zраст · φраст · βсуш · 10-4 = 0 + 17 · 50 · 77 · 10-4 = 6,545 т/г;
г) этилцеллозольв
Мэт.суш = 0 + Zраст · φраст · βсуш · 10-4 =0 + 17 · 30 · 77 · 10-4 = 3,927 т/г;
д) изобутиловый спирт
Миз.сп.суш = 0 + Zраст · φраст · βсуш · 10-4 =0 + 17 · 20 · 77 10-4 =
2,618 т/г. |
Примечание: · |
Проверка по материальному балансу: |
|
1) Zраст = Мкс.ок + Мкс.суш + Мэт.ок + Мэт.суш + Миз.сп.ок |
+ |
Миз.сп.суш; |
|
17 = 1,955 + 6,545 + 1,173 + 3,927 + 0,782 + 2,618; 17 = 17 => баланс по растворителю сошелся, значит решение верно.
2)Zкр · (1- сух · 10-2) = Мб.сп.ок + Мб.сп.суш + Му.сп.ок + Му.сп.суш;
49 · (1 – 0,35) = 0,733 + 2,452 + 6,593 + 22,072;
31,85 = 31,85 => баланс по летучей части исходного ЛКМ сошелся, значит решение верно.
61

Пример 2.8.
Калужский молокозавод имеет один грузовой автомобиль ГАЗ-51, место стоянки которого находится в 100 м (0,1 км) от въездных ворот и 30 м (0,03 км) от выездных ворот. Автомобиль выезжает с территории и въезжает один раз в день.
Определить валовый выброс загрязняющих веществ за 20 отработанных дней в июле.
Решение.
Удельные выделения ЗВ автомобиля с карбюраторным двигателем, грузоподъемностью от 1 до 3 т в июле (теплый период года) составляют [7,8]:
ЗВ |
СО |
СnHm |
NOx |
SO2 |
|
При прогреве |
|
|
|
|
|
Двигателя, |
8,1 |
1,6 |
0,1 |
0,016 |
|
г/мин |
|
|
|
|
|
При пробеге |
|
|
|
|
|
по |
27,6 |
4,9 |
0,6 |
0,1 |
|
территории, |
|||||
|
|
|
|
||
г/км |
|
|
|
|
|
на холостом |
|
|
|
|
|
ходу, |
8,1 |
1,6 |
0,1 |
0,016 |
|
г/мин |
|
|
|
|
По уравнению (1.19) валовое выделение ЗВ одним автомобилем при однократном выезде с территории:
МСО’= gCO пр · tпр + gCO L · L’+ gCO xx· txx = 8,1 ·4 + 27,6 · 0,1 + 8,1 · 1 = 43,26 г;
МСH’ = gCH пр · tпр + gCH L L’+ gCH xx · txx = 1,6 ·4 + 4,9 · 0,1 + 1,6 · 1 = 8,49 г;
62
МNОx’ = gNOx пр · tпр + gNOx L · L’ + gNOx xx · txx =
= 0,1 ·4 + 0,6 · 0,1 + 0,1 · 1 = 0,56 г;
МSО2’ = gSO2 пр · tпр + gSO2 L · L’ + gSO2 xx · txx =
= 0,016 ·4 + 0,1 · 0,1 + 0,016 · 1 = 0,09 г;
По уравнению (1.20) валовое выделение ЗВ одним автомобилем при однократном въезде на территорию:
МСО” = gCO L · L” + gCO xx · txx = 27,6 · 0,03 + 8,1 · 1 = 8,93г; МСH” = gCH L · L” + gCH xx · txx = 4,9 · 0,03 + 1,6 · 1 = 1,75г; МNОx” = gNOx L · L” + gNOx xx · txx = 0,6 · 0,03 + 0,1 · 1 = 0,118г;
МSО2” = gSO2 L · L” + gSO2 xx · txx = 0,1 · 0,03 + 0,016 · 1 = 0,019г.
В данном случае валовый выброс ЗВ равен валовому выделению и за весь месяц составит:
МСО = 20 · (МСО’ + МСО”) = 20 · (43,26 + 8,93) = 1043,8г/мес;
МСH = 20 · (МСH’ + МСH”) = 20 · (8,49 + 1,75) = 204,8г/мес; МNОx = 20 · (МNОx’ + МNОx”) = 20 · (0,56 + 0,118) =
13,6 г/мес;
МSО2 = 20 · (МSО2’ + МSО2”) = 20 · (0,09 + 0,019) = 2,2г/мес;
Примечание:
63
Пример 2.9
Определить годовой валовый выброс оксида углерода от 20 автобусов Икарус-250 Домодедовского автобусного парка при ежедневной работе с коэффициентом выпуска на линию равным 0,7. Расстояние от центра открытой стоянки до ворот 230 м (0,23 км).
Решение.
Удельные выделения СО автобусов большого класса с дизельными по периодам года составляют [7]:
Период года |
Теплый |
Переходной |
Холодный |
|
При |
|
|
|
|
прогреве |
4,6 |
8,01 |
8,9 |
|
двигателя, |
||||
|
|
|
||
г/мин |
|
|
|
|
При пробеге |
|
|
|
|
по |
5,1 |
5,58 |
6,2 |
|
территории, |
||||
|
|
|
||
г/км |
|
|
|
|
На холостом |
|
4,6 |
|
|
ходу, г/мин |
|
|
||
|
|
|
Длительность периодов года для Москвы и Московской области [15]: теплый – 6 месяцев (183 дня); переходный – 3 месяца (92 дня); холодный – 3 месяца (90 дней).
По уравнению (1.19) для одного автобуса валовое выделение за день при выезде составляет:
64
в теплый период
МТСО’ = gTCO пр · tпр + gTCO L · L’ + gCO xx 0,23 + 4,6 · 1 = 24,123 г/день;
в переходный период
МПСО’ = gПCO пр · tпр + gПCO L · L’ + gCO xx 0,23 + 4,6 ·1 = 53,94 г/день;
в холодный период МХСО’ = gХCO пр · tпр + gХCO L · L’ + gCO xx 0,23 + 4,6 · 1 = 184,03 г/день.
·txx = 4,6 · 4 + 5,1 ·
·txx = 8,1 · 6 + 5,58 ·
·txx = 8,9 · 20 + 6,2 ·
По уравнению (1.20) для одного автобуса валовое выделение за день при возврате составляет:
в теплый период
МТСО” = gTCO L · L” + gCO xx · txx = 5,1 · 0,23 + 4,6 · 1 = 6,831
г/день;
в переходный период
МПСО” = gПCO L · L” + gCO xx · txx = 5,58 · 0,23 + 4,6 · 1 = 5,883
г/день;
в холодный период
МХСО” = gХCO L · L” + gCO xx · txx = 6,2 · 0,23 + 4,6 · 1 = 6,026
г/день.
65

По уравнению (1.21) в данном случае валовый выброс равен валовому выделению и по периодам года составляет:
в теплый период
МТСО = α · (МТСО’ + МТСО”) · N DT · 10-6 =
= 0,7 · (24,123 + 6,831) · 20 · 183 · 10-6 = 0,0793 т/г;
в переходный период
МПСО = α · (МПСО’ + МПСО”) · N DП 10-6 =
= 0,7 · (53,94 + 5,883) · 20 · 92 · 10-6 = 0,0771 т/г;
в холодный период
МХСО = α · (МХСО’ + МХСО”) · N DХ · 10-6 =
= 0,7 · (184,03 + 6,026) · 20 · 90 · 10-6 = 0,2395 т/г.
По уравнению (1.22) определяем общий (годовой) валовый выброс оксида углерода
МΣсо = МТсо + МПсо + МХсо = 0,0793 + 0,0771 + 0,2395 = 0,3959 т/г.
Пример 2.10
Архангельский таксопарк выпускает на линию ежедневно 68 легковых автомобилей из 95 имеющихся. Расстояние от ворот до центра крытой стоянки 30 м. Время разъезда 45 мин.
Определить валовый и максимально разовый выбросы в атмосферу оксидов азота общей вытяжной вентиляционной системой крытой стоянки.
Решение.
Удельные выделения NOx легковых автомобилей, использующих в качестве топлива бензин, при хранении в помещении принимаются как для теплого периода и
66
составляют [7]: при прогреве двигателя – 0,05 г/мин; при пробеге по территории – 0,4 г/км; на холостом ходу – 0,05 г/мин.
По уравнению (1.19) валовое выделение для одного легкового автомобиля за день при въезде составляет:
МТNOx’ = gTNOx пр · tпр + gTNOx L L’ + gNOx xx · txx =
= 0,05 · 0,5 + 0,4 · 0,03 + 0,05 · 1 = 0,087 г/день.
По уравнению (1.20) валовое выделение для одного легкового автомобиля за день при выезде составляет:
МТNOx” = gTNOx L · L” + gNOx xx · txx =0,4 · 0,03 + 0,05 · 1 = 0,062 г/день.
По уравнению (1.21) валовый выброс равный в данном случае, валовому выделению за год при коэффициенте выпуска α=68 / 95 = 0,716
МТNOx = α(МТNOx’ + МТNOx”) · N · D · 10-6 =
= 0,716 · (0,087 + 0,062) · 95 · 365 ·10-6 = 0,0037 т/г.
По уравнению (1.23) максимально разовый выброс NOx, в данном случае также равный максимально разовому выделению:
0,716 · 95) / (60 · 45) = 0,0022 г/с.
Пример 2.11
В котельной подмосковного поселка N установлено два котла, работающих на подмосковном угле марки Б2Р. Определить объем дымовых газов, а также максимально
67
разовые выбросы золы и оксидов серы, углерода, азота при следующих показателях.
Технические характеристики котла |
|
|
||||||||
Расчетный расход топлива на один котел |
|
500г/с. |
|
|
||||||
Температура отходящих газов в устье |
|
150оС |
|
|
||||||
трубы |
|
|
|
|
|
|
|
|
|
|
Коэффициент избытка воздуха перед |
|
1,75 |
|
|
||||||
дымовой трубой, ζух |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
Потери теплоты с уносом от |
|
1,0% |
|
|
||||||
механической неполноты сгорания |
|
|
|
|
|
|
||||
топлива |
|
|
|
|
|
|
|
|
|
|
Потеря тепла от неполноты |
|
Механи- |
|
4,0% |
|
|
||||
сгорания топлива |
|
ческой |
|
|
|
|
|
|
||
|
|
Химичес |
|
1,0% |
|
|
||||
|
|
кой |
|
|
|
|
|
|
||
Доля твердых частиц, задерживаемых |
|
0,85 |
|
|
||||||
золоуловителем |
|
|
|
|
|
|
|
|
|
|
Доля оксидов серы, связанных летучей |
|
0,1 |
|
|
||||||
золой в котле |
|
|
|
|
|
|
|
|
|
|
Доля оксидов серы, улавливаемых в |
|
0 |
|
|
||||||
золоуловителе котла попутно с |
|
|
|
|
|
|
||||
улавливанием твердых частиц. |
|
|
|
|
|
|
||||
Характеристики топлива |
|
|
||||||||
Состав угля, %: |
|
|
|
|
|
W – 32,8 |
||||
A – 28,8 |
S – 4,1 |
O – 5,0 |
|
|
||||||
H – 3,6 |
N – 1,0 |
C – 24,7 |
|
|
||||||
Низшая теплота сгорания топлива, МДж/кг – 11,48 |
||||||||||
Коэффициенты, характеризующие: |
|
|
||||||||
Долю потерь теплоты, обусловленную |
|
|
|
R |
|
|
1 |
|
||
|
|
|
|
|||||||
содержанием СО в продуктах сгорания |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|||
Влияние состава топлива на выход |
|
|
|
β1 |
|
|
0,9 |
|
||
NOx |
|
|
|
|
|
|
|
|
|
|
68 |
|
|
|
|
|
|
|
|
|
|
Конструкцию горелок |
|
|
|
|
β2 |
|
|
1 |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
||||
Вид шлакоудаления |
β3 |
1 |
Эффективность воздействия |
ε1 |
|
рециркулирующих газов в |
|
1 |
зависимости от условий их подачи в |
|
|
|
|
|
топку |
|
|
Снижение выбросов NOx при |
ε2 |
1 |
двухступенчатом сжигании |
|
|
|
|
|
Степень рециркуляции дымовых газов |
R |
0 |
Выход оксидов азота, кг/т условного |
Ψ |
5,9 |
топлива |
|
|
|
|
Решение.
По уравнению (1.37) теоретическое количество воздуха, необходимого для горения топлива заданного состава:
V0 = 0,0889 · (С + 0,375 · S) + 0,265 · Н - 0,0333 · О =
0,0889 · (24,7 + 0,375 · 4,1) + 0,265 · 3,6 – 0,0333 · 5,0 = 3,12 м3/кг.
По уравнениям (1.39 … 1.42) теоретический объем равен продуктов сгорания топлива заданного состава:
V*Σ = V*RO2 + V*N + V*H2 O = {0,0186 · (C + 0,375 · S)}+{0,79 ·V0 + 0.008 · N}+{0,111 · H + 0,0124 · W + 0,0161 ·
V0} = 0,0186 · (24,7 + 0,375 · 4,1) + 0,79 · 3,12 + 0,008 · 1,0 +
0,111 · 3,6 + 0,0124 · 32,8 + 0,0161 · 3,12 = 3,8173695 ≈ 3,82
м3/кг.
По уравнению (1.46) объем дымовых газов, выбрасываемых в атмосферу 2 котлами:
Vатм = 2 · {B · 10-3·[V*Σ+(ζух-1·V0] · [Tух+273]}:273= =2·{500·10-3·[3,82+(1,75-
1)·3,12]·[150+273]}:273=9,5446153 ≈ 9,545 м3/с.
По уравнению (1.26) максимально разовый выброс
золы
69
Gтв=Σ 0,01·Вi · [(αун · А+qун · (Qн : 32,7)]·(1-ηоч i) = 2·0,01 · 500 · [(0,85٠·28,8+4,0·(11,48:32,7)]· (1-0,85) = 38,83 г/с.

По уравнению (1.27) максимально разовый выброс
SO2
GSox =Σ 0,02·Bi··S·1-η’SOx i)·(1-η”SOx i)=20,02·500·4,1·(1-0,1)·(1- 0)=73,8 г/с.
По формулам (1.28,1.29) максимально разовый выброс оксида углерода:
GCO= Σ 0,001 · {(qхим · R · Qт) : 1,013} · Вi · ( 1 - qмех I : 100) = 2 · 0,001 · {(1,0·1·11,48):1,013}·500·(1-4,0:100)=10,8792 ≈ 11г/с.
По формуле (1.32) максимально разовый выброс оксидов азота:
GNOx= Σ 0,34 ·10-4 · Ψ · Bi · QH · (1-qмех:100)·β1 · (1-ε1i · ri)·β2i·β3i·ε2=
=·0,34·10-·5,9·500·11,48·(1-4,0:100)·0,9·(1- 1·0)·1·1·1=1,9897≈2 г/с.
Пример 2.19.
Котельная автокомбината оборудована котлом, работающим на природном газе Бухарского месторождения. Определить объем дымовых газов, а также максимально разовые выбросы оксидов углерода.
Технические характеристики котла |
|
|
|
|
|
|||
Расчетный расход топлива на один котел |
|
- |
|
0,2 |
||||
|
|
|||||||
|
|
|
|
|
|
|
|
м3/с |
Температура отходящих газов |
|
|
|
|
- |
|
|
1800С |
Коэффициент избытка воздуха, ζух |
|
- |
|
1,7 |
||||
Потеря тепла от неполноты |
механической |
|
- |
|
0,5% |
|||
сгорания топлива |
химической |
|
- |
|
0,5% |
|||
70 |
|
|
|
|
|
|
|
|
Коэффициенты, характеризующие: |
|
|
|
|
|
|||
Долю потерь теплоты, обусловленную |
|
|
|
R |
|
0,5 |
||
|
|
|
||||||
содержанием СО в продуктах сгорания |
|
|
|
|||
Влияние состава топлива на выход NOx |
|
β1 |
0,9 |
|||
Конструкцию горелок |
|
|
β2 |
1 |
||
Вид шлакоудаления |
|
|
β3 |
1 |
||
Эффективность воздействия рециркулирующих |
|
|
1 |
|||
газов в зависимости от условий их подачи в |
|
ε1 |
||||
топку |
|
|
|
|
|
|
Степень рециркуляции дымовых газов |
|
ε2 |
0 |
|||
Выход оксидов азота, кг/т условного топлива |
|
Ψ |
2,35 |
|||
|
|
Характеристики топлива |
|
|
|
|
Состав газа, %: |
диоксид углерода (СО2) |
- |
0,4; |
|
||
азот (N2) |
- |
0,9; |
пропан (С3Н8) |
- |
0,4; |
|
метан(СН4) - |
94,9; |
бутан(С4Н10) - 0,1; |
|
|
|
|
этан(С2Н6) |
- |
3,2; |
пентан(С5Н12)- 0,1. |
|
|
|
Низшая теплота сгорания топлива, МДж/кг– |
27,63 |
|
|
Влагосодержание газообразного топлива, |
|
|
|
отнесенное к 1 м3 сухого газа (dr), г/м3 |
|
– |
10,0 |
Плотность газа (ρ), кг/м3 |
– |
0,758 |
|
Решение.
По уравнению (1.38) теоретическое количество воздуха, необходимого для горения топлива заданного состава:
V0=0,0476·{0,5·СО+0,5·Н+1,5·Н2S+Σ(m+0.25·n)·CmHn- O}=0,0476·{0,5·0+ +0,5·0+1,5·0+[(1+0,25·4)·94.9+(2+0.25·6)·3.2+(3·0.2·8)·0.4+(4 +0.25·10)·0.1+(5+0.25·12)·0.1]-0}=9,73182 м3/м3.
По уравнениям (1.39,1.43…1.45) теоретический объем продуктов сгорания топлива заданного состава:
71
V*Σ=V*RO2+V*N+V*H2O= 0,01·[Σm·CmHn+CO2+CO+H2O]+0,79·V0+0,01·N+0,01·[Σ0,5·n·
CmHn+H2S+
+H+0,214·0,124·dr+1,61·V0]=0,01·[(1·94,9+2·3,2+3·0,4+4·0,1)+ 0,4+0+0]+0,79·9,732+0,01·0,9+0,01·[(0,5·4·94,9+0,5·6·3,2+0,5·
8·0,4+0,5·10·0,1+0,5·12·0,1+0+0+0,124·10+1,61·9,732]=10,925 4 м3/м3.
По уравнению (1.46) объем дымовых газов, выбрасываемых в атмосферу:
Vатм=B·10-3·[V*Σ+(ζух-1)·V0] · [Tух+273]:273=0,2·103·10-3· ·[10,9254+(1,7-1)·9,7381]·[180+273]:273=5,8865684≈5,89м3/с.
По формулам (1.28,1.29) с учетом того, что в данном случае Вi = 0,2[м3/с]·ρ[кг/м3] = 0,2 0,758 =0,1516 кг/с = 0,1516 · 103г/с, максимально разовый выброс оксида углерода:
GCO=Σ0,001·{(qхим·R·Qт):1,013}·Bi·(1-qмех i:100)= =0,001·{(0,5·0,5·27,63):1,013}·0,1516·103·(1- 0,5:100)=1,0286г/с.
По формуле (1.32) максимально разовый выброс оксидов азота:
GNOx=Σ0,34·10-4·Ψ·Bi·QH·(1-qмех:100)·β1·(1- ε1·ri)·β2i·β3i·ε2=0,34·10-4·2,35
·0,1516·103·27,63·(1-0,5:100)·0,9·(1-1·0)·1·1·1=0,3г/с.
Пример 2.13
На участке оперативной полиграфии в общем зале выделяются 0,0014 т в год бумажной пыли. Определить валовый выброс пыли в атмосферу системой общеобменной вентиляции участка и количество осевшей пыли.
Решение.
По уравнению (1.49) валовый выброс бумажной пыли общеобменной вентиляцией с учетом оседания в
72
помещении и на стенах воздуховодов составляет:
Матм=Мвыд·(1-χос/102)·(1-χ”нл/102)=0,0014·(1-50:100)·(1- 3:100)=0,000679 т/г.
Также оседает: в помещении М1=Мвыд·χос/102=0,0014·50:100=0,0007т/г;
на внутренних стенках воздуховодов
М2=Мвыд(1-χос/102)·χ”нл/102=0,0014·(1- 50:100)٠3:100=0,000021 т/г.
Пример 2.14
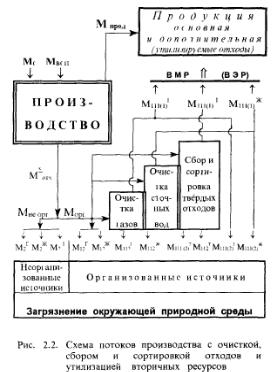
На основе анализа уравнения материального баланса некоторого производства составить схему и аналитическое выражение для определения массы загрязняющих веществ(газопылевых - Г, жидких - Ж и твердых – Т отходов производства), поступающих в окружающую среду, если суммарное количество образовавшихся отходов МΣотх, количество сырьевых и вспомогательных материальных ресурсов, вводимых в технологический процесс, Мс и МВМР соответственно и количество вещества, перешедшие в готовую продукцию, Мпрод.
Решение.
Составим схему материальных потоков производства (не вскрывая его структуры – принцип “черного ящика”), включая очистные сооружения, сбор и сортировку твердых отходов, а также потоки ненаправляемые в окружающую среду (рис. 2.2).
Всего образовалось отходов МΣотх, в том числе газопылевых – Мготх, жидких (сточных вод) – МЖотх,
твердых – Мтотх.
Отходы поступают в окружающую среду через
организованные источники Морг = {М1г,М1ж,М1т} и неорганизованные – источники потерь вещества,
участвующего в технологическом процессе:
73
Мне орг={М2г, М2ж,М2т }.
Организованные отходы подаются на очистные сооружения (М11г и М11ж) или на сбор и сортировку (М11т).
Часть отходов отводится в окружающую среду без очистки
(М12г и М12ж).
Уловлено на очистных (или сортировочных
сооружениях) Мулов={М111г, М111ж, М111т }.
Не уловлено на очистных сооружениях Мне
улов={М112г, М112ж, М112т }.
Уловленные отходы, утилизируемые в качестве вторичных материальных и энергетических ресурсов (ВМР, ВЭР),
74
Мутил={М111(1)г, М111(1)ж, М111(1)т }.
Уловленные, но не утилизированные отходы, вывозимые на свалки и полигоны:
Мне утил={М111(2)г, М111(2)ж, М111(2)т }.
Таким образом, загрязнение окружающей природной среды складывается из факторов загрязнения атмосферы
газопылевыми выбросами:
МАотх=М2г+М12г+М112г+М111(2)г;
загрязнения гидросферы сточными водами
МГотх=М2ж+М12ж+М112ж+М111(2)ж;
загрязнения литосферы твердыми отходами
МЛотх=М2т+М12т+М112т+М111(2)т.
Суммарное загрязнение окружающей среды при наличии i-веществ, поступающих из j-источников,
|
Σ |
|
i |
j |
|
|
i |
j |
|
|
i |
j |
|
|
М |
|
= |
∑ ∑ М А |
+ |
∑ ∑ М Г |
+ |
∑ ∑ М Л |
. |
||||||
|
отх |
|
1 |
1 |
отх.ij |
|
1 |
1 |
отх.ij |
|
1 |
1 |
отх.ij |
|
75
76

КОНТРОЛЬНЫЕ ЗАДАНИЯ |
С+Н2О+СО+Н2 (основная) |
|
|
|
|
|
|||||||
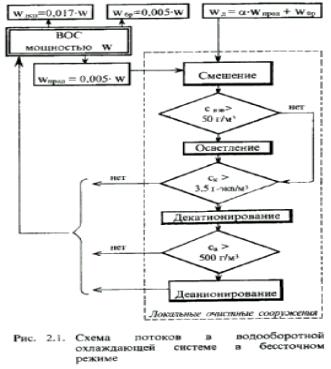
Контрольные задания по балансовым расчетам |
СО+Н2О+СО2+Н2 (побочная). |
|
|
водооборотной |
|||||||||
1. Составить материальный баланс печи (в кг/ч) для |
7. |
Рассчитать |
материальный баланс |
||||||||||
сжигания серы (S+O2=SO2) производительностью 60 тонн в сутки. |
охлаждающей системы производительностью 108 тыс. м3/ч в |
||||||||||||
Степень окисления серы 0,95 (остальная сера возгоняется и сгорает |
соответствии с условиями примера 2,25 . Состав оборотной воды |
||||||||||||
вне печи). Коэффициент избытка воздуха α=1,5. |
Свзв=50 г/м3; Скат=3,5 г-экв/м3; Сан=500 г/м3. Состав подпиточной |
||||||||||||
2. Составить материальный баланс производства криолита |
воды Свзв=20 г/м3; |
Скат=4 |
г-экв/м3; |
Сан=550 г/м3. Коэффициент |
|||||||||
(на 1 т), если процесс описывается суммарным уравнением: |
α=0,03. |
|
|
|
|
|
|
|
|
|
|
|
|
2Аl(OH)3+12HF+3Na2CO3=2Na3AlF6+3CO2+9H2O. |
8. Какие количества 62%- и 92%-ной серной кислоты |
||||||||||||
Плавиковая кислота вводится в процесс в виде 15%-ного |
нужно смешать, чтобы получить 25 кг 73%-ной Н2SO4. |
А, В и С, |
|||||||||||
раствора HF в воде. Сода берется с 4%-ной недостачей от |
9. |
Определить |
количества водных растворов |
||||||||||
стехиометрии (для обеспечения необходимой остаточной |
необходимых для получения 6,6 кг смеси, содержащей 20% |
||||||||||||
кислотности). |
этилового спирта, 37% метилового спирта и 43% воды, если |
||||||||||||
3. Определить расход технического карбида кальция, |
исходные растворы имеют следующий состав: А – 35% С2Н5ОН, |
||||||||||||
содержащего 85% СаС2 для получения 1000 л ацетилена, если |
20% СН3ОН, В – 10% С2Н5ОН, 60% СН3ОН, С – 20% С2Н5ОН и |
||||||||||||
степень разложения СаС2 составляет 0,92. Уравнение реакции |
15% СН3ОН. |
|
|
|
|
|
|
|
|
|
|
||
СаС2+Н2О=СаО+С2Н2. |
10. Рассчитать расход товарной извести, содержащей 50% |
||||||||||||
4. Определить расходный коэффициент для технического |
активной окиси кальция, для нейтрализации сточных вод, |
||||||||||||
карбида кальция в производстве ацетилена (на 1000 кг ацетилена). |
содержащих 2 г/дм3 серной кислоты и 11 г/дм3 железа. |
|
|
||||||||||
Содержание СаС2 в техническом продукте 83%, а степень |
11. На основании данных табл. 9 определить расход |
||||||||||||
использования СаС2 в производстве 0,88. Уравнение реакции в |
известняка для нейтрализации 2500 м3 сточных вод, содержащих |
||||||||||||
предыдущем задании. |
380 г/дм3 фосфорной кислоты. |
|
|
|
Таблица 9. |
||||||||
5. Рассчитать расход сульфата натрия, содержащего 95% |
|
|
|
|
|
|
|
|
|
|
|
||
Na2SO4 и электролитического водорода с содержанием 97% (по |
Количество щелочного реагента, необходимого для |
||||||||||||
массе) Н2 на 1 т технического сульфида натрия (96% Na2S). |
нейтрализации кислот, содержащихся в сточных водах |
|
|
||||||||||
Уравнение реакции: |
Щелочной |
|
Количество реагента, кг/кг кислоты |
|
|
||||||||
Na2SO4+4H2=Na2S+4H2O. |
реагент |
|
Сер- |
Со- |
|
Азот- |
|
Фосфор- |
|
Ук- |
Пла- |
|
|
На побочные реакции расходуется 2% сульфата натрия и |
|
|
ной |
ля- |
|
ной |
|
ной |
|
сус- |
ви- |
|
|
технического водорода от теоретически необходимого для |
|
|
Н2S |
ной |
|
НNO3 |
|
Н3РO4 |
|
ной |
ко- |
|
|
получения 1 т технического продукта. |
|
|
O4 |
НCl |
|
|
|
|
|
СН3 |
вой |
|
|
6. При газификации кокса (содержащего 96,5% С и 3,5% |
|
|
|
|
|
|
|
|
|
|
СО |
HF |
|
Н2О по массе) с водяным паром, полученный водяной газ содержит |
|
|
|
|
|
|
|
|
|
|
ОН |
|
|
6% СО2 (по объему). Рассчитать состав полученного газа и |
|
|
|
|
|
|
|
|
|
|
|
|
|
составить таблицу материального баланса процесса газификации на |
|
|
|
|
|
|
|
|
|
|
|
|
|
1 т кокса. Уравнения реакций: |
|
|
|
|
|
|
|
|
|
|
|
|
|
77 |
|
|
|
|
|
|
78 |
|
|
|
|
|
|
