
- •Основные термодинамические свойства идеальных газов
- •Политропный процесс
- •Второй закон термодинамики
- •Обратимые и необратимые процессы
- •Круговые термодинамические процессы
- •Термический и холодильный коэффициент циклов.
- •Цикл Карно
- •Обратный цикл Карно
- •Математическое выражение второго закона термодинамики.
- •Энтропия
- •Изменение энтропии в обратимых и необратимых процессах.
- •Изменение энтропии идеального газа.
- •Закон возрастания энтропии. Физический смысл энтропии.
- •Газовые процессы в ts− диаграмме.
- •Изотермический процесс.
- •Адиабатный процесс
- •Среднеинтегральная температура
- •Обобщенный цикл Карно
- •Термодинамическая шкала температур
Газовые процессы в ts− диаграмме.
-
Изотермический процесс.
При изотермическом процессе T=const. Поэтому TS− диаграмме он изображается прямой линией, параллельной оси абсцисс.

С учетом того, что dT=0, зависимости изменения энтропии идеального газа в изотермическом процессе примут вид
 (1)
(1)
(уходит
слагаемое
 в правой части)
в правой части)
 (2)
(2)
|
Выражение для энтропии идеального газа
|
Процесс 1-2 – это процесс, в котором энтропия увеличивается, а следовательно, к газу подводится теплота и газ совершает работу расширения, эквивалентную этой теплоте.
Процесс2-1− это процесс сжатия, в котором теплота, эквивалентная работе сжатия, отводится от газа и энтропия уменьшается
Площадь фигуры S112 S2 соответствует количеству теплоты q, сообщаемому газу, и одновременно работе l (изотермический процесс)
-
Адиабатный процесс
В адиабатном процессе q=0 и dq=0, а следовательно dS=0.

Следовательно, в адиабатном процессе S=const и в TS − диаграмме адиабатный процесс изображается прямой линией, параллельной оси T.
Поскольку в адиабатном процессе S=const,то адиабатные обратимые процессы называют также изоэнтропными.
При адиабатном сжатии температура рабочего тела повышается, а при расширении понижается. Поэтому процесс1-2 – это процесс сжатия, а процесс 2-1 – это расширение.

Из уравнения
 (3)
(3)
При
k=const
получим
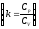
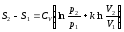
или
 (*)
(*)
Для обратимого адиабатного процесса S1=S2=const, тогда из (*)
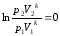
Откуда,

− уравнение адиабаты в координатах p и V.
-
Изохорный процесс
Для изохорного процесса V=const, dV=0.
При постоянной теплоемкости (из ур. (1))
 − вид
на TS
–
диаграмме
− вид
на TS
–
диаграмме
Подкасательная к кривой процесса в любой её точке определяет значение истинной теплоёмкости CV.
Подкасательная будет положительной только в том случае, если кривая будет обращена выпуклостью вниз.
Площадь под кривой процесса 1-2 на TS – диаграмме дает в масштабе количество подведенной (или отведенной в процессе 2-1) теплоты q, равное изменению внутренней энергии U2-U1.

-
Изобарный процесс
В изобарном процессе давление постоянное p=const
В этом случае
 из
(2)
из
(2)
Следовательно, при p=const как и при V=const изобара является логарифмической кривой, поднимается следа направо и обращена выпуклостью вниз.

Подкасательная к кривой 1-2 в любой её точке дает значения истинной теплоёмкости Cp.
Площадь под кривой дает кол-во теплоты q, которая сообщается газу при p=const, равное изменению энтальпии i2-i1.
-
Политропный процесс
В
политропном процессе .Теплоёмкость
в этом процессе
.Теплоёмкость
в этом процессе

Тогда,

Отсюда, для конечного изменения состояния газа

Политропный процесс на TS – диаграмме изображается кривой, расположение которой зависит от показателя n.
-
Круговой процесс. Цикл Карно.
Изобразим в TS – диаграмме произвольный обратимый цикл 1a2b1.

В процессе 1a2 рабочее тело получает кол-во теплоты q1, численно равное площади под кривой 1a2, а в процессе 2-b-1 отдает кол-во теплоты q2, численно равное площади под кривой 2-b-1.
Часть теплоты

переходит в работу цикла l (∆u=0 в цикле).
Работа цикла положительна, если цикл проходит по часовой стрелке и отрицательна, если против часовой стрелки (направление цикла в pV и TS − диаграммах одинакова).
Термический к.п.д. кругового процесса

Изменение энтропии в любом цикле равно нулю.
Цикл Карно состоит из двух изотерм и двух адиабат. В TS – диаграмме он будет изображаться в виде прямоугольника (горизонтальные линии – изотермы, вертикальные – адиабаты)
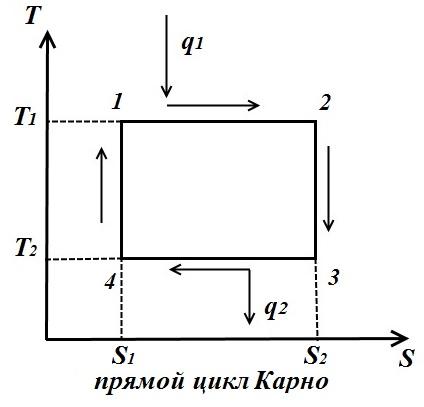
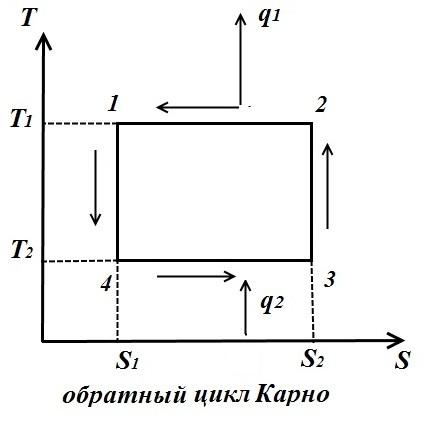
Количество теплоты, подведенное к рабочему телу, числено равно площади прямоугольника 12S2S1:

Количество теплоты, отведенное к холодильнику, соответствует площади прямоугольника 34S1S2:
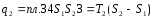
Теплота, эквивалентная работе цикла, равная площади цикла

Термический к.п.д. цикла

Для обратного цикла (рис. справа)

Холодильный коэффициент обратного цикла


 через
T,V
(1)
через
T,V
(1) Tp
(2)
Tp
(2) pV
(3)
pV
(3)