
- •Предисловие
- •Химическая термодинамика, как теоретическая основа биоэнергетики Предмет, методы и основные понятия химической термодинамики
- •Термодинамические системы: изолированные, закрытые, открытые, гомогенные, гетерогенные
- •Термодинамические параметры
- •Внутренняя энергия системы
- •Форма обмена энергии с окружающей средой
- •Первое начало термодинамики. Тепловые эффекты химических реакций
- •1. В изолированной системе сумма всех видов энергии есть величина постоянная.
- •Изобарный и изохорный процессы. Энтальпия. Тепловые эффекты химических реакций
- •Термохимия. Закон Гесса
- •Влияние температуры и давления на тепловой эффект реакции
- •Использование закона Гесса в биохимических исследованиях
- •Энтропия. Второй закон термодинамики Энтропия
- •Второе начало термодинамики. Свободная энергия Гиббса
- •Принцип энергетического сопряжения
- •Химическое равновесие Обратимые и необратимые реакции. Константа равновесия
- •Смещение химического равновесия. Принцип Ле-Шателье
- •Учение о растворах Растворы
- •Физические свойства н2о и строение ее молекул
- •Механизм образования растворов
- •Растворимость веществ. Факторы, влияющие на растворимость
- •Влияние природы веществ на растворимость
- •Влияние давления на растворимость веществ
- •Влияние температуры на растворимость веществ
- •Влияние электролитов на растворимость веществ
- •Взаимная растворимость жидкостей
- •Способы выражения состава растворов
- •Термодинамические аспекты процесса растворения. Идеальные растворы
- •Коллигативные свойства разбавленных растворов
- •Диффузия и осмос в растворах
- •Роль осмоса в биологических процессах
- •Давление насыщенного пара растворителя над раствором. Закон Рауля
- •Следствия из закона Рауля
- •1) Растворы кипят при более высокой температуре, чем чистый растворитель;
- •2) Растворы замерзают при более низкой температуре, чем чистый растворитель.
- •Применение методов криоскопии и эбуллиоскопии
- •Коллигативные свойства растворов электролитов. Изотонический коэффициент Вант-Гоффа
- •Электролитическая диссоциация Электролиты и неэлектролиты. Теория электролитической диссоциации
- •Общая характеристика электролитов
- •Слабые электролиты
- •Сильные электролиты
- •Диссоциация воды. Водородный показатель
- •Теория кислот и оснований. Буферные растворы Теория кислот и оснований
- •Буферные растворы Определение буферных систем и их классификация
- •Механизм действия буферных систем
- •Вычисление рН и рОн буферных систем. Уравнение Гендерсона-Гассельбаха
- •Буферная емкость
- •Буферные системы человеческого организма
- •Нарушения кислотно-оснóвного равновесия крови. Ацидоз. Алкалоз
- •Химическая кинетика и катализ Кинетика химических реакций
- •Понятие о скорости химической реакции. Закон действующих масс
- •Кинетическая классификация химических реакций. Понятие о молекулярности и порядке химической реакции Порядок и молекулярность простых химических реакций
- •Понятие о сложных химических реакциях
- •Классификация сложных реакций
- •Измерение скорости химической реакции
- •Влияние температуры на скорость химической реакции
- •Катализ Общие положения и закономерности катализа
- •Механизм гомогенного и гетерогенного катализа
- •Особенности каталитической активности ферментов
- •2. Другим важным отличием ферментов от катализаторов небелковой природы является их высокая специфичность, т.Е. Избирательность действия.
- •Физическая химия дисперсных систем Определение дисперсных систем
- •Классификация дисперсных систем и их общая характеристика
- •Классификация дисперсных систем по агрегатному состоянию вещества дисперсной фазы и дисперсионной среды
- •Классификация по взаимодействию между частицами дисперсной фазы или степени структурированности системы
- •Классификация по характеру взаимодействия дисперсной фазы с дисперсионной средой
- •Методы получения дисперсных систем
- •Диспергирование жидкостей
- •Диспергирование газов
- •Конденсационные методы
- •Методы физической конденсации
- •Методы химической конденсации
- •Очистка золей
- •Компенсационный диализ и вивидиализ
- •Молекулярно-кинетические свойства золей
- •Броуновское движение
- •Диффузия
- •Седиментация в золях
- •Осмотическое давление в золях
- •Оптические свойства золей
- •Рассеяние света (опалесценция)
- •Оптические методы исследования коллоидных систем Ультрамикроскоп
- •Механизм образования и строение коллоидной частицы – мицеллы
- •1. Получение золя берлинской лазури:
- •2. Получение с помощью гидролиза FeCl3 золя гидроксида железа (III).
- •3. Получениезоля As2s3:
- •Электрокинетические свойства золей
- •Устойчивость гидрофобных коллоидных систем. Коагуляция золей Виды устойчивости золей
- •Теория коагуляции Дерягина-Ландау-Фервея-Овербека
- •Влияние электролитов на устойчивость золей. Порог коагуляции. Правило Шульца-Гарди
- •Чередование зон коагуляции
- •Коагуляции золей смесями электролитов
- •Скорость коагуляции
- •Коллоидная защита
- •Роль процессов коагуляции в промышленности, медицине, биологии
- •Растворы высокомолекулярных соединений
- •1) Своеобразное тепловое движение частиц растворенного вещества, схожее с броуновским движением мицелл в золях;
- •Общая характеристика высокомолекулярных соединений
- •Классификация полимеров
- •Набухание и растворение вмс
- •Термодинамические аспекты процесса набухания
- •Давление набухания
- •Свойства растворов высокомолекулярных соединений
- •Осмотическое давление растворов вмс
- •Онкотическое давление крови
- •Вязкость растворов полимеров
- •Свободная и связанная вода в растворах
- •Полиэлектролиты
- •Факторы, влияющие на устойчивость растворов полимеров. Высаливание
- •Электрохимия растворы электролитов как проводники второго рода. Электропроводность растворов электролитов
- •Эквивалентная электропроводность растворов
- •Практическое применение электропроводности
- •Равновесные электродные процессы
- •Металлический электрод
- •Измерение электродных потенциалов
- •Окислительно-восстановительные электроды
- •1. Переход окисленной формы в восстановленную и наоборот заключается только в обмене между ними электронами:
- •Диффузионный и мембранный потенциалы
- •Химические источники электрического тока. Гальванические элементы
- •Потенциометрия
- •Содержание
Применение методов криоскопии и эбуллиоскопии
Определение понижения температуры замерзания или кипения раствора позволяет решать целый ряд вопросов, касающихся свойств данного раствора и растворенного вещества. Метод исследования, основанный на измерении температуры замерзания растворов, называется криоскопическим методом или криоскопией, а метод, основанный на измерении температуры кипения растворов получил название эбуллископического метода или эбуллиоскопии (рис. 28).
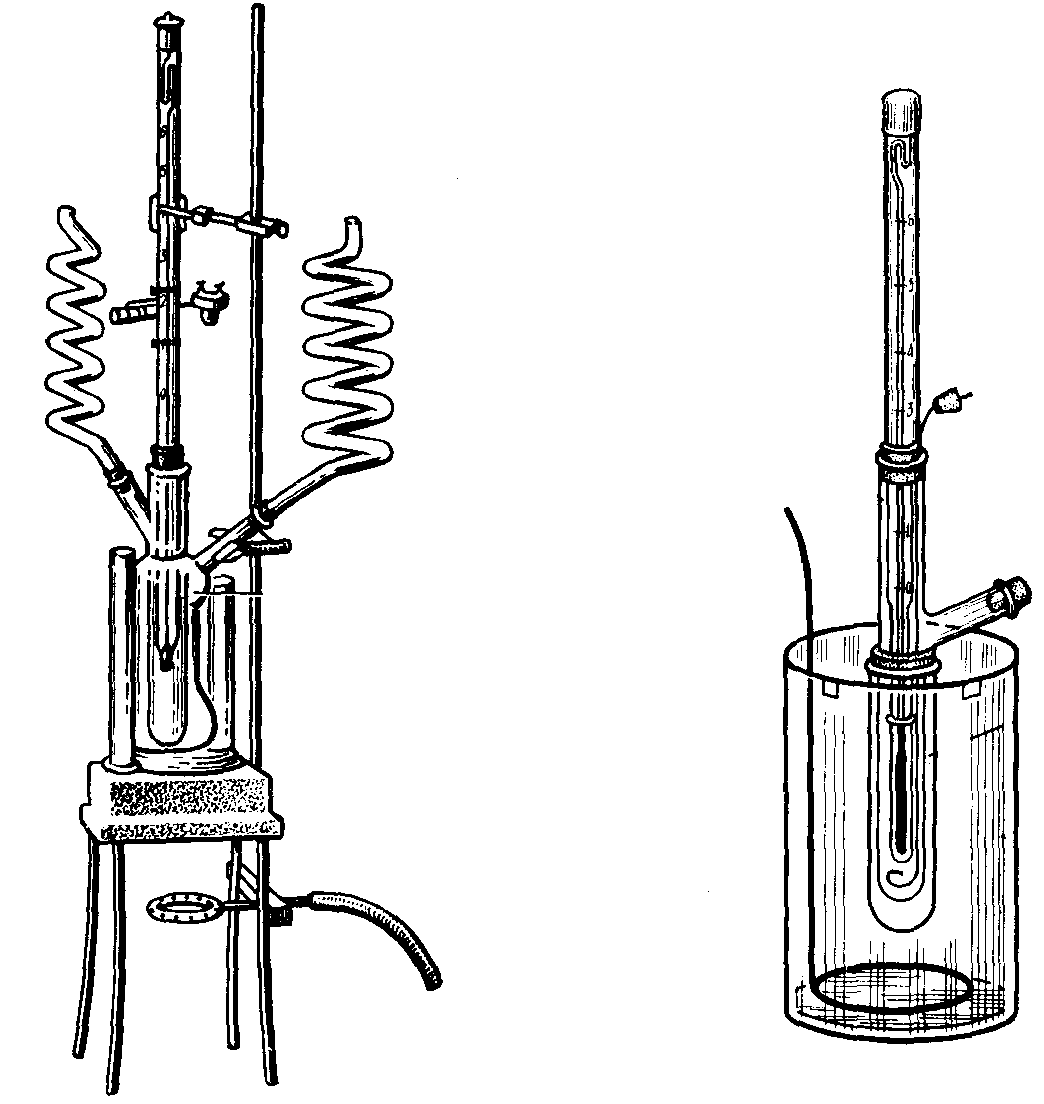
а б
Рис. 28. Аппараты для эбуллиоскопического (а) и криоскопического (б) определения молекулярных масс
В лабораторной практике криоскопический метод нашел значительно большее распространение по сравнению с методом эбуллиоскопии, т.к. измерять температуры замерзания растворов значительно проще и безопаснее, чем температуры их кипения.
Так, криоскопический метод часто используется для определения молекулярной массы вещества. Согласно следствию из закона Рауля
tзам.=K·m=
![]()
где nв-ва – химическое количество растворенного вещества; mр-теля – масса растворителя (в граммах).
Учитывая, что
![]() и подставив это выражение в вышестоящее
уравнение, можно решить его относительно
Мв-ва
и подставив это выражение в вышестоящее
уравнение, можно решить его относительно
Мв-ва
Мв-ва=K![]()
Измерение осмотического давления раствора с помощью осмометра часто бывает не совсем точным, т.к. на практике трудно подобрать подходящую мембрану, которая обладала бы идеальной полупроницаемостью. В этом случае более правильное значение росм.можно получить косвенным путем, например, с помощью метода криометрии.
Измерив tзам.раствора,
можно рассчитать его моляльную
концентрацию![]() .
.
Для разбавленных растворов (плотность которых близка к плотности воды) без большой погрешности можно принять, что их молярная концентрация С, выраженная в моль/дм3, равна моляльной концентрацииmвыраженной в моль/кг. Тогда в уравнение Вант-Гоффа для осмоса вместо С можно подставитьm(моляльную концентрацию)
росм.=![]()
и рассчитать значение осмотического давления раствора.
С помощью метода криометрии можно определять суммарную моляльную концентрацию всех веществ, содержащихся в биологических жидкостях
![]() ,
,
а также степень диссоциации слабых электролитов и изотонический коэффициент Вант-Гоффа.
Коллигативные свойства растворов электролитов. Изотонический коэффициент Вант-Гоффа
Законы Вант-Гоффа и Рауля справедливы
для идеальных растворов, т.е. таких, в
которых нет химического взаимодействия
между компонентами раствора, а также
не происходит диссоциация или ассоциация
частиц растворенного вещества. Для
данных систем экспериментально найденные
и теоретически рассчитанные величины
росм.,tкип.,tзам.,![]() совпадают.
совпадают.
Реальные растворы электролитов по своим свойствам отличаются от идеальных.
Так, для растворов электролитов
экспериментально найденные значения
вышеперечисленных величин всегда
больше, чем рассчитанные по законам
Вант-Гоффа и Рауля. Т.е., растворы
электролитов на практике ведут себя
так, как будто они содержат больше частиц
растворенного вещества, чем это следует
из их аналитической концентрации.
Исходя из этого, Вант-Гофф предложил
для растворов электролитов при
теоретическом расчете росм.,tкип.,tзам.,![]() использовать
поправочный коэффициентi,
который получил названиекоэффициента
Вант-Гоффаилиизотонического
коэффициента:
использовать
поправочный коэффициентi,
который получил названиекоэффициента
Вант-Гоффаилиизотонического
коэффициента:
росм.=iCRT;tкип.=iEm;tзам.=iKm;![]() =i1.
=i1.
Изотонический коэффициент показывает, во сколько раз реальное число частиц растворенного вещества больше, чем теоретически ожидаемое (если предполагать, что вещество в растворе присутствует только в виде молекул).
Для идеальных растворов электролитов i>1.
КоэффициентВант-Гоффа показывает также,
во сколько раз наблюдаемое опытное
значение росм.,tкип.,tзам.,![]() больше теоретически вычисленного, т.е.:
больше теоретически вычисленного, т.е.:
![]()
Причину отклонения растворов электролитов от законов Рауля и Вант-Гоффа впервые объяснил шведский ученый С. Аррениус. Он показал, что электролиты за счет действия молекул растворителя распадаются на ионы. Этот процесс приводит к увеличению реального числа частиц растворенного вещества.
Максимально значение изотонического коэффициента (imax) для любого электролита будет при этом равно числу ионов, которые образуются при полной диссоциации его молекулы (или формульной единицы), т.к. именно во столько раз возрастет число частиц электролита в растворе.
С ванте
Аррениус (1859 – 1927).
Шведский физикохимик, основные работы
которого посвящены учению о растворах
и кинетике химических реакций. Он получил
Нобелевскую премию по химии в 1903 году
за создание теории электролитической
диссоциации. Также им была разработана
одна из наиболее известных теорий кислот
и оснований. Однако еще большую известность
имеют его работы в области химической
кинетики. С. Аррениус высказал мысль,
что реакционными являются не все, а
только активные молекулы. Он ввел понятие
энергии активации и вывел уравнение
зависимости константы скорости реакции
от температуры, носящее его имя.
ванте
Аррениус (1859 – 1927).
Шведский физикохимик, основные работы
которого посвящены учению о растворах
и кинетике химических реакций. Он получил
Нобелевскую премию по химии в 1903 году
за создание теории электролитической
диссоциации. Также им была разработана
одна из наиболее известных теорий кислот
и оснований. Однако еще большую известность
имеют его работы в области химической
кинетики. С. Аррениус высказал мысль,
что реакционными являются не все, а
только активные молекулы. Он ввел понятие
энергии активации и вывел уравнение
зависимости константы скорости реакции
от температуры, носящее его имя.
Так, для NaCl imax = 2, для Na3PO4imax = 4.
В реальных растворах диссоциация часто протекает не полностью, особенно если электролит является слабым.
Кроме того, наблюдаются межионные взаимодействия, приводящие к уменьшению числа кинетически активных частиц.
В этом случае величина iбудет меньше его возможного максимального значения и будет зависеть от степени диссоциации электролита:
i= 1 +α(m– 1)
где α – степень диссоциации электролита (в долях единицы); m – число ионов, образующихся при полном распаде одной молекулы или одной формульной единицы электролита.
Таким образом, из двух растворов однотипных электролитов (т.е. распадающихся на одно и то же число ионов) с одинаковой молярной концентрацией изотонический коэффициент будет больше в растворе электролита с более высокой степенью диссоциации α. Соответственно, и росм.,tкип.,tзам.для такого раствора тоже будут иметь большие значения.
Если же молярная концентрация и степень диссоциации электролитов разного типа в растворе одинаковые, то значение iбудет выше для электролита, диссоциирующего на большее число ионовm.
