
УМК по теплотехнике
.pdf
т. е. |
|
dS |
Q |
|
|
|
(3.60) |
|
|
T |
|
|
|
||||
|
|
|
|
|
|
|
||
— второе начало термодинамики или принцип возрастания энтропии |
|
|||||||
dS dS dS і |
Q |
, но dS |
Q |
, |
тогда dS 0 , или dS і |
Q |
, |
|
T |
T |
T |
||||||
|
|
|
|
|
||||
т. е. для изолированных систем энтропия всегда только возрастает.
T |
|
Q*1 |
2 |
|
|
|
B |
|
|
|
A |
|
|
|
1 |
|
|
|
|
|
D |
C |
1 |
|
|
|
|
||
|
|
T |
|
|
|
|
|
|
|
|
|
|
T2 |
|
|
|
Q*2 |
|
|
S1 |
|
dS |
S2 |
S |
Рис. 3.15. К определению энтропии
3.1.11. ТЕРМОДИНАМИЧЕСКИЕ ЦИКЛЫ ДВИГАТЕЛЕЙ ВНУТРЕННЕГО СГОРАНИЯ
Термодинамическими циклами ДВС называются циклы, в которых процессы подвода и отвода тепла осуществляются на изобарах и изохорах (P=idem, V=idem), а процессы сжатия и расширения протекают адиабатически ( Q=0) при неизменном количестве рабочего тела на всех стадиях процесса. Различают три основных вида двигателей: а) поршневые; б) турбинные; в) реактивные.
В поршневых двигателях осуществляется рабочий процесс при непрерывном изменении объема; основным видом работы является термодинамическая. Основные рабочие процессы (сжатие, подвод теплоты, расширение) осуществляются последовательно в одном и том же заданном объеме. В турбинных двигателях эти процессы осуществляются одновременно, но в разных частях машины; основным видом работы является потенциальная.
Для обозначения наименований циклов первым символом для поршневых ДВС будет степень сжатия (для газотурбинных — соотношение
50

давлений сжатия С), и вторым последующим символом — процессы, в ко- |
||||||||
торых осуществляется подвод теплоты ( -V; C-P). |
|
|
||||||
|
3.1.11.1. Циклы поршневых двигателей внутреннего сгорания |
|||||||
|
а) с подводом теплоты при V=idem (цикл Отто) |
|
||||||
P |
|
3 |
|
|
T |
m |
3 |
|
|
|
|
|
|
|
|||
|
|
|
|
|
T3 |
|
||
|
|
|
|
|
|
|
|
|
|
|
q1 |
|
|
|
|
q1 |
|
|
|
|
|
|
|
|
|
|
P2 |
|
|
|
|
2 |
=idem |
|
|
2 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
q2 |
|
|
=idem |
|
|
|
|
|
|
|
|
|
|
P1 |
|
|
|
|
1 |
|
n |
|
|
|
1 |
|
T |
1 |
|
|
|
|
|
|
|
|
q2 |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
a |
b |
S |
|
|
|
|
Рис. 3.16. Карбюраторные и газовые ДВС |
|
|
|
|
|||||
|
|
|
|
|
|
t |
1 |
1 |
; |
|
|
|
(3.61) |
|
|
|
|
|
|
k 1 |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
степень сжатия |
1 |
; степень повышения давления |
P3 |
(рис. 3.16); |
|||||||||
|
|
|
|
|
2 |
|
|
|
|
P |
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
P |
2 |
q1 p |
3 |
|
|
|
|
T |
|
|
|
|
|
|
|
|
|
|
m |
|
|
3 |
|
||||
P2 |
|
|
|
|
|
|
|
T3 |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
q1 p |
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
=idem |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
2a |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
q2 |
|
=idem |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
q2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P1 |
|
|
|
|
|
|
|
1 |
|
|
|
n |
|
|
|
|
|
|
1 |
|
T |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
a |
|
|
b |
S |
|
|
|
|
|
|
Рис. 3.17. Изображение цикла Дизеля |
|
|
|
|
|||
б) с подводом теплоты при P=idem (цикл Дизеля)
51

|
|
|
|
|
|
|
|
t |
1 |
|
1 |
|
k 1 |
|
; |
|
|
|
|
|
(3.62) |
|
|
|
|
|
|
|
|
|
k 1 |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
k 1 |
|
|
|
|
|
|
|
||||
степень сжатия |
1 |
; степень предварительного расширения |
3 |
(рис. |
||||||||||||||||||
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
3.17); |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
в) цикл с комбинированным подводом теплоты (цикл Тринклера или |
||||||||||||||||||||||
Сабате) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2-3 =idem; |
3-4 P=idem; |
5-1 =idem (рис. 3.18); |
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
P |
|
|
|
|
|
t |
1 |
|
1 |
|
|
k 1 |
|
|
|
|
|
|
1 |
; |
3 ; |
|
4 |
|
; |
k 1 |
1 k 1 |
. |
|
(3.63) |
||||||||
|
|
|
2 |
|
|
P |
|
3 |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
P |
2' |
q1 p |
|
3 |
|
|
|
|
|
|
|
|
T |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|||||
|
q1 |
|
|
|
|
|
|
|
|
|
|
T3 |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
P2 |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
q1p |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
q1 |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2' |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2b |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2a |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
q2 |
|
|
|
|
|
|
q2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P1 |
|
|
|
|
|
|
|
1 |
|
|
|
T1 |
|
1 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
a |
|
|
|
b |
|
S |
||||
Рис. 3.18. Цикл Тринклера
3.1.11.2. Циклы газотурбинных установок
а) цикл с подводом теплоты при V=idem (цикл Гемфри)
|
|
|
|
1 |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
t |
1 |
1 |
|
k |
1 |
; |
P |
|
|
||
|
|
|
|
3 |
(рис. 3.19); |
(3.64) |
|||||
k 1 |
1 |
P |
|||||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
2 |
|
|
|
б) цикл с подводом теплоты при P=idem (цикл Брайтона)
1 |
1 |
; |
1 |
1 |
|
; |
|
1 |
; |
|
P2 |
(рис. 1.20). |
(3.65) |
||
k 1 |
|
k 1 |
|
|
P |
||||||||||
t |
|
t |
|
|
|
|
|
|
|
|
|||||
|
|
k |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
2 |
|
|
1 |
|
|
Сравнение циклов ГТУ при одинаковых значениях соотношений давлений сжатия в компрессоре и одинаковых температурах перед турбиной Т3 показывает, что термический к.п.д. цикла ГТУ при сгорании при V=idem несколько выше, чем к.п.д. цикла ГТУ со сгоранием при P=idem. Вместе с тем в реальных установках эффективность цикла ГТУ с подводом тепла при V=idem ниже, чем при P=idem из-за снижения к.п.д. турбины.
52
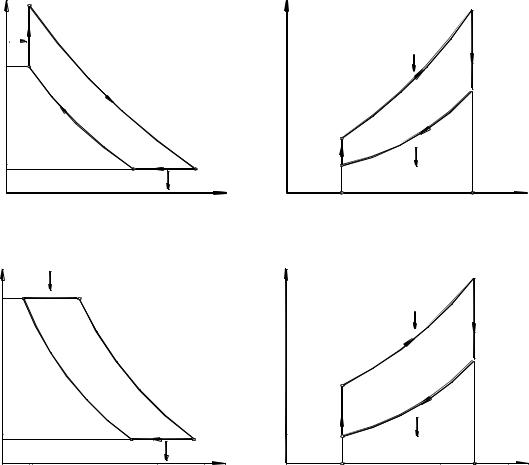
Кроме того, такая схема предусматривает более сложную конструкцию камеры ГТУ. По указанным причинам ГТУ со сгоранием при V=idem не имеют широкого применения в технике.
P |
|
3 |
|
|
T |
|
|
|
q1 |
|
|
|
|
|
|
P2 |
|
|
|
|
|
|
q1 |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
idem |
|
|
|
|
|
|
= |
|
|
|
|
|
|
|
|
P=idem |
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
P1 |
|
|
|
|
1 |
|
q2p |
|
1 |
|
4 |
|
|
||
|
|
q2p |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
a |
|
|
|
|
|
Рис. 3.19. Цикл Гемфри |
|
|
||
P |
|
q1p |
|
|
T |
|
|
|
2 |
|
|
|
|
|
|
P2 |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
q1 |
|
|
|
|
|
|
2=idem |
|
|
|
|
|
|
|
P |
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
1=idem |
|
|
|
|
|
|
|
P |
P1 |
|
|
|
|
1 |
|
q2p |
|
|
|
|
|
|
||
|
|
1 |
q2p |
4 |
|
|
|
|
|
|
|
|
a |
|
|
 3
3
 4
4
b  S
S
 3
3
 4
4
b  S
S
Рис. 3.20. Цикл Брайтона
Эффективность ГТУ простейшей схемы с подводом тепла при P=idem может быть повышена, если в цикле осуществить регенеративный подогрев воздуха, поступающего в камеру сгорания, за счет теплоты продуктов сгорания, выходящих из турбины. Такие ГТУ называются газотурбинными установками с регенерацией теплоты.
53
3.1.12. Типовые задачи к разделам курса «термодинамика»
3.1.12.1. Параметры, уравнение состояния идеального газа
Задача 1. Ртутный вакууметр, присоединенный к сосуду с метаном СН4, показывает разряжение 0,056 МПа. Атмосферное давление по ртутному барометру составляет 768 мм рт. ст. (0,102 МПа). Определить абсолютное давление в сосуде и плотность метана, если температура в сосуде равна 20 С. Показания вакуумметра и барометра приведены к температуре
0 С.
Решение. Абсолютное давление в сосуде определяется по формуле Рабс=В0 Рвак=0,102 0,056=0,046 МПа. Плотность газа находим из уравнения состояния, предварительно определив газовую постоянную:
|
|
R |
|
R |
|
|
8314 |
518 |
Дж / кг К ; |
PV RT ; |
|||||
|
|
|
|
16,04 |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
1 |
|
|
|
|
1 |
|
|
P |
|
0,046 106 |
|
|||
P |
|
RT |
|
|
|
|
|
|
|
0,302 кг / м3 . |
|||||
|
V |
RT |
518 273 20 |
||||||||||||
Задача 2. Баллон с кислородом емкостью 20 л находится под давлением 1,0 МПа при t=15 С. После израсходования части кислорода давление понизилось до 0,76 МПа, а температура уменьшилась до 10 С. Определить массу израсходованного кислорода.
Решение. Из уравнения состояния PV=GRT находим, что до расходования кислорода его масса в баллоне была равна:
|
P V |
|
1,0 106 20 10 |
3 |
||
G |
1 |
1 |
|
|
|
0,267 кг |
|
|
|
|
|||
1 |
R |
T1 |
|
259,8 288 |
|
|
|
|
|
|
|||
R |
|
|
R |
|
|
8314 |
259,8 |
Дж / кг К . |
|||
|
|
|
|
||||||||
|
o |
2 |
|
|
32 |
|
|
|
|||
После израсходования части кислорода масса его в баллоне будет |
|||||||||||
равна: |
|
|
|
|
|
|
|
|
|
|
|
G2 |
|
P V |
|
0,7 106 0,02 |
0,207 кг ; |
||||||
|
2 |
|
|
|
|
|
|
||||
|
R T2 |
259,8 283 |
|||||||||
|
|
|
|
||||||||
следовательно, расход кислорода составит:
G G1 G2 0,267 0,207 0,06 кг .
Задача 3. Определить удельный объем пропана (С3Н8) как идеального газа при следующих условиях: температура газа t=20 С, манометрическое давление газа в баллоне 5,6 МПа, абсолютное давление газа в помещении равно 0,099 МПа.
Решение. Абсолютное давление газа в баллоне Рабс=Рман+В0=5,6+0,099=5,699 МПа;
54

удельная газовая постоянная пропана
R |
|
R |
|
8314 |
188,6 Дж / кг К ; |
|
|
44,09 |
|||
|
|
|
|
абсолютная температура газа Т=273+20=293 К;
удельный объем пропана в рассматриваемых условиях
V |
RT |
|
188,6 293 |
0,0097 м3 |
/ кг ; |
|
P |
5,699 106 |
|||||
|
|
|
|
удельный молярный объем пропана при тех же условиях равен:
V C3 H8 V 44,9 0,0097 0,435 м3 / кмоль ,
или, что то же самое:
|
|
|
|
|
|
|
8314 293 |
|
|
|
|
|
RT |
|
|
||
V |
|
|
0,435 м3 / кмоль. |
|||||
|
P |
5,699 106 |
||||||
|
|
|
|
|
|
|||
3.1.12.2. Газовые смеси
Задача 1. По данным анализа установлен следующий объемный состав природного газа: СН4=96%; С2Н6=3%; С3Н8=0,3%; С4Н10=0,2%; СО2=0,1%; N2=0,4%. Определить среднюю молекулярную массу природного газа ( m), плотность газа в нормальных условиях ( ), массовые концентрации компонентов (mi), их парциальные давления (Pi), средние теплоемкости (Сpm, Cvm) и показатель адиабаты.
Решение. Молекулярные массы составляющих смеси газов находим по данным физических характеристик компонентов газа из справочных таблиц:
CH |
=16,04; |
C |
H |
|
=30,07; |
C |
H |
=44,09; |
||
|
4 |
|
2 |
|
6 |
|
3 |
|
|
8 |
C |
H |
=58,12; |
CO |
=44,01; |
N |
|
=28,02. |
|||
4 |
|
1 0 |
|
|
2 |
|
|
2 |
|
|
Молекулярная масса природного газа определяется по уравнению
n |
|
1 |
|
|
|
m ri i |
|
|
; |
||
|
|
|
|
||
n |
|
mi |
|
||
i 1 |
|
|
|
||
|
i |
|
|
||
|
i 1 |
|
|
|
|
где i — молекулярная масса компонентов смеси;
ri — молярная (объемная) концентрация компонентов смеси; mi — массовая концентрация компонентов смеси.
Так как в условии задачи дан объемный состав газа, то удобнее воспользоваться первым уравнением соотношения:
n
m ri i =0,96 16,04+0,03 30,07+0,003 44,09+0,002 58,12+
i 1
55

+0,001 44,01+0,004 28,02=16,704 (кг/кмоль).
Плотность газа при нормальных условиях (0 С и 0,1 МПа) можно определить из уравнения Клапейрона PV=RT или из закона Авогадро, утверждающего, что удельный молярный объем газа в нормальных условияхвеличина постоянная и равна:
|
|
|
|
V |
m |
|
|
V |
m |
22,4 м 3 / кмоль ; |
|||||
|
|||||||
|
|
|
|
|
|||
|
|
|
|
|
|
||
ь 16,7 0,745 кг / м3 .
М22,4
Из уравнения Клапейрона при t=0 C и Р=0,1 МПа
|
P |
|
|
|
|
|
|
0,1 10 |
6 |
0,74 кг / м3 |
, |
|||
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
||||||
|
RT |
|
|
|
|
497,7 273,15 |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
где R |
|
|
|
R |
|
|
|
8314 |
|
497,7 Дж / кг К . |
||||
|
m |
|
16,70 |
|
||||||||||
|
|
|
|
|
|
|
|
|
||||||
Массовые и объемные концентрации газа связаны между собой соотношением
mi |
|
ri |
, отсюда m |
|
|
i |
r , |
|
|
i |
|
||||
i |
m |
|
|
i |
|||
|
|
|
|||||
cледовательно, массовые концентрации отдельных компонентов смеси равны:
m |
|
|
|
|
CH4 |
|
|
r |
|
|
|
16,04 |
0,96 0,95 ; |
||||||||||||||||||
CH4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
m |
|
|
|
|
CH4 |
|
16,07 |
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
m |
|
|
|
|
|
C2 H 6 |
r |
|
|
|
30,07 |
0,03 0,056 ; |
|||||||||||||||||||
C2 H 6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
m |
|
|
|
|
C2 H 6 |
|
|
|
16,07 |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
m |
|
|
|
|
|
|
C3 H 8 |
|
|
|
r |
|
|
|
44,09 |
|
0,003 0,00823 ; |
||||||||||||||
C3 H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
8 |
|
|
|
|
|
m |
|
|
|
|
|
|
C3 H 8 |
|
|
|
16,07 |
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
m |
|
|
|
|
|
|
C4 H1 0 |
|
r |
|
|
|
|
58,12 |
0,002 0,00723 ; |
||||||||||||||||
C4 H1 0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
m |
|
|
|
|
C4 H1 0 |
|
|
|
16,07 |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
m |
|
|
|
|
N 2 |
|
r |
|
|
|
|
|
|
|
28,02 |
0,004 0,00697 ; |
|||||||||||||||
N |
2 |
|
|
m |
N |
2 |
|
|
|
16,07 |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
m |
|
|
|
CO2 |
|
r |
|
|
|
44,01 |
0,001 0,002738 . |
||||||||||||||||||||
CO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
m |
|
|
|
CO |
|
16,07 |
|
|
|
|
|
||||||||||||||
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Сумма массовых концентраций, как и молярных (объемных), равна единице:
n |
n |
mi |
ri 1. |
i 1 |
i 1 |
56

Парциальные давления отдельных компонентов газа определяются по закону Дальтона из соотношения Pi=ri P. Находим давление каждого компонента, входящего в смесь:
PCH4 |
rCH4 P 0,96 0,1 0,096 МПа , |
|
PC2 H 6 |
rC2 H 6 |
P 0,03 0,1 0,003 МПа , |
PC3 H8 |
rC3 H8 |
P 0,003 0,1 0,0003 МПа , |
PC4 H1 0 rC4 H1 0 P 0,002 0,1 0,0002 МПа , PCO2 rCO2 P 0,001 0,1 0,0001 МПа , PN 2 rN 2 P 0,004 0,1 0,0004 МПа .
Сумма парциальных давлений равна давлению смеси:
n |
|
|
|
|
|
|
Pi |
PCH4 |
PC2 H 6 |
PC3 H8 |
PC4 H10 PCO2 |
PN2 |
0,1 МПа . |
i 1 |
|
|
|
|
|
|
Средняя теплоемкость смеси определяется по уравнениям:
n
массовая теплоемкость смеси: C pm mi C pmi ;
i 1
n
молярная теплоемкость смеси: C pm ri C pmi ,
i 1
где C pmi — массовая теплоемкость компонентов смеси при данной температуре;
C pmi — молярная теплоемкость компонентов смеси при данной температуре.
При температуре 0 С и давлении 0,1 МПа можно принять, что тепло-
емкость метана CPCH |
4 |
= 2,17 кДж/(кг К); этана CPC |
H |
= 1,65 кДж/(кг К); |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
6 |
||||
пропана CC |
H |
8 |
= 1,56 кДж/(кг К); бутана CPC |
H |
10 |
= 1,58 кДж/(кг К); углекис- |
||||||||||||||||
3 |
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
||||||||
лого газа CPCO |
= 0,815 кДж/(кг К); азота CPN |
2 |
= 1,039 кДж/(кг К). Следова- |
|||||||||||||||||||
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
тельно, массовая теплоемкость смеси при постоянном давлении равна: |
||||||||||||||||||||||
|
|
n |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
C pm mi C pmi |
0,95 2,17+0,056 1,65+0,008 1,56+0,007 1,58+ |
|||||||||||||||||||||
|
|
i1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
+0,0027 0,815+0,0069 1,039=2,18 кДж/(кг К). |
|||||||||||||||||||
Молярная теплоемкость смеси газов при постоянном давлении |
||||||||||||||||||||||
|
|
|
|
|
pm m C pm 16,07 2,18 35,11 кДж/(кмоль К). |
|||||||||||||||||
|
|
|
|
C |
||||||||||||||||||
Из уравнения Майера C p Cv R ; |
|
p |
|
|
v |
|
|
можно определить |
||||||||||||||
C |
C |
R |
||||||||||||||||||||
теплоемкость смеси при постоянном объеме: |
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
Cv |
C p R 2,18 0,497 1,683 |
кДж/(кг К); |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
p |
|
35,11 8,314 26,79 кДж/кг К. |
||||||||||
|
|
|
|
|
|
C v |
C |
R |
||||||||||||||
57
Показатель адиабаты природного газа указанного состава (как идеального газа)
|
C p |
|
|
|
|
|
|
|
|
|
K |
|
C p |
|
2,18 |
|
35,11 |
1,30. |
|||
|
|
|
|
|
||||||
Cv |
|
|
1,68 |
26,79 |
||||||
C v |
||||||||||
|
|
|
|
|
||||||
Задача 2. До какого давления необходимо сжать смесь газов, состоящую по весу из СО2=12%, О2=8%, N2=80%, чтобы при температуре t=20 С ее плотность была 1,6 кг/м3.
Решение. Находим молекулярную массу смеси через массовые концентрации компонентов смеси:
m |
|
1 |
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
29,6 |
кг/кмоль. |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
mi |
|
|
mO2 |
|
mN 2 |
|
|
|
|
|
0,08 |
0,8 0,12 |
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
mCO2 |
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
n |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
i 1 i |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
32 |
|
28 44 |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
O |
2 |
|
|
|
|
N |
2 |
|
|
CO |
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
Давление смеси определим из уравнения состояния PV RT |
|
R |
T : |
|||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
P |
|
|
|
RT |
|
|
RT |
|
8314 293 1,6 |
1,31 105 |
0,13 МПа. |
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
V |
|
|
|
|
|
29,6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
Задача 3. Определить весовой состав газовой смеси, состоящей из углекислоты СО2 и азота N2, если известно, что парциальное давление углекислого газа PCO2 =1,1 ат, а давление смеси равно 3 ат.
Решение. Определим парциальное давление азота:
PN Pm PCO2 3 1,1 1,9 ат.
Объемная концентрация азота по закону Дальтона
r |
Pi |
; r |
|
|
PN |
|
1,9 |
0,633. |
|
N |
|
|
|||||
i |
Pm |
|
|
Pm |
3 |
|
||
|
|
|
|
|
||||
Объемная концентрация углекислого газа
rCO2 1 0,633 0,367.
Молекулярная масса смеси
n
m i ri CO2 rCO2 N rN 44 0,367 28 0,633 33,96 кг/кмоль.
i 1
Используя соотношение i/ m=mi/ri, определим весовую концентрацию азота и углекислого газа:
m |
|
r |
|
|
N |
|
0,633 |
28 |
|
0,52 ; |
|||
N |
N |
|
|
m |
|
33,96 |
|||||||
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
m |
|
r |
|
CO2 |
0,367 |
44 |
0,48 . |
||||||
CO |
|
|
|
|
|
||||||||
|
|
|
CO |
|
|
m |
|
|
33,96 |
|
|||
|
2 |
|
2 |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
||||
58

n
Проверка: mi 1 ; mi 0,52 0,48 1.
i 1
3.1.12.3. Первое начало термодинамики
Задача 1. При движении природного газа по трубопроводу его параметры изменяются от t1=50 C и P1=5,5 МПа до t2=20 C и P2=3,1 МПа. Средняя молекулярная масса газа m=16 кг/кмоль. Средняя теплоемкость газа Сpm=1,62 кДж/(кг С). Считая газ идеальным и принимая во внимание, что внешняя полезная работа на участке трубопровода равна нулю (w*1,2=0), определить удельную величину внешнего (q*1,2) и внутреннего (q*1,2) теплообмена.
Решение. Из уравнения первого начала термодинамики по внешнему балансу тепла и работы для потока в условиях, когда w*1,2=0, имеем
Q*1,2=i2-i1=Cpm(T2-T1)=Cpm(t2-t1)=1,62(50-20)=48,6 кДж/кг.
Снижение давления газа в газопроводе с 5,5 МПа до 3,1 МПа вызывает внутренний теплообмен в трубе. Вся работа, связанная с падением давления, идет на необратимые потери. Величину этих потерь можно определить из уравнения изотермического процесса движения газа по газопроводу. Потенциальная работа изотермического процесса расширения (T2=idem) определяется уравнением
2 |
2 |
dP |
P V m ln |
P1 |
|
|
w1,2 V dP P V |
; |
|||||
P |
P2 |
|||||
1 |
1 |
|
|
|||
PV RT ; w1*,*2 RTm ln PP1 ;
2
средняя теплоемкость газа в газопроводе
T |
T1 T2 |
|
323,2 |
293,2 |
313,2 K ; |
|
|
|
|||
m |
2 |
2 |
|
|
|
|
|
|
|||
следовательно, внутренний теплообмен
q** |
w** |
RT |
|
ln |
P1 |
|
8314 |
313 ln |
5,5 |
93,2 кДж/кг. |
m |
|
|
|
|||||||
1,2 |
1,2 |
|
|
P2 |
16 |
3,1 |
|
|||
|
|
|
|
|
|
|||||
Приведенный теплообмен в трубопроводе q1,2=q*1,2+q**1,2=48,6+93,2=141,8 кДж/кг.
Задача 2. 3 кг метана (СН4) сжимаются при затрате работы 800 кДж. Внутренняя энергия при этом изменяется на 595 кДж. Молярная теплоемкость при постоянном объеме 26,5 кДж/(кмоль К). Определить количество теплоты, разность температур и изменение энтальпии.
59
