- •Министерство образования и науки российской федерации
- •«Тюменский государственный нефтегазовый университет» г.К.Севастьянова, т.М.Карнаухова Общая химия
- •Оглавление
- •1.2. Основные понятия химии
- •1.3. Основные законы химии
- •2. Современная теория строения атома. Периодический закон и система элементов д.И. Менделеева
- •2.1. Общие положения
- •2.2. Развитие представлений о строении атома
- •2.3. Квантово – механическая модель атома водорода. Исходные представления квантовой механики
- •2.4. Модель состояния электрона в атоме
- •2.5. Квантовые числа
- •2.6. Электронные конфигурации (формулы) элементов
- •2.7. Порядок заполнения электронами уровней, подуровней, орбиталей в многоэлектронных атомах
- •2.8. Электронные семейства элементов
- •2.9. Понятие об электронных аналогах
- •2.10. Периодический закон и периодическая система элементов д.И. Менделеева
- •2.11. Структура периодической системы химических элементов д. И. Менделеева
- •2.12. Периодическая система д.И. Менделеева и электронная структура атомов
- •2.13. Периодичность свойств элементов
- •3.Химическая связь и строение молекул
- •3.1. Основные понятия и определения
- •3.2. Теория метода валентных связей
- •3.3. Ковалентная связь
- •3.4. Насыщаемость ковалентной связи
- •3.5. Направленность ковалентной связи
- •3.6. Полярность и поляризуемость химической связи
- •3.7. Полярность молекул (типы ковалентных молекул)
- •3.8. Алгоритм выполнения заданий по теме «Химическая связь. Строение молекул»
- •3.8. Ионная связь
- •3.9. Металлическая связь
- •4. Основные классы неорганических соединений
- •4.1. Классификация веществ
- •4.2. Оксиды
- •4.3. Гидроксиды
- •4.4. Кислоты
- •4.5. Основания
- •4.6. Соли
- •5. Энергетика и направленность химических процессов (элементы химической термодинамики)
- •5.1 Основные понятия и определения
- •5.2. Первый закон термодинамики
- •5.3. Тепловой эффект химической реакции. Термохимия. Закон Гесса
- •5.4. Энтропия
- •5.5. Свободная энергия Гиббса
- •5.6. Свободная энергия Гельмгольца
- •6. Химическая кинетика
- •6.1. Основные понятия химической кинетики
- •6.2. Влияние природы реагирующих веществ
- •6.3. Закон действующих масс
- •6.4. Зависимость скорости химической реакции от температуры
- •6.5. Влияние катализатора
- •7. Химическое равновесие
- •7.1. Общие представления о химическом равновесии. Константа химического равновесия
- •7.2. Смещение химического равновесия. Принцип Ле Шателье
- •7.3. Фазовые равновесия. Правило фаз Гиббса
- •8. Дисперсные системы. Растворы
- •8.1. Дисперсные системы и их классификация
- •8.2. Общая характеристика растворов
- •8.3. Способы выражения концентрации растворов
- •8.4. Растворимость
- •8.5. Природа жидких растворов
- •8.6. Типы и свойства растворов
- •8.7. Свойства растворов неэлектролитов
- •8.8. Растворы электролитов
- •2. Температура.
- •3. Концентрация раствора.
- •4. Наличие одноименных ионов.
- •8.9. Равновесия и обменные реакции в растворах электролитов
- •8.10. Гидролиз солей
- •8.11. Комплексные соединения
- •9. Окислительно-восстановительные реакции
- •9.1. Общие понятия и определения
- •1. Метод электронного баланса.
- •2. Метод ионно-электронный (метод полуреакций; метод ионно-электронного баланса).
- •9.2. Восстановители и окислители
- •Важнейшие восстановители и окислители
- •9.3. Влияние среды на окислительно-восстановительные реакции
- •Кислая среда (рн 7)
- •9.4. Типы окислительно-восстановительных реакций
- •9.5. Окислительно – восстановительные (электродные) потенциалы
- •9.6. Направление протекания окислительно-восстановительных реакций
- •10. Электрохимические процессы
- •10.1. Гальванические элементы (химические источники электрического тока)
- •10.2. Электролиз
- •10.3. Коррозия металлов
- •10.4. Защита металлов от коррозии
- •11. Свойства металлов
- •11.1. Физические свойства металлов
- •11.2. Химические свойства металлов
- •Очень разб.
- •Литература
- •Приложение 1 Электронные конфигурации элементов
- •625000, Г. Тюмень, ул. Володарского, 38
- •625039, Г. Тюмень, ул. Киевская, 52
3.7. Полярность молекул (типы ковалентных молекул)
Следует отличать полярность молекулы от полярности связи. Для двухатомных молекул типа АВ эти понятия совпадают, как это уже показано на примере молекулы HCl. В таких молекулах чем больше разность электроотрицательностей элементов (∆ЭО), тем больше электрический момент диполя. Например, в ряду HF, HCl, HBr, HI он уменьшается в той же последовательности, как и относительная электроотрицательность.
Молекулы могут быть полярными и неполярными в зависимости от характера распределения электронной плотности молекулы. Полярность молекулы характеризуется значением электрического момента диполя μмол, который равен векторной сумме электрических моментов диполей всех связей и несвязывающих электронных пар, расположенных на гибридных АО: → →
n m
м-лы = (связи)i + (несвяз.эл.пары)j.
i=1 j=1
Результат сложения зависит от полярности связей, геометрического строения молекулы, наличия неподеленных электронных пар. Большое влияние на полярность молекулы оказывает её симметрия.
Например, молекула СО2 имеет симметричное линейное строение:
![]() .
.

Поэтому, хотя связи С=О и имеют сильно полярный характер, вследствие взаимной компенсации их электрических моментов диполя молекула СО2 в целом неполярна ( м-лы = связи = 0). По этой же причине неполярны высокосимметричные тетраэдрические молекулы СН4, СF4, октаэдрическая молекула SF6 и т. д.
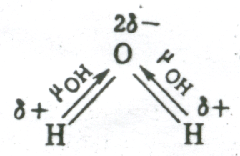
В угловой молекуле Н2О полярные связи О–Н располагаются под углом 104,5º: → →
n=2 m=2
Н2О = O–H + несвяз.эл.пары 0.
i=1 j=1
Поэтому
их моменты взаимно не компенсируются
и молекула оказывается полярной ( ).
).


Электрическим моментом диполя обладают также угловая молекула SO2, пирамидальные молекулы NH3, NF3 и т. д. Отсутствие такого момента
свидетельствует о высокосимметричной структуре молекулы, наличие электрического момента диполя – о несимметричности структуры молекулы (табл. 3.2).
Таблица 3.2
Строение и ожидаемая полярность молекул
|
Тип |
Пространственная конфигурация |
Ожидаемая полярность |
Примеры |
|
|
Линейная |
Неполярная |
|
|
|
Линейная |
Полярная |
|
|
|
Линейная |
Неполярная |
|
|
|
Угловая |
Полярная |
|
|
|
Линейная |
Полярная |
|
|
|
Плоскотреугольная |
Неполярная |
|
|
|
Тригонально-пирамидальная |
Полярная |
|
|
|
Тетраэдрическая |
Неполярная |
|
На
значение электрического момента диполя
молекулы сильно влияют несвязывающие
электронные пары, расположенные на
гибридных орбиталях и имеющие собственный
электрический момент диполя
 (направление вектора – от ядра, по оси
расположения гибридной АО). Например,
молекулыNH3
и NF3
имеют одинаковую тригонально-пирамидальную
форму, полярность связей N–H
и N–F
также примерно одинакова. Однако
электрический момент диполя NH3
равен 0,49·10-29
Кл·м, а NF3
всего 0,07·10-29
Кл·м. Это объясняется тем, что в NH3
направление электрического момента
диполя связывающей N–H
и несвязывающей электронной пары
совпадает и при векторном сложении
обусловливает большой электрический
момент диполя. Наоборот, в NF3
моменты связей N–F
и электронной пары направлены в
противоположные стороны, поэтому при
сложении они частично компенсируются
(рис. 3.15).
(направление вектора – от ядра, по оси
расположения гибридной АО). Например,
молекулыNH3
и NF3
имеют одинаковую тригонально-пирамидальную
форму, полярность связей N–H
и N–F
также примерно одинакова. Однако
электрический момент диполя NH3
равен 0,49·10-29
Кл·м, а NF3
всего 0,07·10-29
Кл·м. Это объясняется тем, что в NH3
направление электрического момента
диполя связывающей N–H
и несвязывающей электронной пары
совпадает и при векторном сложении
обусловливает большой электрический
момент диполя. Наоборот, в NF3
моменты связей N–F
и электронной пары направлены в
противоположные стороны, поэтому при
сложении они частично компенсируются
(рис. 3.15).
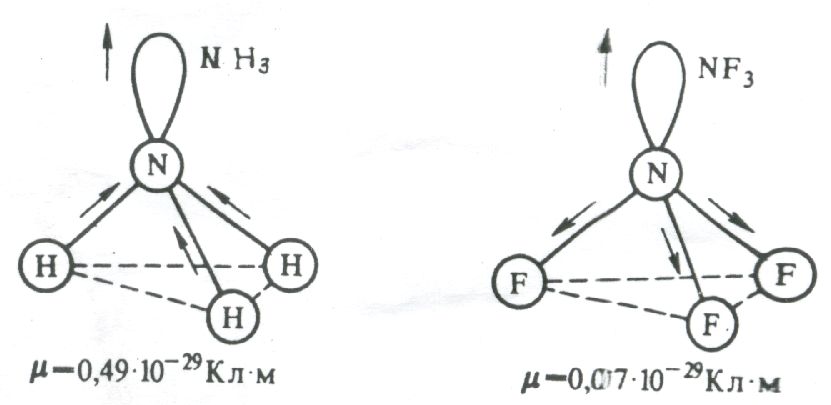

Рис 3.15. Сложение электрических моментов диполя связывающих и несвязывающих электронных пар молекул NH3иNF3
Неполярную молекулу можно сделать полярной. Для этого её надо поместить в электрическое поле с определенной разностью потенциалов. Под действием электрического поля «центры тяжести» положительных и отрицательных зарядов смещаются и возникает индуцированный или наведенный электрический момент диполя. При снятии поля молекула опять станет неполярной.
Под действием внешнего электрического поля полярная молекула поляризуется, т. е. в ней происходит перераспределение зарядов, и молекула приобретает новое значение электрического момента диполя, становится ещё более полярной. Это может происходить и под влиянием поля, создаваемого приблизившейся полярной молекулой. Способность молекул поляризоваться под действием внешнего электрического поля называют поляризуемостью.
Полярностью и поляризуемостью молекул обусловлено межмолекулярное взаимодействие. С электрическим моментом диполя молекулы связана реакционная способность вещества, его растворимость. Полярные молекулы жидкостей благоприятствуют электролитической диссоциации растворенных в них электролитов.

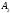
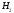 ,
,
 ,
,
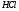 ,
,
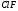
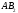
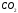 ,
,
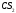 ,
,
 ,
,
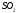 ,
,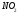
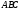
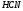
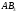
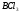 ,
,
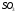
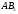
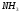 ,
,
 ,
,
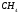 ,
,
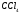 ,
,