
- •1. Механика
- •1.1. Кинематика
- •1.2. Динамика материальной точки и твердого тела
- •1.3. Законы сохранения
- •1.4. Элементы специальной теории относительности.
- •1.5. Элементы механики сплошных сред
- •2. Молекулярная физика и термодинамика
- •2.2. Статистические распределения
- •2.3. Основы термодинамики
- •2.4. Явления переноса
- •2.5. Реальные газы
- •3.Электричество и магнетизм
- •3.1. Электростатика
- •3.2. Постоянный электрический ток
- •3.3. Магнитное поле
- •3.4. Магнитное поле в веществе
- •3.5. Явление электромагнитной индукции
- •3.7. Электромагнитные колебания
- •1.1 Свет как электромагнитные волны. Геометрическая оптика
- •1.2. Интерференция волн
- •Что собой представляет волновой пакет? Суперпозиция волн, малоотличающихся друг от друга по частоте, занимающая в каждый момент времени ограниченную область пространства.
- •Что называют временем когерентности? Среднее время (tк), в течение которого амплитуда, начальная фаза колебаний и частота остаются неизменными.
- •Почему при наложении двух пучков естественного света не наблюдается интерференционной картины? Пучки должны быть когерентными.
- •В чем заключается принцип Гюйгенса? Каждая точка, до которой доходит волна, служит центром вторичных волн, а огибающая этих волн задает положение волнового фронта в следующий момент времени
- •Почему существует предел разрешающей способности оптических приборов? Из-за неточности изготовителя
- •2. Квантовая физика
- •2.1. Тепловое излучение
- •2.2. Экспериментальное обоснование основных идей квантовой теории
2.3. Основы термодинамики
Внутренняя энергия идеального газа.
Это энергия хаотического (теплового) движения микрочастиц системы (молекул, атомов, электронов, ядер и т.д.) и энергия взаимодействия этих частиц.
![]()
Число степеней свободы. Распределение энергии по степеням свободы.
Число
степеней свободы – это число независимых
переменных, полностью определяющих
положение системы в пространстве.
Одноатомный газ: 3 всего (3 поступательных),
двухатомный: 5 всего (3 поступательных,
2 вращательных), многоатомные: 6 всего
(3 поступательных, 3 вращательных)
*одноатомный
газ (i=3)
U=![]()
*двухатомный
газ (i=5)
U=![]()
*полиатомный
газ (i=6)
U=![]()
Работа газа при изменении его объема.
![]() A=
A=![]()
Количество теплоты. Удельная и молярная теплоемкости.
Количество
теплоты – это энергия, которая необходима
для нагревания тела. Удельная теплоемкость
– величина, равна количеству теплоты,
необходимому для нагревания 1кг вещества
на 1К. Молярная теплоемкость – величина,
равная количеству теплоты, необходимому
для нагревания 1 моль вещества на 1К.
c=![]() [
[![]() ]Молярная
теплоемкость:
Cm==
]Молярная
теплоемкость:
Cm==![]() ;
ν=
;
ν=![]()
Зависимость теплоемкости идеального газа от вида процесса. Уравнение Майера.
![]()
![]()
![]() -уравнение
Майера
-уравнение
Майера
Первое начало термодинамики.
Первое начало термодинамики является законом сохранения энергии для тепловых процессов
![]() ,
A,Q-
функции процесса, U-функция
состояния
Теплота,
сообщаемая системе расходуется, на
изменение ее внутр энергии и работы
совершаемой ею против внешних сил.
,
A,Q-
функции процесса, U-функция
состояния
Теплота,
сообщаемая системе расходуется, на
изменение ее внутр энергии и работы
совершаемой ею против внешних сил.
Какой процесс называется адиабатным? Уравнение Пуассона.
Адиабатный процесс – это процесс, при котором не происходит обмен теплом с окружающей средой. (δQ=0)
![]() -уравнение
Пуассона
-уравнение
Пуассона
Применение первого закона термодинамики к изобарному процессу
![]()
Применение первого закона термодинамики к изохорному процессу.
![]()
Применение первого закона термодинамики к изотермическому процессу.
![]()
Работа газа при адиабатном процессе.
![]()
Какой процесс называется политропным? Уравнение политропы.
Процесс,
в котором теплоемкость остается
постоянной (C=const)
называется политропическим. Уравнение
политропы -
![]() ,
где коэффициент
,
где коэффициент![]() называется показателем политропы.n=
называется показателем политропы.n=
![]() ,
если С=
,
если С=![]() ,
n=1-ур-е
изотермы.С=0,
n=γ,
ур-е адиабаты. С=Cp
,
n=0-ур-е
изобары. С=Сv
,n=
,
n=1-ур-е
изотермы.С=0,
n=γ,
ур-е адиабаты. С=Cp
,
n=0-ур-е
изобары. С=Сv
,n=![]() -ур-е
изохоры.
-ур-е
изохоры.
КПД тепловой машины
η=![]()
![]()
Цикл Карно и его КПД.Тепловая машина которая имеет наиб КПД изоюрел Карло: η=
 Цикл
Карно состоит из двух изотерм и двух
адиабат. КПД
цикла Карно
не зависит от в-ва рабочего тела, а
зависит только от состояния, температуры
нагревания и холодильника
Цикл
Карно состоит из двух изотерм и двух
адиабат. КПД
цикла Карно
не зависит от в-ва рабочего тела, а
зависит только от состояния, температуры
нагревания и холодильника
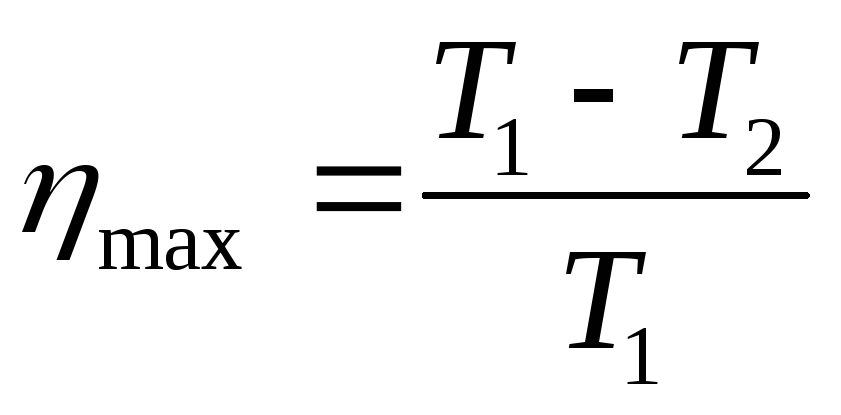
Второе начало термодинамики
Невозможен процесс самопроизвольной передачи тепла от холодного тела к горячему. *любой необратимый процесс в замкнутой системе происходит так, что энтропия системы при этом возрастает;
*в проц происход в замкнутых системах, энтропия не убывает.
Энтропия (определение, статистический смысл).
Энтропией
S
называется функция состояния системы,
дифференциалом которой является
![]() .
Энтропия является мерой неупорядочности
системы, большая энтропия соответствует
большему хаосу. Энтропия изолированных
систем не может убывать при любых
процессах.
.
Энтропия является мерой неупорядочности
системы, большая энтропия соответствует
большему хаосу. Энтропия изолированных
систем не может убывать при любых
процессах.![]() =0
– для обратимых процессов,
=0
– для обратимых процессов,
![]() >0
– для необратимых.
>0
– для необратимых.
Статистическое толкование второго начала термодинамики.
Второе начало термодинамики определяет направление протекания термодинамических процессов, указывая какие процессы в природе возможны, а какие нет.
