Archive / Конспект лекций от 02.04.12 - копия / ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ 7
.docx
ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ.
ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ.
1.Первое начало термодинамики.
Опыт показывает, что температура, а следовательно, внутренняя энергия газовой системы увеличивается при сообщении ей некоторого количества теплоты и уменьшается при совершении системой положительной работы.
ΔU = ΔQ – A или
ΔQ = ΔU + A
Это выражение представляет собой закон, который называется первым началом термодинамики. Формулировка его такова:
Количество теплоты, сообщённое системе, расходуется на увеличение её внутренней энергии и на работу, совершённую системой над внешними телами.
Первое начало термодинамики – это закон сохранения энергии применительно к тепловым процессам.
2.Применение первого начала термодинамики к различным газовым процессам.
Рассмотрим изохорный, изотермический, изобарный и адиабатный процессы.
Первые три процесса известны, а адиабатным называется процесс, который происходит без теплообмена с окружающей средой, т.е. теплота не подводится к системе и не отводится от системы.
|
Изохорный процесс V=const |
Изотермический процесс T=const |
Изобарный процесс P=const |
Адиабатный процесс ΔQ=0 |
|
A=0
Запишем уравнение Клапейрона-Менделеева для двух состояний газа P1V=νRT1 (1) P2V=νRT2 (2) Вычтем (1) из (2) Получим (P2-P1)V=νR(T2-T1), т.е. ΔP V = νR ΔT Следовательно,
|
ΔU=0
Так
как
|
ΔQ=ΔU+A
Запишем уравнение Клапейрона-Менделеева для двух состояний газа PV1=νRT1 (1) PV2=νRT2 (2) Вычтем (1) из (2) Получим P(V2-V1)= νR(T2-T1), т.е. P ΔV= νR ΔT Следовательно,
|
ΔQ=0 A= - ΔU , т.е. работа совершается за счёт внутренней энергии. |
2.Второе начало термодинамики.
Первое начало термодинамики устанавливает соответствие между количеством теплоты, полученной системой (или отнятой у системы), изменением внутренней энергии и работой, совершённой системой (или над системой). Однако первое начало термодинамики ничего не говорит о направлении протекания тепловых процессов. Например, этот закон не запрещает переход теплоты от менее нагретого тела к более нагретому, чего на опыте не наблюдается.
Закон, который определяет направление протекания тепловых процессов, называется вторым началом термодинамики. Существует несколько формулировок второго начала термодинамики. Одну из них дал Клаузиус.
Невозможен самопроизвольный переход тепла от менее нагретого тела к более нагретому телу.

 ΔQ=ΔU
ΔQ=ΔU
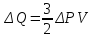
 ΔQ=A
ΔQ=A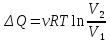
 ,
то
,
то