
tons2
.pdf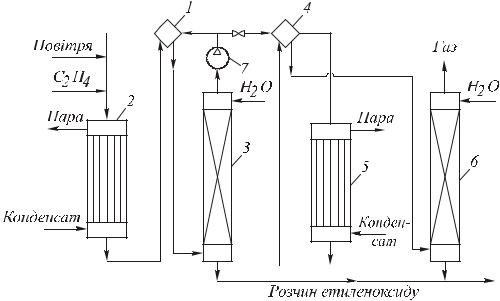
до більш повного використання етилену і кисню та знижує вибухонебезпечність сумішей завдяки їх розведенню азотом і диоксидом вуглецю.
Рис. 13. Технологічна схема одержання етиленоксиду окисненням етилену повітрям:
1, 4) теплообмінники; 2, 5) реактори; 3, 6) абсорбери; 7) компресор
Свіже повітря і етилен перед подачею на першу ступінь окиснення змішують із рециркулюючим газом цієї ступені. Газ із верху абсорбера 3 (після дотискання до робочого тиску) попередньо підігрівають у теплообміннику 1 газом з реактора 2. Суміш, що надходить у реактор 2, містить 4–6 % об. етилену, 6–8 % об. кисню і 8–10 % об. СО2; решта — азот та інертні домішки з вихідного етилену.
Процес у першому реакторі здійснюють при часі контакту 1–4 с і конверсії етилену 30–40 %, причому газ, що виходить з реактора, містить 1,5 % об. етиленоксиду. Тепло газу використовують у теплообміннику 1 і після додаткового охолодження направляють газ в абсорбер 3 першої ступені, де етиленоксид поглинається водою. Газ на виході з абсорбера розділяють на два потоки: основну частину повертають на першу ступінь окиснення, а решта йде на доокиснення – через теплообмінник 4 у реактор 5.
Оскільки газ після другої ступені скидають в атмосферу, у реакторі 5 підбирають такий режим, щоб отримати максимальний вихід етиленоксиду, тобто ведуть процес при значній конверсії етилену, що залишився, і при дещо зниженій селективності. Газ другої ступені, як і після першої, охолоджують у теплообміннику 4 і подають в абсорбер 6 другої ступені, де поглинається етиленоксид. Газ після цього абсорбера скидають в атмосферу, а розчини етиленоксиду (і СО2) з абсорберів 3 і 6 переробляють спільно, виділяючи чистий продукт. Загальний вихід α-оксиду 60 % по етилену при середній селективності ~ 65% і сумарній ступені конверсії етилену ~ 90 %.
Також в установках цього типу застосовують циркуляцію газу і після другої
21
ступені окиснення, а при великій потужності цеху стає вигідним триступінчасте окиснення із циркуляцією газу після кожного ступені. Цим шляхом можна довести вихід оксиду етилену до 65 %.
ОДЕРЖАННЯ ЕТИЛЕНОКСИДУ ОКИСНЕННЯМ ЕТИЛЕНУ КИСНЕМ
Окиснення етилену киснем є найбільш перспективним процесом синтезу етиленоксиду. Незважаючи на застосування більш дорогого кисню, переваги цього методу полягають у підвищенні селективності окиснення до 70–75 %, зниженні втрат етилену з газом, розведеним азотом повітря, що відходить, зменшенні габаритів апаратури.
При окисненні етилену киснем також здійснюють рециркуляцію газу після абсорбції з нього етиленоксиду, причому здійснюють реакцію при надлишку етилену відносно до кисню і при ступені конверсії етилену ~10 % за один прохід через реактор. Вміст інертних домішок в етилені і кисні незначний, тому для підтримки постійного складу суміші потрібно віддувати тільки невелику частину газу, що надає можливість роботи з одним реактором. Проте через утворення СО2 циркулюючий газ потрібно очищати від СО2, щоб зберегти його постійну концентрацію в рециркуляті.
Рециркулюючий газ дотискають до робочого тиску (~2 МПа), підігрівають у теплообміннику 2 за рахунок гарячого реакційного газу та змішують зі свіжим етиленом і киснем (рис.14). Отримана суміш, що надходить у реактор 1, містить 20–30 % об. етилену, 7–8 % об. кисню і 4–5 % об. СО2; решта – інертні домішки (N2, Аr тощо) з вихідних газів. Окиснення здійснюють у трубчастому реакторі 1 з охолодженням проміжним теплоносієм; у парогенераторі 3 продукується пара з тиском ~2 МПа. Гарячі реакційні гази, що містять 1,8–2 % об. етиленоксиду, охолоджують у теплообміннику 2, холодильнику 4 і подають в абсорбер 5, де поглинають водою весь етиленоксид і частину СО2. Газ після абсорбера розділяють на два потоки; один надходить на рециркуляцію, а інший – в абсорбер 6 на очищення від СО2 водним розчином карбонату калію:
К2СО3 + 3О2 + Н2О ↔ 2КНСО3
На холоді під тиском карбонат поглинає з газу СО2, і цей очищений газ повертають у реактор після дотискання компресором 7 до робочого тиску. Отриманий в абсорбері розчин підігрівають у теплообміннику 8 зворотним потоком абсорбенту, дроселюють і скеровують у десорбер 9, де при нагріванні відганяється СО2. Регенерований абсорбент насосом повертають через теплообмінник 8 в абсорбер 6.
22
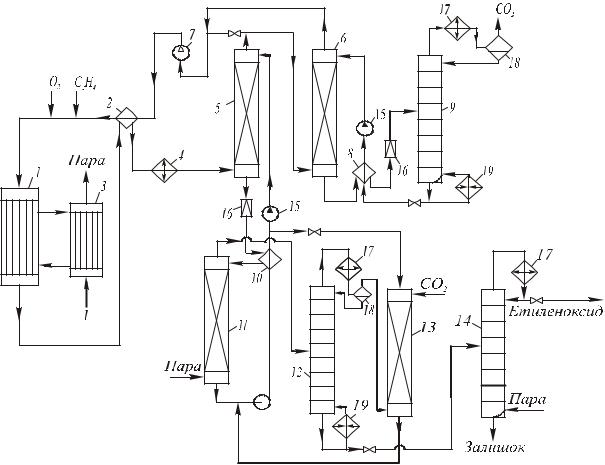
Рис. 14. Технологічна схема одержання етиленоксиду окисненням етилену киснем:
1)реактор; 2, 8, 10) теплообмінники; 3) парогенератор; 4) холодильник; 5, 6, 13) абсорбери;
7)циркуляційний компресор; 9) десорбер; 11) відпарна колона; 12, 14) ректифікаційні колони; 15) насоси;
16)дросельний вентиль; 17) конденсатори; 18) сепаратори; 19) кип’ятильники
Водний розчин етиленоксиду і СО2 з куба абсорбера 5 дроселюють до 0,5 МПа і через теплообмінник 10 подають у відпарну колону 11, де відганяються етиленоксид, СО2 і частина води. Основна маса води залишається в кубі, і після охолодження в теплообміннику 10 її повертають в абсорбер 5. Пари з відпарної колони 11 скеровують у ректифікаційну колону 12, де відганяють СО2 і частину етиленоксиду. Оксид поглинають із газу водою в абсорбері 13, повертаючи водний розчин у колону 11. Кубова рідина колони 12 надходить у ректифікаційну колону 14, де одержують чистий етиленоксид.
Виробництво етиленоксиду за допомогою цього методу має високу економічність і за показниками перевершує спосіб, заснований на застосуванні повітря. Здійснено ефективну систему утилізації тепла, відсутні шкідливі викиди в навколишнє середовище.
Диоксид вуглецю, що утворюється у вигляді побічного продукту, можна використовувати для виробництва карбаміду або сухого льоду.
23
ОДЕРЖАННЯ ПРОПІЛЕНОКСИДУ І СТИРОЛУ ХАЛКОН-МЕТОДОМ
Головне застосування Халкон-метод знайшов для одержання пропіленоксиду. Він реалізований у промисловості у двох варіантах: стирольному та ізобутеновому. У першому випадку сировиною є етилбензол і пропілен, які при участі кисню перетворюються в пропіленоксид і стирол:
С6Н5–СН2–СН3 + О2 → С6Н5–СН(СН3)ООН, С6Н5–СН(СН3)ООН + СН3–СН=СН2 → С6Н5–СНОНСН3 + СН3–СН–СН2О,
|_______|
С6Н5–СНОН–СН3 → С6Н5–СН=СН2
-Н2О
На синтез надходить 20–30 %-ий розчин гідропероксиду (ГП) в етилбензолі, що містить побічні продукти окиснення – метилфенілкарбінол і ацетофенон. Цей розчин змішують зі свіжим молібденовим каталізатором, рециркулюючими важкими продуктами зі стадії розділення, що містять каталізатор, і з надлишком пропілену. Отриману суміш скеровують у реакційний вузол 1 (рис. 15). Епоксидування здійснюють при 100–110 °С і тиску 2,5–3 МПа, що необхідний для підтримування суміші в рідкому стані. Щоб досягти більш повної конверсії гідропероксиду при високій питомій продуктивності і безпечних умовах роботи, реакційний вузол виконують у вигляді каскаду з декількох реакторів з мішалками, що охолоджуються водою (на схемі зображені два).
Продукти реакції скеровують у колону 2, де відганяється найбільш леткий пропілен, що повертається на епоксидування. Далі у колоні 3 у вигляді дистиляту одержують пропіленоксид, а кубовий залишок переганяють у вакуумній колоні 4, відокремлюючи важкий залишок, що містить каталізатор. Частину важкого залишку повертають на епоксидування, а решту спалюють або подають на регенерацію каталізатора. Дистилят колони 4 складається головним чином з етилбензолу, метилфенілкарбінолу і ацетофенону.
З цієї суміші після нейтралізації лугом (на схемі не зображено) спочатку відганяють у колоні 5 найбільш леткий етилбензол, що рециркулюють на синтез гідропероксиду. Кубовий залишок колони 5 надходить у випарник 6, де метилфенілкарбінол і ацетофенон у струмені перегрітої водяної пари випаровуються і відокремлюються від смол. Суміш парів, підігріта в теплообміннику 7 до 300 °С, послідовно проходить два реактори 8, заповнених гетерогенним каталізатором кислотного типу, і піддається дегідратації. Ця реакція ендотермічна, тому суміш, що охолола після першого реактора 8, підігрівають парою у теплообміннику 9. Сумарний ступінь конверсії метилфенілкарбінолу при дегідратації становить 90%.
Одержані пари охолоджують і конденсують у холодильнику 10, після чого водний шар відокремлюють від органічного в сепараторі 11. Вода знову йде на
24
одержання пари-розріджувача, чим створюється система замкнутого водообороту. Органічний шар містить стирол, ацетофенон і неперетворений метилфенілкарбінол. Із цієї суміші в колоні 12 відганяють стирол, що додатково очищують з одержанням продукту мономерної чистоти (на схемі не зображено). В кубі колони 12 залишаються ацетофенон і залишки метилфенілкарбінолу. Їх скеровують на установку гідрування, де ацетофенон перетворюється у метилфенілкарбінол:
С6Н5–СО–СН3 + Н2 → С6Н5–СНОН–СН3
Продукт гідрування повертають на стадію дегідратації.
Селективність перетворення пропілену в α-оксид досягає 95–97 %. Селективність по гідропероксиду на стадіях його синтезу і епоксидування становить 80–85 %, але завдяки корисному використанню побічних продуктів окиснення етилбензолу і розкладу гідропероксиду (метилфенілкарбінол і ацетофенон) вихід стиролу досягає 90 % по етилбензолу. При цьому на 1 т пропіленоксиду виходить 2,6–2,7 т стиролу.
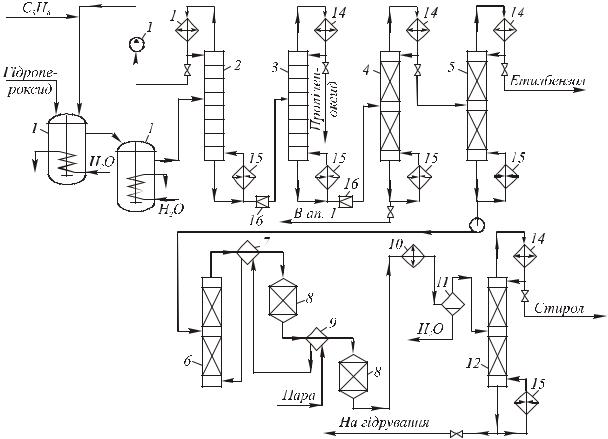
Рис. 15. Технологічна схема одержання пропіленоксиду і стиролу Халкон-методом:
1)реактори епоксидування; 2-5, 12) ректифікаційні колони; 6) випарник; 7, 9) теплообмінники;
8)реактори дегідратації; 10) холодильник; 11) сепаратор; 13) насос; 14) дефлегматори;
15)кип’ятильники; 16) дросельні вентилі
25
ДВОСТАДІЙНИЙ СИНТЕЗ АЦЕТАЛЬДЕГІДУ ПРИ ОКИСНЕННІ ЕТИЛЕНУ ПОВІТРЯМ
У цьому процесі важливо досягти відповідності між швидкостями окиснення етилену на PdCl2, окиснення відновленої форми паладію за допомогою СuС12 і окиснення Сu2С12 киснем. Найбільш повільною стадією є остання, тому каталізаторний розчин повинен містити надлишок мідних солей. Наприклад, хороші результати одержують зі слабким солянокислим розчином, що містить 0,3–0,5 % PdCl2 і 10–25 % СuС12, до якого для регулювання рН середовища додано 2–3 % ацетату міді. Із цим розчином всі стадії протікають досить інтенсивно при 100–130 °С, але для підтримки реакційної суміші в рідкому стані необхідний підвищений тиск (0,3–1 МПа), що одночасно сприяє інтенсифікації процесу.
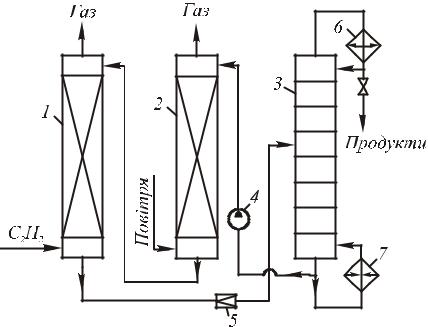
Рис. 16. Технологічна схема двостадійного синтезу ацетальдегіду при окисненні етилену повітрям:
1)реактор; 2) регенератор; 3) відпарна колона; 4) насос; 5) дросельний вентиль; 6) дефлегматор;
7)кип’ятильник
Реакційними апаратами є барботажні колони; їх для інтенсифікації масопереносу від газу до рідини іноді заповнюють насадкою. Через сильнокорозійні властивості середовища виконують реактори з титану або інших кислотостійких матеріалів. Вони не мають теплообмінних пристроїв, і реакційне тепло відводиться за рахунок підігріву холодних реагентів і випаровування. Процес розроблений у двох- і одностадійному варіантах.
У двостадійному варіанті окиснення етилену каталізаторним розчином і регенерацію останнього повітрям здійснюють у двох різних апаратах (рис. 16). У
26
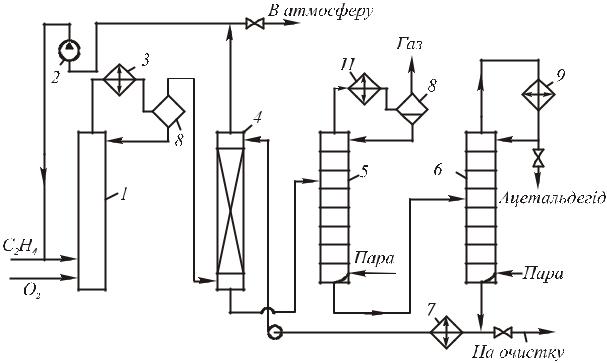
реактор 1 з кислототривкою насадкою подають етилен і регенерований каталізаторний розчин, причому реакцію ведуть до майже повної конверсії етилену при 0,8–0,9 МПа і 100–115 °С. Отриманий розчин ацетальдегіду у відновленому каталізаторному розчині дроселюють і скеровують у відпарну колону 3, де відганяють ацетальдегід і розчинені гази, що надходять на подальше розділення. Каталізаторний розчин з низу відпарної колони подають насосом при ~1 МПа у регенератор 2; туди вводять повітря, що окиснює йон металу до вищого валентного стану. Регенерований розчин повертають у реактор 1. Переваги цього варіанту – його безпека (через розділення стадій, у яких присутні етилен і повітря) і використання повітря як окисника.
ОДНОСТАДІЙНИЙ СИНТЕЗ АЦЕТАЛЬДЕГІДУ ПРИ ОКИСНЕННІ ЕТИЛЕНУ КИСНЕМ
В одностадійному методі окиснення етилену і регенерація каталізатора поєднані в одному апарату. Щоб уникнути утворення вибухонебезпечних сумішей, процес здійснюють у надлишку етилену, що повертають потім на реакцію. Це створює необхідність застосовувати як окисник не повітря, а технічний кисень, конверсія якого в реакторі повинна бути майже повною.
Рис. 17. Технологічна схема одностадійного синтезу ацетальдегіду при окисненні етилену киснем:
1)реактор; 2) циркуляційний компресор; 3) холодильник; 4) абсорбер; 5) відпарна колона;
6)ректифікаційна колона; 7) холодильник; 8) сепаратори; 9) дефлегматори
27
У реактор 1 типу пустотілої барботажної колони, що заповнена каталізаторним розчином, подають кисень і етилен (свіжий і рециркулюючий) (рис. 17). Реактор працює з постійним рівнем рідини при 130 °С і ~0,3 МПа. Надлишковий етилен видуває з розчину ацетальдегід, що утворився, чим запобігають побічним реакціям його конденсації. Разом з ацетальдегідом випаровується частина води, що конденсується в холодильнику 3 і повертається в реактор.
Газопарову суміш скеровують в абсорбер 4, де ацетальдегід поглинають водою, що зрошує насадку абсорбера. Основну кількість залишкового газу, що містить етилен, трохи кисню та інертні домішки, повертають на окиснення, дотискаючи її циркуляційним компресором 2. Меншу частину газу виводять з установки, щоб уникнути надмірного нагромадження у ньому інертних домішок. Водний розчин ацетальдегіду з куба абсорбера 4 надходить у відпарну колону 5, де відганяють розчинені гази і леткі домішки. Далі у колоні 6 у вигляді дистиляту одержують ацетальдегід, а більшу частину кубової рідини, що містить менш леткі побічні продукти (кротоновий альдегід тощо), повертають після охолодження на абсорбцію. Частину цієї рідини виводять у систему очищення стічних вод.
У порівнянні із двостадійним процесом одностадійний синтез ацетальдегіду дає економію у капіталовкладеннях та витраті енергії, але пов'язаний із застосуванням більш дорогого окисника (кисень).
СИНТЕЗ ВІНІЛАЦЕТАТУ З ЕТИЛЕНУ
Даний метод полягає у окисному приєднанні оцтової кислоти до етилену:
СН2=СН2 + СН3СООН + 0,5О2 → СН2=СН–ОСОСНз + Н2О
Газофазний синтез вінілацетату здійснюють із гетерогенним каталізатором (Pd на SiО2, Аl2О3 або на алюмосилікаті з добавкою ацетату натрію), у якому роль мідних солей виконує носій, що сприяє окисненню Pd у двовалентну форму:
Pd + 0,5О2 + 2СН3–СООН → Pd2++ Н2О + 2СН3–СОО-
Pd2+ + СН2=СН2 + СН3–СООН → Pd + СН2=СН–ОСО–СН3 + 2Н+
Процес здійснюють при 170–180 °С і 0,5– 1 МПа, пропускаючи парогазову суміш реагентів через гетерогенний каталізатор. Щоб уникнути утворення вибухонебезпечних сумішей, застосовують надлишок етилену і оцтової кислоти. При цьому неперетворений етилен повертають на окиснення, що робить обов'язковим використання як окисника не повітря, а кисню. Вихідна суміш складається з етилену, парів оцтової кислоти і кисню в об'ємному відношенні
28
~8:4:1. Їх конверсія за один прохід через реактор становить відповідно 10, 20 і 60–70 %. Селективність за вінілацетатом досягає 91–92 %, а основним побічним продуктом є СО2 з утворенням тільки 1 % інших речовин (етилацетат, етилідендиацетат).
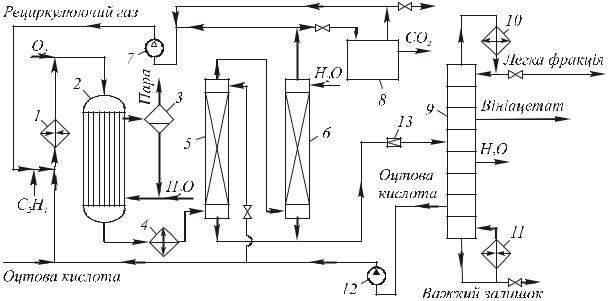
Рис. 18. Технологічна схема синтезу вінілацетату з етилену:
1) паровий нагрівач; 2) реактор; 3) парозбірник; 4) холодильник; 5, 6) скрубери; 7) циркуляційний компресор; 8) блок карбонатного очищення від СО2; 9) система ректифікаційних колон; 10) дефлегматор;
11) кип’ятильник; 12) насос; 13) дросельний вентиль
Суміш свіжих і рециркулюючих етилену і оцтової кислоти підігрівають у паровому нагрівачі 1, змішують зі свіжим киснем і подають у трубчастий контактний апарат 2 зі стаціонарним шаром каталізатора, що перебуває в трубах. Тепло, що виділяється, відводять за рахунок випаровування (у міжтрубному просторі) водного конденсату; при цьому виробляють пару, яку відокремлюють в збірнику 3. Реакційну суміш охолоджують у холодильнику 4 і промивають газ послідовно в скруберах 5 і 6 рециркулюючою оцтовою кислотою і водою для вловлювання відповідно вінілацетату та оцтової кислоти. Більшу частину промитого газу повертають циркуляційним компресором 7 на синтез, але частина його проходить блок 8 карбонатного очищення від СО2. Очищений газ здебільшого рециркулює, але деяку його кількість виводять із системи, щоб уникнути надмірного нагромадження інертних домішок, що містяться в етилені і кисні. Суміш рідких продуктів з куба скруберів 5 і 6 подають на розділення у систему ректифікаційних колон 9, де відокремлюються вінілацетат, вода, оцтова кислота і важкі домішки, що скеровують на спалювання.
29

ОСНОВНІ ХАРАКТИРИСТИКИ І УМОВИ ПРОВЕДЕННЯ ПРОЦЕСІВ
№ |
Назва процесу |
Окисник |
Каталізатор |
Цільові |
Побічні |
Т, °С |
Тиск, |
Конверсія, |
Селектив- |
|
п/п |
(ініціатор) |
продукти |
продукти |
МПа |
% |
ність, % |
||||
|
|
|
||||||||
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
мурашина |
|
|
|
|
|
|
Кумольний метод одержання |
|
гідроперо- |
|
кислота, |
|
|
|
|
|
1 |
повітря |
ксид |
фенол, |
формальдегід, |
105 – 120 |
~ 0,4 |
|
|
||
фенолу і ацетону |
ізопропіл- |
ацетон |
фенольна |
|
|
|||||
|
|
|
|
|
|
|||||
|
|
|
бензолу |
|
смола, α– |
|
|
|
|
|
|
|
|
|
|
метилстирол |
|
|
|
|
|
2 |
Окиснення легкої фракції |
повітря |
|
|
|
170 – 200 |
5 |
~ 70 |
~ 60 |
|
прямогонного бензину |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
||
3 |
Окиснення твердого парафіну |
повітря |
KMnO4 |
вищі жирні |
нижчі кислоти |
105 – 130 |
атм. |
30 – 35 |
|
|
кислоти |
|
|||||||||
|
|
|
|
|
|
|
|
|
||
|
Окиснення циклогексану у суміш |
|
|
циклогексан |
естери, |
|
|
|
|
|
|
|
нафтенат |
ол, |
|
|
|
|
|||
4 |
повітря |
дикарбонові |
145 – 150 |
4 |
~ 4 |
~ 78 |
||||
анолу та анону |
кобальту |
циклогексан |
||||||||
|
|
кислоти |
|
|
|
|
||||
|
|
|
|
он |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
||
|
Окиснення циклододекану в |
|
|
циклододека |
|
|
|
|
|
|
5 |
повітря |
Н3ВО3 |
нол, |
естери борної |
150 – 200 |
атм. |
30 – 35 |
90 |
||
присутності борної кислоти |
циклододека |
кислоти |
||||||||
|
|
|
|
|
|
|
||||
|
|
|
|
нон |
|
|
|
|
|
|
|
Окиснення циклогексанолу в |
|
оксид міді, |
|
оксиди азоту, |
60 – 80 |
|
|
|
|
|
азотна |
адипінова |
(І стадія), |
|
|
|
||||
6 |
метаванадат |
дикарбонові |
0,3 – 0,5 |
вихід 90 – 95 |
||||||
адипінову кислоту |
кислота |
кислота |
100 – 120 |
|||||||
|
амонію |
кислоти |
|
|
|
|||||
|
|
|
|
(ІІ стадія) |
|
|
|
|||
|
|
|
|
|
|
|
|
|
||
7 |
Виробництво |
повітря |
солі |
диметилтере |
ксилол |
140 – 180 |
0,6 – 1 |
вихід 85 – 90 |
||
диметилтерефталату |
кобальту |
фталат |
||||||||
|
|
|
|
|
|
|
||||
|
Одностадійний синтез |
|
кобальт- |
терефталева |
карбоксибен- |
|
|
|
|
|
8 |
повітря |
бромідний |
125 – 275 |
до 4 |
|
|
||||
терефталевої кислоти |
кислота |
зилальдегід |
|
|
||||||
|
|
каталізатор |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
||
|
|
|
|
оцтова |
етилацетат, |
|
|
|
|
|
|
Сумісне одержання оцтової |
|
|
формальдегід, |
|
|
|
|
||
|
|
ацетати міді і |
кислота, |
|
|
|
|
|||
9 |
повітря |
оцтовий |
50 – 70 |
0,4 |
вихід 95 |
|||||
кислоти і оцтового ангідриду |
кобальту |
оцтовий |
||||||||
|
|
ангідрид, |
|
|
|
|
||||
|
|
|
|
ангідрид |
|
|
|
|
||
|
|
|
|
ацеальдегід |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
||
