
6_спирты,_фенолы
.pdf
55
H3C O
O CH3 + HI
CH3 + HI  H3C
H3C OH + H3C
OH + H3C I
I
|
|
|
O CH3 + HI |
|
t |
|
H3C |
|
|
|
+ CH3I |
|
|
|
||||||
H3C |
|
|
|
|
OH |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
+2HI |
|
t |
|
H3C |
|
I + CH3I |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
OR HX (k) |
|
OH |
+ RX ; |
|
|
|
OCH3 HI (k) |
|
|
OH |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ CH3I |
||
|
|
|
|
t |
|
|
|
|
|
|
|
120-180 C |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
3. Галогенирование.
Благодаря способности эфирного атома кислорода облегчать образование свободного радикала в -положении простые эфиры легко вступают в реакции радикального хлорирования.
Cl2, h 20 C
H3C O
O CH3
CH3  H3C
H3C O
O CH3 + HCl
CH3 + HCl
Cl
-хлордиэтиловый эфир
Применение.
Диэтиловый эфир. Этоксиэтан. Называют его чаще всего эфиром, серным эфиром. Летучая подвижная жидкость со своеобразным запахом. Легко воспламеняется. Нашел наибольшее применение в медицине более 150 лет для ингаляционного наркоза, растираний и приготовления настоек и экстрактов. Промышленность выпускает эфир для наркоза, обычно стабилизированный антиоксидантами, и эфир медицинский для наружного применения. При хранении на воздухе легко образует взрывчатый гидропероксид.
О2, воздух
H3C O
O CH3
CH3  H3C
H3C O
O CH3
CH3
O O H
Гидропероксиды легко взрываются. Поэтому, перед употреблением эфира следует убедиться в отсутствии в нём гидропероксидов (проба с раствором йодида калия в разбавленной уксусной кислоте: появление желтой окраски свидетельствует о наличии пероксидов).
Фенолы
Фенолами называются производные аренов, в которых один или несколько атомов водорода ароматического кольца замещены на гидроксильные группы. По числу гидроксильных групп в ароматическом кольце различают одно- и многоатомные (двух- и трёхатомные) фенолы. Для большинства фенолов используются тривиальные названия. Структурная изомерия фенолов связана с различным положением гидроксильных групп.
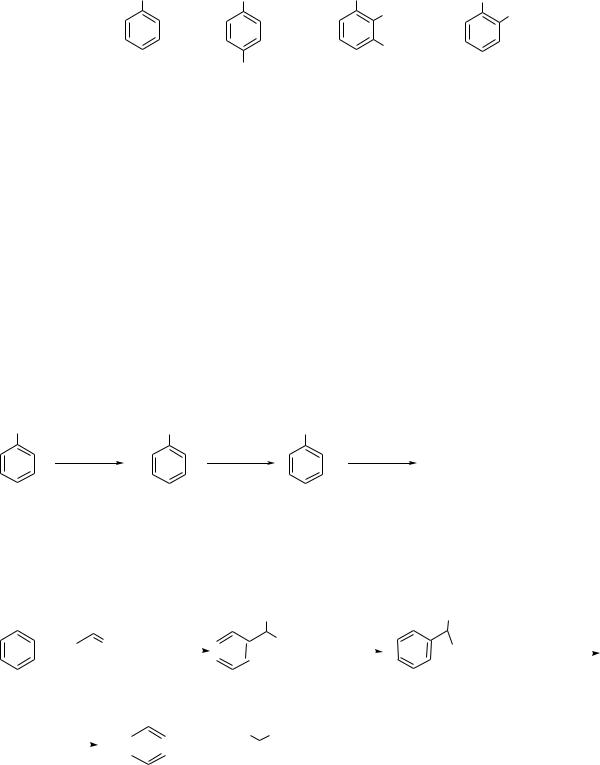
OH
фенол
56
OH |
OH |
OH |
|
OH |
CH3 |
|
OH |
|
OH |
|
|
п-гидрохинон |
пирогаллол |
о-крезол |
о-пирокатехин |
|
|
м-резорцин |
|
|
Фенол твердое вещество, с характерным запахом, вызывает ожоги при попадании на кожу. Ядовит. Растворяется в воде, его раствор называют карболовой кислотой (антисептик). Она была первым антисептиком, введённым в
хирургию. Широко используется для производства пластмасс, лекарственных средств (салициловая кислота и её производные), красителей, взрывчатых веществ.
Способы получения
1. Выделение из каменноугольной смолы.
Каменноугольную смолу, образующуюся при коксовании угля, перегонкой разделяют на фракции, одной из которых является карболовое масло (175 - 210 С). Это масло подвергают непрерывной экстракции раствором щелочи. Извлечённые соли разлагают диоксидом углерода и перегоняют.
OH |
ONa |
OH |
NaOH |
CO2 |
перегонка |
- H2O
экстракция
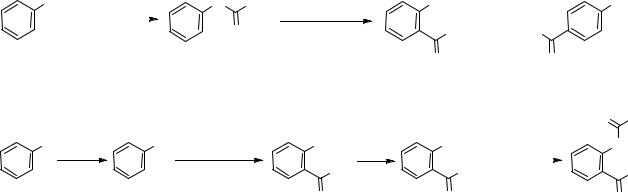
2. Кумольный способ.
Преимущества метода: безотходная технология (выход полезных продуктов > 99%) и экономичность. В настоящее время кумольный способ используется как основной в мировом производстве фенола.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
CH3 |
|||||||
|
|
|
|
CH2 |
|
H+ |
|
|
|
|
|
|
|
|
CH |
O2 |
|
|
O |
|
OH H2SO4 |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||
+ |
|
|
|
|
|
|
3 |
|
|
|
CH3 |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
CH3 |
|
|
|
|
|
|
|
|
|
90 - 130 C |
50-90°C |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
кумол |
|
|
гидропероксид |
||||||||||||
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
кумола |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
+ |
|
H3C |
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
фенол |
|
|
ацетон |
|
|
|
|
|
|
|
|
|
|||||||||||
3. Сплавление солей сульфокислот со щелочами.
Наиболее старый способ получения фенола. Основными недостатками этого способа являются жесткие условия процесса и большое количество отходов, загрязняющих окружающую среду.
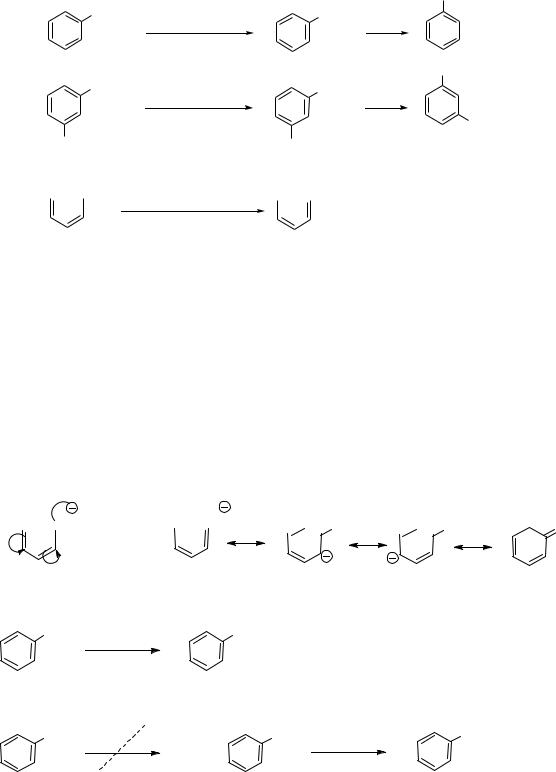
|
57 |
|
|
|
OH |
SO3Na 2NaOH, 350 C |
ONa |
H+ |
- Na2SO3 |
|
|
|
|
OH |
SO3Na 4NaOH, 350 C |
ONa |
H+ |
- Na2SO3 |
|
OH |
SO3Na |
ONa |
резорцин |
4. Гидролиз хлорбензола.

 Cl 10-15 %NaOH, 350 C
Cl 10-15 %NaOH, 350 C 
 OH
OH
300 атм.
Химические свойства
Реакционными центрами в молекуле фенола является фенольная гидроксильная группа и ароматическое кольцо, взаимовлияющие друг на друга.
-Фенольная -ОН за счёт p, -сопряжения с кольцом является донором;
-Это обуславливает дефицит электронной плотности на атоме кислорода, в результате чего протон гидроксильной группы фенолов более подвижен, чем в спиртах, т.е. увеличиваются кислотные свойства;
Кислотность фенолов выше, чем спиртов, поскольку феноксид-ион в результате мезомерной делокализации отрицательного заряда стабильнее алкоксид-ионов:

 O
O 
 O
O 
 O
O 
 O
O  O
O
или
феноксид-ион
Повышенная кислотность фенолов проявляется в их способности взаимодействовать с растворами щелочей:
OH |
NaOH |
ONa |
|
феноксид Na |
|
|
|
- H2O
Однако фенол не реагирует с гидрокарбонатом натрия (фенол слабее, чем угольная кислота).
OH |
NaHCO3 |
ONa CO2, H2O |
OH |
|
; |
|
|
|
|
|
|
|
|
- NaHCO3 |
|
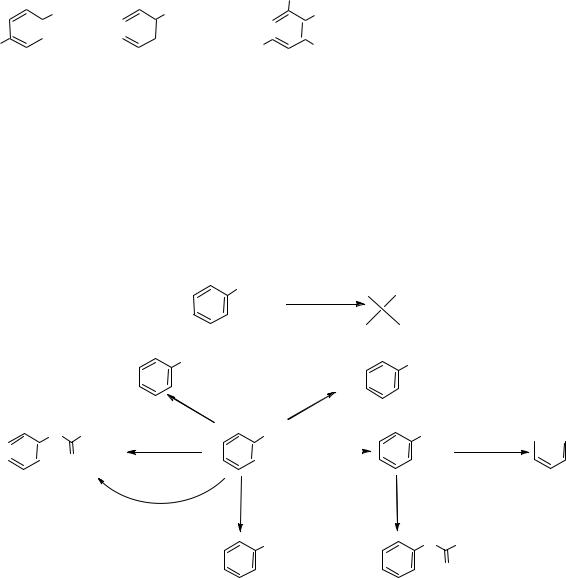
-За счёт +М эффекта существенно изменены характеристики связи САР-О, а именно появляется некоторая двоесвязанность, что приводит к увеличению её прочности и укорочению в сраванении с С-О в спиртах. Поэтому реакции, связанные с разрывом связи САР-ОН, встречается у фенолов редко.
-Благодаря электронодонорному эффекту влиянию фенольного гидроксила электронная плотность ароматического кольца повышена по сравнению с
58
бензолом в орто- и пара-положениях. Реакции электрофильного замещения протекают легче, чем у бензола.
Заместители в ароматическом кольце в значительной степени влияют на кислотность фенолов. Электродонорные заместители (ОСН3, NH2) несколько снижают кислотность, тогда как электроакцепторные (NO2) сильно её увеличивают.
|
|
|
|
|
|
|
|
|
NO2 |
|
|
|
|
|
OH |
|
|
|
|
OH |
|
|
OH |
HNO3 |
pKa ~ - 1.64 |
|
|
< |
|
|
|
|
< |
|
|
|
||
|
|
|
|
|
|
|
|
|
CH3COOH pKa ~ 4.76 |
|||
|
|
|
|
|
|
|
||||||
H2N |
|
|
|
|
|
O2N |
|
NO2 HCl |
pKa ~ -7 |
|||
pKa 10.5 |
pKa 10 |
pKa 0.8 |
|
|
||||||||
2,4,6-тринитрофенол (пикриновая кислота)
1. Реакции по ОН-группе.
Реакции образования сложных эфиров, простых эфиров идут труднее, чем у спиртов и поэтому фенол надо превратить в фенолят. Реакции с HX, RCOOH, SOCl2 нет.
1) HX
OH 2) RCOOH 3) SO2Cl
трифенилфосфат- |
мало! |
|
||
основной продукт! |
|
|||
Cl |
|
|||
|
|
|
|
|
(C6H5O)3P=O + 4 HCl + |
|
|||
|
|
|
P |
|
|
|
|
C |
|
|
|
|
|
l |
|
|
|
|
5 |
|
|
O CH3 |
CH3COCl |
|
|
|
|
|
|
|
|
O |
- HCl |
|
|
|
|
||
|
|
|
|
|
|
|
|
(CH3CO)2O, t |
|
Zn
- CH3COOH
|
|
|
|
|
|
|
|
|
|
|
т |
|
|
|
|
|
|
|
|
|
|
|
а |
|
|
|
|
|
|
|
|
|
|
ф |
|
|
|
|
|
|
|
|
|
|
ь |
|
|
|
|
|
|
|
|
|
л |
|
|
||
|
|
|
|
|
|
у |
|
|
|
||
|
|
|
|
|
с |
|
|
|
, |
||
|
|
|
|
л |
|
|
|
|
|||
|
|
|
|
и |
|
|
|
O2 |
|||
|
|
|
|
|
|
S |
|
||||
|
|
|
т |
|
|
|
|
|
|||
|
|
|
е |
|
|
|
) |
|
|
||
|
|
м |
|
O |
2 |
|
|||||
и |
|
H3 |
|
|
|
|
|||||
д |
|
|
|
|
|
|
|||||
|
|
|
C |
|
|
|
|
|
|
H |
|
|
|
|
( |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
a |
|
|
|
|
OH |
|
|
N |
|
|
||||
|
|
|
|
|
NaOH |
||||||
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
- NaCl
OCH3
+ CH3OSO3Na
ONa CH3J 
 OCH3
OCH3
-NaJ
CH3COCl метилфениловый эфир (анизол)
H |
O CH3 |
O
фенилацетат
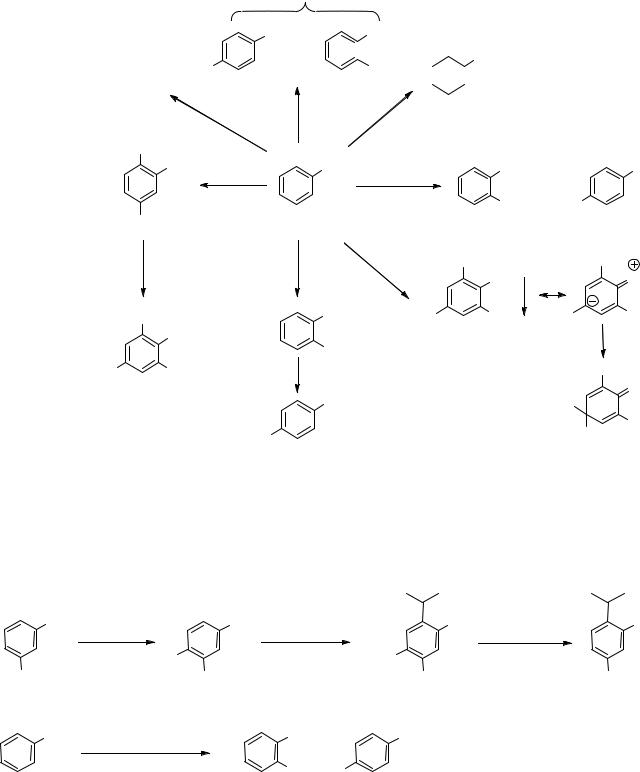
2. Реакции по ароматическому кольцу.
Фенольная гидроксильная группа является электродонором и одним из сильнейших ориентантов I рода. Она значительно облегчает протекание типичных реакций электрофильного замещения по сравнению с бензолом, но и позволяет проводить специфические для фенолов реакции.
59
фенолформальдегидные смолы
|
|
OH |
|
|
+ |
|
HOH2C |
|
фиолетовое Fe(OAr)3 |
|
|
окрашивание |
Fe 3+ |
+ |
|
|
H2CO, H |
|
OH |
|
|
OH 2-гидроксибензиловый спирт |
||||
|
CH2OH |
|
OH |
||
|
|
||||
|
|
циклогексанол |
|||
|
H |
|
|
|
|
3 |
2 |
|
p |
|
|
|
|
|
|
||
|
, |
|
|
||
|
|
t |
|
|
|
|
|
, |
|
|
|
|
i |
|
|
|
|
|
N |
|
|
|
|
SO3H |
2 H SO |
OH 20% HNO (p) |
OH |
OH |
|
|
3 |
|
|
||
|
2 |
4 |
|
|
+ |
|
|
|
|
|
|
SO3H |
100°C |
0 - 5°C |
NO2 |
O2N |
|
|
|
о-нитрофенол |
п-нитрофенол |
||
|
|
|
|||
|
|
|
H |
|
B |
Br |
|
|
Br |
|
|
|
|
|
r |
|
|
|
|||
|
3 HNO3(k), |
H2SO4, |
20°C 2 |
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|||
|
H2SO4, 100°C |
O |
|
|
OH |
|
|
OH |
||
|
|
2 |
|
|
|
|||||
|
|
|
|
, |
|
|
|
|
|
|
|
|
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
° |
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
NO2 |
|
OH |
|
|
Br |
Br |
Br |
|
Br |
|
OH |
|
|
|
|
качеств. реакция |
|
Br2 |
||
|
|
|
SO3H |
|
|
|||||
|
|
|
|
белый цвет! |
|
|
|
|||
O2N |
NO2 |
100°C |
|
|
|
|
Br |
|
||
|
|
|
-4 |
моль/л |
|
|
||||
|
|
|
|
|
|
|||||
|
|
|
|
|
|
чувств.: 10 |
|
|
O |
|
пикриновая |
|
|
|
|
|
|
|
|
||
|
OH |
|
|
|
|
Br |
|
|
||
|
кислота |
|
4-гидроксибензол |
желтый |
|
Br |
||||
|
|
|
сульфоновая к-та |
тетрабром Br |
||||||
|
|
HO3S |
|
|||||||
|
|
|
|
|
|
фенол |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Алкилирование фенолов в условиях реакции Фриделя-Крафтса затруднено тем, что кислоты Льюиса образуют с НПЭ атома кислорода нереакционноспособный донорно-акцепторный комплекс. Однако фенолы могут алкилироваться спиртами и алкенами в присутствии серной или фосфорной кислот.
избежать полиалкилирования можно введением Э.А. группы -SO3H, которая затем легко удаляется
OH |
H SO |
4 |
OH (CH ) CHOH |
OH H O > 100 C |
OH |
|
|
2 |
3 2 |
|
2 |
|
|
|
|
HO3S |
H2SO4 |
HO3S |
H2SO4 |
|
CH3 |
|
CH3 |
|
CH3 |
|
CH3 |
|
|
|
|
|
|
тимол |
|
|
|
|
|
(антисептик) |
|
OH |
1) ROH/ H2SO4 |
OH |
OH |
|
|
|
|
+ |
|
|
|
||
|
|
|
|
|
|
|
|
2) R'CH=CH2/ H2SO4 |
R |
R |
|
|
|
выход невелик! конкурирует полиалкилирование! смесь: моно-, ди-, триалкил фенолов
Ацилирование фенолов хлорангидридами или ангидридами карбоновых кислот по Фриделю-Крафтсу нередко осложняется образованием нерастворимых фенолятов алюминия ArO-AlCl2. Поэтому используют непрямое ацилирование
60
(перегруппировка Фриса – миграция ацильной группы сложных эфиров фенолов при их взаимодейцствии с хлоридом алюминия в соотношении 1:1).
OH CH3COCl |
O CH3 |
AlCl3 |
OH |
+ |
OH |
|
O |
перегрупп. |
CH3 |
H3C |
|
|
|
||||
|
|
Фриса |
O |
|
O |
|
|
|
|
Карбоксилирование. Реакция Кольбе-Шмитта (1860 г). При действии диоксида углерода на твёрдые феноксиды щелочных металлов образуются фенолкислоты.
|
|
|
|
O |
CH3 |
OH Na |
ONa CO2 |
OH H+ |
OH (CH3CO)2O |
O |
|
|
125 C, 5 атм. |
ONa |
OH |
|
OH |
|
|
O |
O |
|
O |
|
|
салицилат |
салициловая |
аспирин |
|
|
|
натрия |
кислота |
(ацетилсалиц. к-та) |
|
|
|
|
|
в природе нет! |
|
