
Биофизика 02
.pdf
зображення АF і ВFформ ДНК — на рис. 3.27.
АF, ВF і СFформи ДНК є правими. У 1978 р. була отримана ліва спіраль ДНК — молекула синтетичного полімеру поліFдезоксіFГЦ. Його сахарофосфатний кістяк має зигзагоподібний вигляд. Тому така конформація ДНК одержала назву ZFформа. ZFформа може бути енергетично вигідна тільки в тому випадку, якщо ланцюг ДНК, утворений чергуванням пуринових і піримідинових азотистих основ, наприклад,
—Г і Ц. Таким чином одиницею, що повторюється в такій структурі, є дві пари нуклеотидів:
ZFформа має 12 пар основ на виток спіралі, тобто поворот пар основ дорівнює 30°.
Для будьFякої конформації ДНК, крім ZFформи, характерна наявність широкої і вузької борозенки на поверхні спіралі.
Молекула рибонуклеїнової кислоти (РНК) також, як і ДНК, утворена певною послідовністю нуклеотидів, але частіше усього складається з одного ланцюга. Молекула цукру в ній подана рибозою, і замість тиміну в її склад входить піримідинова основа — гуанін. Під час синтезу матричної РНК (транскрипції) генетична інформація, що міститься на певній ділянці ДНК, за принципом комплементарності переходить на РНК, на якій, як на матриці, в рибосомах відбувається синтез білка (трансляція). Приєднання потрібних амінокислот до поліпептидного ланцюга, що синтезуються, здійснюється за допомогою транспортної РНК. У такий спосіб РНК є посередником між ДНК і білком, а в деяких вірусах — носієм генетичної інформації.
Різні конформації полінуклеотидного ланцюга досягаються завдяки можливості поворотів навколо деяких зв’язків (рис. 3.28). Конформація нуклеїнових кислот значною мірою визначається конформацією дезоксирибози в ДНК або рибози в РНК.
Молекула вуглеводу є циклічною. У залежності від того, який з атомів вуглецю (С2’ або С3’) знаходиться поза площиною інших чотирьох атомів, розрізняють наступні конформації. Якщо атом С2’ або С3’ знаходиться з того ж боку від площини, що й атом С5’, то така конформація називається ендоF, якщо з іншого боку, то
—екзоFконформація. Отже, можливі чотири випадки: С2’Fендо, С3’FендоF, С2’FекзоF та С3’FекзоFконформації (рис. 3.29). У залежності від конформації вуглеводу, розрізняють два сімейства конформацій ДНК: АFсімейство (С3’FендоFконформація, АFформа ДНК) і
ВFсімейство (С2’FендоFконформація, ВF, СF і ТFформи ДНК). На рисунку 3.29 видно, що в С2’FендоF і С3’FекзоFконформаціях кут ϕ невеликий (складає 2–6°), тому у ВFсімействах ДНК нуклеотидні пари розташо-
вані майже перпендикулярно до осі спіралі, для С3’FендоFконформації ϕ = 20°. Конформаційні переходи ДНК усередині одного сімейства
71
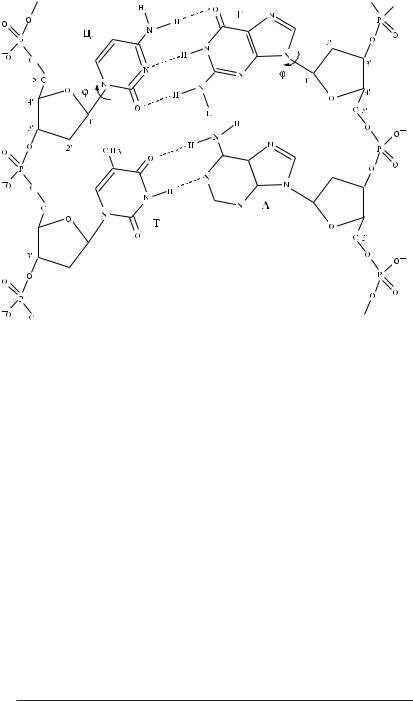
Рис. 3.26. Ділянка ланцюга ДНК ( ϕ – кут між перпендикуляром до осі спіралі і площиною
основ).
здійснюються плавно, а перехід з АF у ВFсімейство — стрибкоподібно, супроводжуючись зміною конформації вуглеводу від С3’Fендо до С2’Fекзо.
Молекули ДНК є найбільшими в природі. Наприклад, кільцеві ДНК
|
|
|
|
|
|
Табл. 3.1 |
Геометричні характеристики ДНК у різних формах |
||||||
|
|
|
|
|
|
|
|
Воло- |
Число |
Крок |
Пере- |
Пово- |
Кут ϕ між перпен- |
|
гість, % |
ланок |
спіралі, |
міщення |
рот на |
дикуляром до осі |
Сіль ДНК |
|
на виток |
нм |
на один |
нуклео- |
спіралі і площи- |
|
|
спіралі |
|
нуклео- |
тид, |
ною основ |
|
|
|
|
тид, нм |
град. |
|
|
|
|
|
|
|
|
Na, АFформа |
75 |
11 |
2,82 |
0,255 |
32,7 |
20 |
|
|
|
|
|
|
|
Na, ВFформа |
92 |
10 |
3,46 |
0,346 |
36 |
2 |
|
|
|
|
|
|
|
Li, ВFформа |
66 |
10 |
3,37 |
0,337 |
36 |
2 |
|
|
|
|
|
|
|
Li, СFформа |
66 |
9,3 |
3,10 |
0,332 |
39 |
6 |
|
|
|
|
|
|
|
72
фага Т2 мають довжину 49 мкм, а ДНК E. coli — 400 мкм, молекулярна маса останньої складає 109. Кожна хромосома містить тільки одну молекулу ДНК, що має довжину від кількох міліметрів до кількох сантиметрів. Сумарна довжина всіх молекул ДНК однієї клітини людини
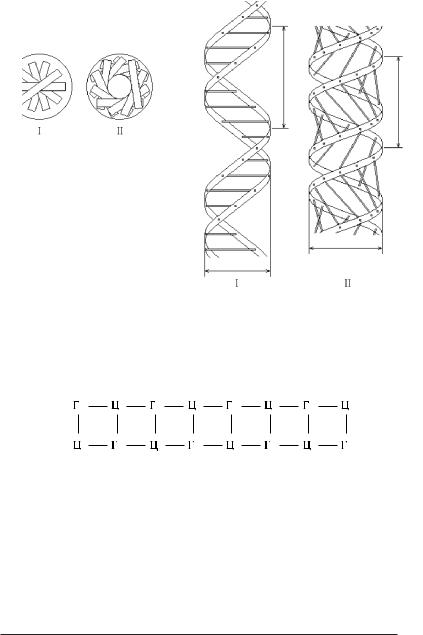
Рис. 3.27. Схема будови А[ і В[форм ДН. І – В[форма, ІІ – А[форма; а – вигляд
зверху, б – вигляд збоку.
В В[формі центри ваги пар основ знаходяться на осі спіралі, а в А[формі зсунуті
до периферії, тому в центрі залишається отвір біля 4 нм.
складає біля двох метрів.
Величезні розміри молекул нуклеїнових кислот вимагають їхньої особливої укладки в межах малих розмірів клітин або вірусів. Це досягається за рахунок можливості утворення в молекулі ДНК перегинів, петель, суперспіралей, що формує її третинну структуру.
Особлива будова молекули ДНК — щільна упаковка азотистих основ, зв’язаних сильними і слабкими взаємодіями — забезпечує високу схоронність генів навіть при значних варіаціях умов навколишнього середовища. Комплементарні пари основ зв’язані одна з одною водневими зв’язками, що відносяться до слабких взаємодій. Наприклад, для Г–ЦFпар енергія зв’язку Есв складає усього лише 5 кДж/моль, а константа дисоціації К, відповідно до рівняння Больцмана:
73
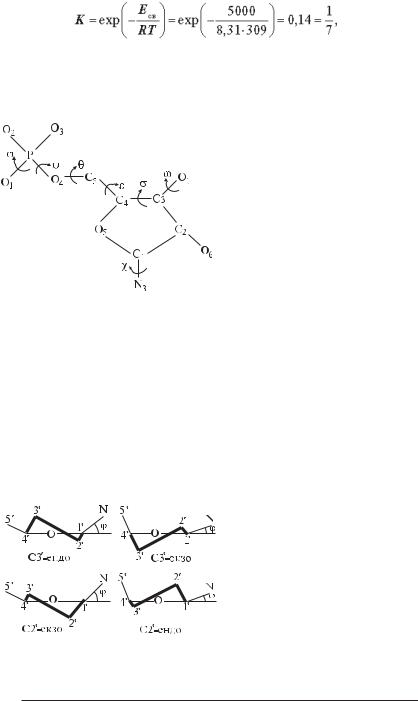
тобто в одномолярному розчині на кожні сім пар основ приходиться одна розірвана. Для двох пар основ константа дисоціації складає (1/7)2 = 1/49. Для ланцюга з кількох тисяч пар нуклеотидів константа дисоціації вже настільки мала, що рівновага майже цілком зміщена убік утворення
|
комплексів пар основ. |
|
|
Вторинна структура ДНК |
|
|
є стабільною лише у певних |
|
|
умовах. Зміни температури, |
|
|
розчинника, рН, іонного складу |
|
|
середовища можуть привести |
|
|
до руйнації слабких водневих |
|
|
зв’язків між парами нуклеотидів |
|
|
і утворенню замість подвійної |
|
|
спіралі ДНК або двоспіральних |
|
|
ділянок РНК окремих нуклео- |
|
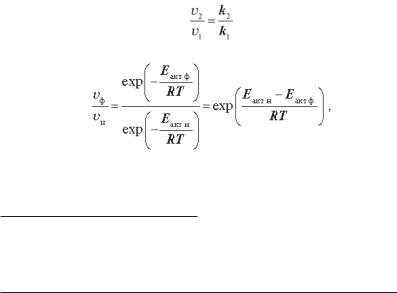
Рис. 3.28. Кути повороту в ланці полінуклео- |
тидних ланцюгів, що зверта- |
|
ються в клубок. Цей процес |
||
тидного ланцюга. |
||
|
називають денатурацією або |
плавленням нуклеїнових кислот.
Упроцесі плавлення ДНК відбувається зменшення в’язкості розчину,
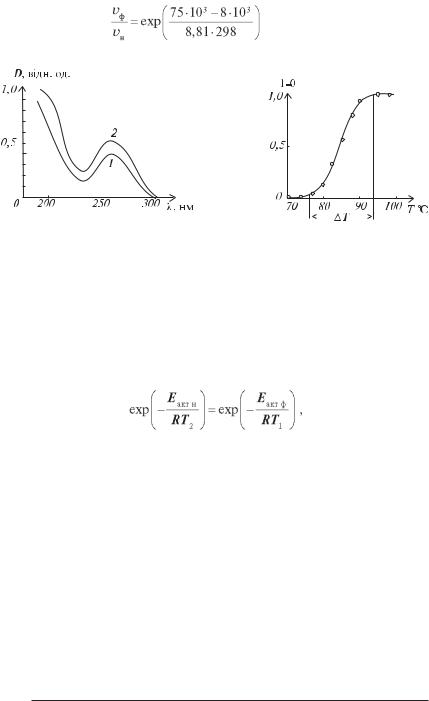
вобласті максимального поглинання (260 нм) — збільшення оптичної густини (гіпохромізм). Тому явище плавлення легко виявити по спектру поглинання ДНК (рис. 3.30). Зміна поглинання ДНК при переході спіраль–клубок дає кількісну оцінку спіральності ДНК1.
ДНК характеризується не визначеною температурою плавлення, а деяким температурним інтервалом, у якому відбувається перехід спі- раль–клубок. SFобразний вигляд кривої плавлення (рис. 3.31) свідчить про кооперативність цього процесу.
Рис. 3.29. Чотири найбільш стійкі конформації цукрового кільця в нуклеотиді.
74
Температура плавлення подвійної спіралі ДНК залежить від співвідношення АТF і ГЦFпар. Аденін зв’язаний із тиміном двома водневими зв’язками, а гуанін із цитозином — трьома. Тому, чим більше в складі ДНК ГЦFпар, тим вища її температура плавлення. Так, для синтетичного полімеру поліFАТ температура плавлення складає 65 °С, а для поліFГЦ уже —104 °С.
Значення температури плавлення нуклеїнових кислот залежить також від концентрації катіонів у розчині: чим вона вища, тим вища температура плавлення (залежність близька до логарифмічної). Це пояснюється тим, що в розчині відбувається дисоціація фосфорної кислоти. Негативні заряди, що утворюються, відштовхують один від одного комплементарні ланцюги. Катіони в цьому випадку компенсують негативний заряд і зменшують сили відштовхування.
Приклади розв’язання задач
Задача 3.1. При переносі етану з бензолу у воду при температурі 25 °С ентальпія зменшилася на 9240 Дж/моль, а ентропія — на 84 Дж/(моль·К). Розрахувати зміну повного термодинамічного потенціалу в цьому процесі. Чи буде бензол розчинятися у воді?
Розв’язання. Зміна повного термодинамічного потенціалу складе:
∆G = ∆H – T∆S = –9240 – 298·(–84) ≈ 16000 Дж/моль = 16 кДж/моль.
Завдяки тому що ∆G > 0, то бензол слабко розчинний у воді.
Задача 3.2. При неферментативному розкладанні перекису водню енергія активації реакції складає 75 кДж/моль, а при участі ферменту каталази знижується до Eакт ф =8 кДж/моль. Розрахувати, в скільки разів збільшиться швидкість ферментативної реакції в порівнянні з неферментативною при температурі 25 °С.
Розв’язання. Відношення швидкостей реакції дорівнює відношенню констант цих реакцій
або, відповідно до рівняння Арреніуса,
де vф і vн — швидкості; Eакт ф і Eакт н — енергії активації ферментативної і неферментативної реакцій, відповідно. Підставляючи чисельні дані, отримуємо
1 Цей метод також можна використовувати при вимірі ступеня спіральності білків, однак максимум їхнього поглинання лежить у далекій ультрафіолетовій області (200 нм), у котрій важко проводити спектрофотометричні виміри.
75
= 5,6·1011.
Задача 3.3. Використовуючи умову попередньої задачі, розрахува-
|
|
|
|
|
|
Рис. 3.30. Залежність оптичної густини |
Рис. 3.31. Перехід спіраль[клубок |
||||
(D) від довжини хвилі (λ) для спіральної |
у ДНК (θ – частка спіралізованих |
||||
(1 ) і клубкоподібної (2) конформації ДНК |
ланок, θ = 1 для цілком спіралізованої |
||||
тимуса теляти у важкій воді. |
ДНК, θ = 0 для цілком розплетеної |
||||
|
|
ДНК). |
|||
ти, при якій температурі середовища Т2, швидкість неферментативної реакції буде дорівнювати швидкості ферментативної при температурі
Т1 = 25 °С. |
|
|
|
|
|
|
|
|
|
|
|
Розв’язання. За умови, що vн = vф, із рівняння Арреніуса, отримує- |
|||||||||||
мо: |
|
|
|
|
|
|
|
|
|
|
|
звідси |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
T |
|
= |
T1Eакт н |
. |
|
|
|
|
|
|
|
2 |
|
|
|||
|
|
|
|
|
|
|
|
E акт ф |
|||
|
|
|
|
|
|
|
|
|
|||
Підставляючи чисельні дані, отримаємо |
|||||||||||
T |
|
= |
T1E акт н |
= |
298 ·75 ·103 |
|
|
||||
2 |
|
|
|
|
|
|
|
|
|||
|
E акт ф |
|
8 ·103 = 2794 К ≈ 2500°С. |
||||||||
|
|
|
|
|
|||||||
|
|
|
|
|
|
||||||
Питання тестового контролю
3.1. Енергія ванFдерFваальсового притягання обернено пропорцій-
на:
а) r; б) r2;
76
в) r6; г) r8; д) r12,
де r — відстань між атомами.
3.2.Координаційне число води в структурі льоду складає: а) 1; б) 2; в) 3; г) 4; д) 5.
3.3.Координаційне число води в рідкому стані складає біля: а) 2,3; б) 3; в) 4; г) 4,4; д) 5,7.
3.4.При утворенні упорядкованої структури води:
а) ∆S < 0, ∆H < 0, ∆G < 0; б) ∆S > 0, ∆H > 0, ∆G > 0; в) ∆S > 0, ∆H < 0, ∆G > 0; г) ∆S < 0, ∆H > 0, ∆G < 0; д) ∆S < 0, ∆H > 0, ∆G < 0.
3.5.При розчиненні у воді гідрофобної сполуки: а) ∆S > 0, ∆H > 0, ∆G < 0;
б) ∆S > 0, ∆H > 0, ∆G > 0; в) ∆S < 0, ∆H < 0, ∆G < 0; г) ∆S < 0, ∆H > 0, ∆G < 0; д) ∆S < 0, ∆H < 0, ∆G > 0.
3.6.Залежність енергії молекул, що мають осьову симетрію С3, від кута повороту ϕ приблизно визначається формулою:
а) U = 1/2U0 (1 – sin 3ϕ); б) U = 1/2U0 (1 – cos 3ϕ); в) U = 1/3U0 (1 + sin 2ϕ); г) U = 1/3U0 (1 + cos 3ϕ);
=1/4U0 (1 – cos 2ϕ).
3.7.У білках ковалентними зв’язками стабілізована переважно: а) тільки первинна структура; б) первинна і вторинна структури;
в) первинна, вторинна і третинна структури; г) тільки четвертинна структура; д) усі типи організації білка.
3.8.Якщо в білку відношення числа полярних залишків до неполярних (b) перевищує відношення об’єму гідрофільної фази до об’єму
гідрофобного ядра (bs ), то глобула буде прагнути: |
77 |
|

а) прийняти сферичну форму; б) прийняти витягнуту форму;
в) утворити надмолекулярну структуру; г) така структура завжди нестабільна. 3.9. Дія ферментів зводиться:
а) до збільшення вільної енергії кінцевого продукту; б) збільшення енергії активації реакції, яка каталізується; в) зменшення вільної енергії кінцевого продукту;
г) зменшення енергії активації реакції, яка каталізується; д) зміни хімічної рівноваги в реакціях.
3.10. Рівняння Міхаеліса — Ментен має вигляд:
а)
б)
в)
г)
д)
3.11.У присутності конкурентного інгібітора: а) швидкість реакції не змінюється; б) швидкість реакції збільшується;
в) максимальна швидкість реакції не змінюється; г) максимальна швидкість реакції зменшується; д) максимальна швидкість реакції збільшується.
3.12.У присутності неконкурентного інгібітора: а) швидкість реакції не змінюється; б) швидкість реакції збільшується;
в) максимальна швидкість реакції не змінюється; г) максимальна швидкість реакції зменшується; д) максимальна швидкість реакції збільшується.
3.13.Розрахувати константу дисоціації нуклеотидного ланцюга, який складається з чотирьох пар нуклеотидів, якщо константа дисоціації однієї пари нуклеотидів дорівнює 1/7:
а) 7,3·10–5; б) 4·10–4;
78

в) 0,49; г) 2,4·103; д) 5·103.
3.14. Явище гіпохромізму ДНК полягає:
а) у збільшенні оптичної щільності в області 260 нм при переході спіраль–клубок;
б) збільшенні в’язкості; в) зменшенні оптичної щільності в області 260 нм при переході
спіраль–клубок; г) збільшенні кількості водневих зв’язків між аденіном і тиміном;
д) зменшенні кількості водневих зв’язків між аденіном і тиміном.
79

80
