
Биофизика 02
.pdf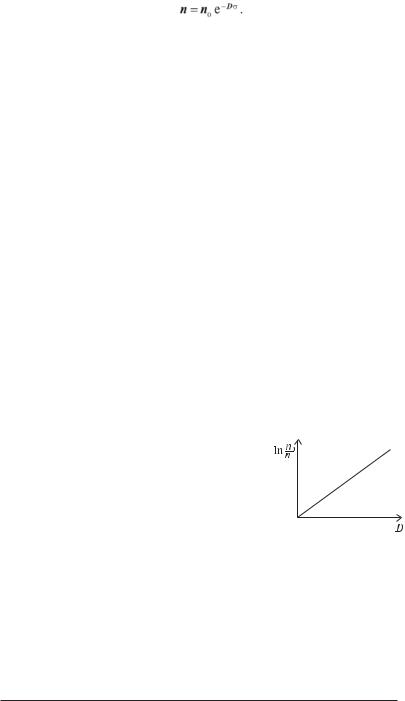
Величинуσможнавизначитияктангенскутанахилупрямоїln(n0/n)=f (D) (рис. 9.7).
У реальних біологічних системах не завжди фотозміни молекул можна розглядати по одноударному механізму, крім того багато ушкоджень відновлюються за допомогою репараційних систем клітини.
§ 46. Оптичне випромінювання в медицині
Оптичне випромінювання широко використовується при лікуванні і діагностиці ряду захворювань. Наприклад, тепловий ефект інфрачервоного випромінювання ближньої області (λ = 0,76 – 2,5 мкм) використовують для прогрівання поверхневих шарів тіла (на глибині біля 2 см). За джерело випромінювання використовують спеціальні лампи. Теплорегулююча система організму, намагаючись остудити нагріту ділянку, підсилює кровообіг у ньому, що і викликає терапевтичний ефект.
Невеликі дози ультрафіолетового опромінення роблять сприятливу дію на серцевоFсудинну, ендокринну, нейрогуморальну, дихальну системи. На жаль, молекулярний механізм такого впливу ультрафіолету в більшості випадків точно невідомий.
Комбінована дія фотосенсибілізаторів псораленів і ультрафіолетового опромінення АFзони (так звана ПУФАFтерапія) широко використовується, іноді як єдиний ефективний метод, при лікуванні ряду шкірних захворювань, наприклад, псоріазу, вітіліго, деяких форм облисіння (гніздна плішивість). Однак ПУФАFтерапія має ряд побічних ефектів, наприклад, приводить до утворення еритеми, едеми.
Випромінювання гелійFнеонового лазера
(λ=632 нм) застосовується для прискорення загоєння ран. У хірургії використовуються лазерні скальпелі, здатні викликати високотемпературну руйнацію тканини з одночасною коагуляцією білка. Такі операції протіка-
ють безкровно і широко практикуються при лікуванні відшарування сітківки, глаукоми (лазером проколюються мікроскопічні отвори діаметром 50–100 мкм, що викликає відтік внутрішньоочної рідини і, отже, зниження внутрішньоочного тиску).
Фотосенсибілізатор гематопорфірин і його похідні використовують
при лікуванні злоякісних пухлин, тому що виявлено, що ці сполуки
1 Залежність поперечного перетину інактивації молекули від довжини хвилі також як і залежність квантового виходу від довжини хвилі, називають спектром дії.
171

накопичуються винятково в пухлинних клітинах і відсутні в здорових. Сенсибілізатори підвищують чутливість пухлини до дії видимого світла, опромінення яким приводить до її загибелі. Даний метод фотохіміотерапії використовують при лікуванні пухлин як шкіри, так і внутрішніх органів. У останньому випадку опромінення здійснюється за допомогою спеціальних світловодів. Виборче накопичування в пухлинах гематопорфіринів використовують також при діагностиці онкологічних захворювань, тому що люмінесценція цих молекул дозволяє визначити розміри пухлини.
Ультрафіолетове випромінювання великої потужності чинить бактерицидний ефект, що використовується при стерилізації медичних інструментів і помешкань. За джерело випромінювання застосовують спеціальні бактерицидні лампи.
Деякі речовини, наприклад, лікарські препарати промазин, сульфаніламіди, прометазин та інші в сполученні з ультрафіолетовим випромінюванням викликають фотоалергічні реакції. Поглинаючи ультрафіолет АFзони, вони зв’язуються з білками, створюючи антиген (рис. 9.8). При першому утворенні такого комплексу речовина – білок у результаті імунної відповіді організму утворюються сенсибілізовані лімфоцити, а при повторному — спостерігаються алергічні реакції і навіть анафілактичний шок.
§ 47. Взаємодія іонізуючого випромінювання з речовиною
Іонізуюче випромінювання (далека область ультрафіолетового випромінювання, рентгенівське і γFвипромінювання) має достатню енергію для того, щоб викликати іонізацію молекул, і як наслідок цього здатне привести до найбільш небезпечних для біологічних структур наслідків: поразці та інактивації окремих структур і загибелі організму.
Природний радіоактивний фон створюється космічним випромінюванням і випромінюванням радіоактивних ізотопів земної кори. Останнім часом з’явилися штучні джерела випромінювання, використовувані в енергетиці, військовоFпромисловому комплексі, а також у медицині (рентгенівські та γFустановки).
Рентгенівське випромінювання виникає при гальмуванні прискорених електронів у речовині, γFвипромінювання — при переході атомних ядер зі збудженого стану в основний або при анігіляції електронноFпозитронної пари (див. далі), а також під час розпаду деяких частинок. При взаємодії цих видів випромінювання з речовиною можливі наступні ефекти: фотоефект, ефект Комптона та ефект утворення пари.
Фотоефект — явище, при якому квант рентгенівського або γFвипромінювання вибиває електрон з електронної оболонки атома (рис.
172

9.9). Для того, щоб це сталося, енергія падаючого кванту hν повинна перевищувати енергію зв’язку електрона в атомі W. Квант цілком передає енергію атому, витрачаючи її на розрив зв’язку електрона і повідомлення йому деякої кінетичної енергії Екін:
Екін = hν – W.
Рис. 9.8. Фотоалергічна реакція організму.
Імовірність фотоефекту збільшується зі зростом заряду ядра і наближенням енергії кванта світла до енергії зв’язку електрона в атомі.
У випадку ефекту Комптона (рис. 9.10) квант, зіштовхуючись з атомом, витрачає частину своєї енергії на вибивання електрона і продовжує свій рух, але вже в іншому напрямку і володіючи меншою кількістю енергії. Такий фотон називається розсіяним, а вибитий електрон — комптонівським електроном або електроном віддачі. Розсіяний фотон здатний взаємодіяти з іншими атомами і викликати нові ефекти Комптона або фотоефект.
Чим менша довжина хвилі падаючого фотона, тобто, чим більша його енергія, тим більша імовірність ефекту Комптона і менша імовірність фотоефекта. У результаті кількох послідовних ефектів Комптона енергія розсіяних фотонів поступово зменшується в порівнянні з первинним фотоном і зростає імовірність фотоефекту.
Якщо енергія фотона перевищує 1,022 МеВ, то взаємодія падаючого кванта з полем ядра може привести до перетворення кванта в дві частинки: електрон і позитрон (ефект утворення пар) (рис. 9.11):
hν → e– + e+.
Енергія, рівна 1,022 МеВ, витрачається на перетворення в масу спокою електрона і позитрона, а інша частина енергії кванта — на повідомлення кінетичної енергії частинкам, що утворюються:
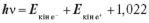 МеВ,
МеВ,
де — кінетична енергія електрона; — кінетична енергія позитрона.
Можливий і зворотний ефект, коли електрон і позитрон анігілюють, в результаті чого з’являються два γFкванти:
e– + e+ → 2γ.
173
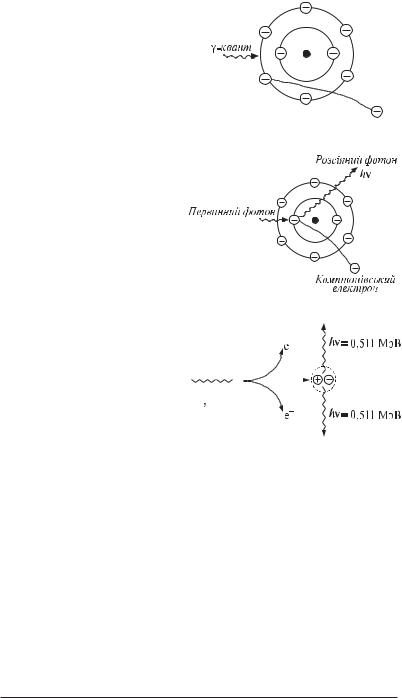
Енергія кожного з квантів, що утворюються, складає не менше 0,511 МеВ.
Імовірність ефекту утворення пар залежить не тільки від енер-
гії кванта, але і від заряду ядра z.
Чим вища величина z, тим більша імовірність утворення пари. До складу біологічних систем в основному входять легкі ядра, тому
ефект утворення пар відбувається рідко в порівнянні з іншими ефектами (фотоефектом і ефектом Комптона).
У п р о ц е с і ф о т о F , КомптонFефектів і утворення
пари відбувається первинна іонізація атомів. Вибиті електрони в процесі свого руху можуть віддавати свою енергію атомам і
тим самим приводити до їхнього збудження й іонізації, в результаті чого породжуються вторинні електрони. Багаторазово взає- 
 модіючи з атомами, електрон
модіючи з атомами, електрон 
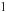
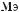
поступово втрачає свою енергію доти, поки вона не знизиться настільки, що електрон захопиться
якимFнебудь нейтральним атомом і утворить із ним негативний іон.
Крім рентгенівських і γFпроменів до іонізуючого випромінювання відносять також потоки αFчастинок (ядер атомів гелію), βFчастинок (електронів і позитронів), протонів, нейтронів і ін. Заряджені частинки, які взаємодіють з електричними полями електронів, здатні перевести атоми в збуджений стан або іонізувати їх. Нейтрони, так як вони не мають заряду, можуть викликати іонізацію атомів лише непрямим шляхом. Наприклад, поглинання нейтрона ядром атома (частіше усього водню, іноді азоту, вуглецю, кисню) приводить до збільшення кінетичної енергії останнього. Так зване ядро віддачі, що при цьому утворюється, взаємодіючи з іншими атомами може викликати їхню іонізацію. Іноді тільки частина енергії нейтрона йде на повідомлення ядру кінетичної
174
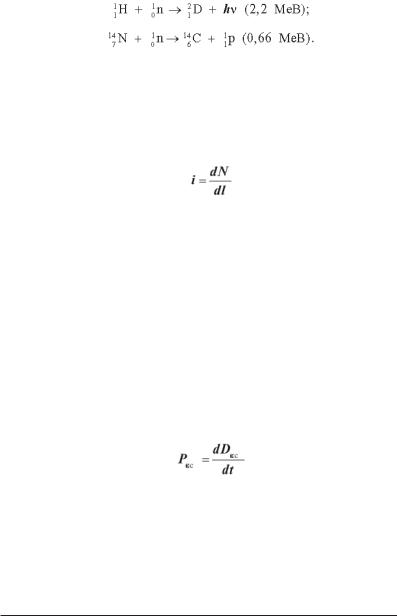
енергії, а інша частина — на збудження ядра. Перехід ядра зі збудженого стану в основний супроводжується випромінюванням γFквантів. При низьких швидкостях нейтронів їхня взаємодія з речовиною може привести до ядерних реакцій, в результаті яких утворюються γFкванти
ізаряджені частинки:
Упроцесі свого руху іонізуюче випромінювання втрачає свою енергію
іпередає її речовині. Середня енергія, передана речовині на одиницю довжини пробігу, називається лінійною передачею енергії. Відстань, яку випромінювання проходить у речовині, зберігаючи здатність до іонізації (середній лінійний пробіг), характеризує проникаючу спроможність випромінювання. Відношення кількості пар іонів N, утворених випромінюванням на довжині пробігу l — лінійна щільністю іонізації i
характеризує іонізуючу спроможність випромінювання. Чим більше заряд і маса частинки, тим вища її іонізуюча і менша проникаюча спроможність. Ці величини також залежать від густини речовини, що опромінюється, і різні для αF, βF, γFвипромінювання.
§ 48. Дози іонізуючих випромінювань
При вивченні ступеня ураження тих або інших біологічних об’єктів важливо мати кількісне уявлення про фізичні характеристики випромінювання, особливо його енергії.
Іонізуюче випромінювання, насамперед, характеризується своєю здатністю іонізувати речовину. Кількісно цю характеристику відбиває експозиційна доза Dекс. При експозиційній дозі, рівній 1 Кл/кг у 1 кг сухого повітря утворюється 1 Кл зарядів кожного знака. Найчастіше експозиційна доза вимірюється в позасистемних одиницях — рентгенах (1 Р = 2,58·10–4 Кл/кг). Потужність експозиційної дози дорівнює:
і вимірюється в Кл/кг·с або Р/с.
Випромінювання може впливати на речовину тільки в тому випадку, якщо відбудеться поглинання цього випромінювання речовиною. Тому важливо знати не експозиційну, а поглинену дозу, яка визначає енергію, передану одиниці маси речовини. Одиницею виміру поглиненої дози є Грей (1 Гр = 1 Дж/кг) або рад1 (1 рад =
175

= 10–2 Дж/кг). Потужність поглиненої дози дорівнює:
і вимірюється в Гр/с або рад/с.
Експериментальному виміру піддається експозиційна, але не поглинена доза, однак між ними існує залежність
Dпогл = kDекс,
де k — деякий коефіцієнт, що залежить як від самого випромінювання, так і від речовини, що опромінюється.
Дія іонізуючого випромінювання однакової енергії, але різного виду (наприклад, αF, βF і γFвипромінювання) чинить різний біологічний ефект, так як ці випромінювання розрізняються своєю іонізуючою і проникаючою спроможністю. У радіобіології існують поняття еквівалентних доз опромінення. Доза випромінювання, що чинить такий же біологічний ефект, як і доза в 1 Р рентгенівського або γFвипромінювання, складає 1 бер (біологічний еквівалент рентгена), а доза, еквівалентна 1 Гр, складає 1 зіверт (Зв).
Поглинена доза Dпогл і еквівалентна доза Н зв’язані між собою співвідношенням
H = KDпогл,
де К — коефіцієнт якості випромінювання (відносна біологічна ефективність), яка показує, у скільки разів ефективність біологічної дії даного виду випромінювання більша, ніж рентгенівського або γFвипромінювання, при однаковій дозі. К експериментально визначений для кожного виду випромінювання (табл. 9.2).
Іноді опромінення біологічного об’єкта робиться джерелом, розташованим не зовні, а всередині його, наприклад, при введенні в пухлинну тканину радіонуклідних голок (цей метод використовується в радіотерапії), включенні в організм радіоактивних ізотопів. У цьому випадку дози опромінення розраховуються по відомих значеннях активності ізотопів і коефіцієнтів поглинання даної тканини.
§ 49. Вплив іонізуючого випромінювання на організм
Іонізація і збудження молекул, викликані дією іонізуючої радіації, приводять до хімічних змін у них, тобто до радіаційних ушкоджень. Якщо радіаційне ураження молекули обумовлене безпосереднім влученням у неї кванта, то говорять про пряму дію випромінювання, якщо взаємодією з радіаційними продуктами, то — про непряму дію випромінювання.
1 Абревіатура від англ. Radiation Absorbed Dose.
176

Ураження клітин викликаються в основному ушкодженнями молекул білків, нуклеїнових кислот, ліпідів, що знаходяться у водяній фазі. Так як кількість молекул води набагато перевищує кількість розчинених у ній молекул, то радіаційні ушкодження біологічних молекул частіше усього викликаються їхньою взаємодією з продуктами радіолізу води, у ході якого утворюються сольватовані електрони і вільні радикали:
Н2О → Н2О+ + е–; Н2О + е– → Н2О–; Н2О– → ОН– + Н·;
ОН– → ОН· + е–.
У нуклеїнових кислотах під дією іонізуючого випромінювання відбуваються зміни як в окремих нуклеотидах (наприклад, розмикання піримідинового або імідазольного кілець, дезамінірування аденіну, гуаніну і цитозину, окислювання спиртових груп і розриви вуглецьFвуглецевих зв’язків у дезоксирибозі), так і в спіральній структурі (одноF і дволанцюжкові розриви, зшивки між нуклеотидами одного або різних ланцюгів, зшивки ДНК–білок). Викликані зміни в молекулах нуклеїнових кислот приводять до виникнення генних (зміни нуклеотидного складу окремого гена) і хромосомних (зміни структури хромосом) мутацій.
Дія іонізуючого випромінювання на білки викликає ушкодження
амінокислот, розриви водневих, дисульфідних, поліпептидних зв’язків
Табл. 9.2
Коефіцієнти якості різних видів випромінювання
Вид випромінювання |
Коефіцієнт якості |
|
|
Рентгенівське, γF і βFвипромінювання |
1 |
|
|
Нейтрони (~0,01 еВ) |
3 |
|
|
Нейтрони (5 еВ) |
7 |
|
|
Нейтрони (0,5 МеВ), протони |
10 |
|
|
αFвипромінювання |
20 |
|
|
і, як наслідок, утрату їхніх біологічних функцій. Ці порушення можуть бути викликані як безпосереднім улученням кванта випромінювання, так і взаємодією білка з вільними радикалами або іншими продуктами радіолізу сусідніх молекул.
Ушкодження ліпідів в основному викликані перекисним окислюванням ненасичених жирних кислот. Ініціаторами даної реакції є вільні
177

радикали води або самих ліпідів. Внаслідок ланцюгового характеру даної реакції уражається значна кількість ліпідних молекул у результаті влучення усього лише одного кванта. Радіаційні ушкодження ліпідних молекул приводять до утворення альдегідів, кетонів, спиртів, а також зшивок між молекулами.
У клітині існують спеціальні репараційні системи, що відновлюють ушкоджені молекули. Ці системи здатні репарувати молекули від ушкоджень, викликаних різними чинниками як фізичної (ультрафіолетове, γFопромінення), так і хімічної (хімічні агенти) природи, тому що часто ушкодження, що ініціюються ними, подібні.
В даний час відомі репараційні системи для відновлення ДНК і мембран. Найбільш добре вивченими є системи, що репарують одноF і дволанцюжкові розриви ДНК. Ушкодження мембран усуваються шляхом заміни ушкоджених компонентів (ліпідів і білків). Відновлення компонентів мембрани відбуваються й у процесі нормального функціонування клітини, але при опроміненні цей процес прискорюється. Репарація інших біологічних сполук, у тому числі і білків, не так важлива, тому що такі молекули, якщо вони ушкоджені, можуть витіснятися з метаболізму і замінятися іншими.
Репарація ушкоджень пояснює так званий ефект фракціонування, що полягає в наступному. Допустимо, що однократне опромінення клітин певною дозою викликає їхню 50%Fну загибель (доза D50). У той же час, якщо опромінення цією ж дозою розділити на дві напівдози з проміжком часу між ними ∆t, то загибель клітин вже буде складати менше 50%, причому виживаність буде тим вища, чим більший проміжок ∆t. Справа в тому, що під час одноразового опромінення відбувається підсумовування і посилення радіопошкоджень, а при фракційному опроміненні — після першої дози деякі з виниклих ушкоджень встигають відновитися. Тому сумарні ушкодження при однократному опроміненні вищі, ніж при фракційному.
Репараційні системи не здатні усунути всі порушення. З іншого боку, іноді відбувається помилкова репарація молекул, що приводить до ще більших їхніх ушкоджень.
Дослідження процесів пошкоджень багатоклітинного організму найбільш важке, тому що клітини різних тканин мають різну радіочутливість. Відповідно до правила Бергон’є і Трибондо, радіочутливість клітин у тканині тим вища, чим більша їхня проліферативна1 активність і менша ступінь диференціації. Тому в організмі людини в першу чергу пошкоджуються стовбурні клітини червоного кісткового мозку й епітелію кишечника.
Ушкодження клітини неоднакові в різні фази її клітинного циклу. Радіочутливість клітин максимальна наприкінці G1Fфази (пресинтетичної) і початку SFфази (синтетичної або реплікативної), тому що виниклі
178
в цей час ушкодження не встигають репаруватися.
Радіобіологічні ефекти можуть виявлятися як безпосередньо після опромінення, так і через деякий проміжок часу: місяці, роки і навіть покоління. Наприклад, у людини віддаленими наслідками опромінення можуть виступати процеси утворення злоякісних пухлин, ослаблення імунітету, скорочення тривалості життя, народження дітей із патологіями.
§ 50. Кількісна оцінка радіопошкоджень
Кількісно ступінь пошкоджень від радіаційного опромінення оцінюють за допомогою дозових кривих — залежностей ефекту опромінення від дози випромінювання. Ефект опромінення визначається за деякою реакцією об’єкта, що опромінюється, яка називається тестFреакцією. Нею може бути,наприклад,виживаністьклітин,радіостійкістьмолекуліт.д.Кривідоза
— ефект частіше усього мають експоненціальну форму, що вказує на те, що навіть при дуже великих дозах зберігаються клітини, що вижили, або непошкоджені молекули. Криві зручно представляти в напівлогарифмічній системі координат, тому що в цьому випадку залежність ефекту від дози являє собою пряму.
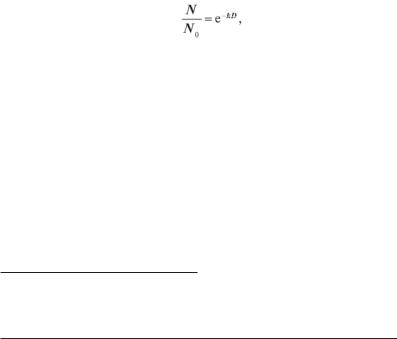
Допустимо, що як тестFреакції виступає відношення кількості непошкоджених молекул (клітин) N до їхньої загальної кількості N0. Тоді рівняння залежності доза — ефект має вигляд
де k — коефіцієнт радіочутливості молекул (клітин); D — доза опромінення.
Для характеристики радіочутливості молекул або клітин уводять значення дози, при якій кількість непошкоджених об’єктів зменшується в е раз у порівнянні з вихідним, тобто зберігається 37% матеріалу (D37), або дози, при якій зберігається 50 % матеріалу (D50 або напівлетальна доза).
Влучення кванта випромінювання на даний об’єкт є дискретним і статистичним процесом (принцип улучення), ушкодження об’єкта викликається влученням кванта лише у певну його ділянку (принцип мішені), уражений об’єкт є причиною ушкодження інших (принцип підсилювача). Поясненням останнього принципу є, наприклад, випадки поразки ДНК, що приводять до синтезу інших молекул ДНК, які містять цю ж помилку, і білкових молекул, нездатних виконувати потрібну
1 Проліферація (від лат. proles – нащадок і fero – несу) – збільшення кількості клітин шляхом мітозу.
179

біологічну функцію.
Відповідно до принципу мішені, відношення кількості непошкоджених клітин N до їхньої загальної кількості N0, якщо пошкодження відбувається за одноударним механізмом, визначається рівнянням
де ν — об’єм мішені; D – доза опромінення.
Якщо ж для прояву радіобіологічного ефекту потрібно n влучень у дану мішень (при цьому n – 1 влучення ефекту не викликає), то виживаність клітин описується наступним виразом:
де k — кількість влучень у мішень (k < n).
Частіше усього загибель клітини викликається пошкодженням не однієї, а кількох мішеней. Допустимо, що кількість цих мішеней дорівнює l, і загибель клітини станеться, якщо в кожну мішень потрапить принаймні один квант. Тоді виживаність клітин дорівнює:
При великих дозах опромінення
або після логарифмування
Графік цієї залежності (рис. 9.12.) дозволяє визначити кількість мішеней l, що уражаються.
§ 51. Модифікація радіобіологічних ефектів
Існують речовини, що підсилюють радіобіологічний ефект (радіосенсибілізатори) або ослаблюють його (радіопротектори). Дія одних модифікаторів виявляється до опромінення, а інших — після. Перші з них називаються модифікаторами профілактичної дії, а другі — терапевтичної.
Найбільше вивченими радіопротекторами є речовини, що володіють антиоксидантними властивостями, тобто здатні інактивувати вільні радикали. На практиці широко застосовують як радіопротектори сульфгідрильні сполуки: цистеїн, цистеамін, цистамін, глутатіон. 3Fамін опропіламіноFетілфосфотионова кислота, що є аналогом цистеаміну,
180
