
- •V. 6 феноли
- •6.1 Класифікація. Номенклатура. Ізомерія
- •6.2 Електронна будова фенолу
- •6.3 Фізичні властивості
- •6.4 Хімічні властивості
- •І Кислотні властивості
- •Іі Реакції електрофільного заміщення
- •IV Окиснення та відновлення
- •V Якісні реакції на феноли
- •6.5 Одержання фенолів
- •6.6 Застосування фенолів
IV Окиснення та відновлення
За рахунок підвищеної електронної густини на бензеновому кільці феноли окиснюються надзвичайно швидко: навіть при константі з повітрям фенол набуває червонуватого забарвлення, зумовленого продуктами окиснення.
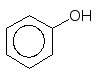
Слабкі окисники окиснюють фенол до пірокатехіну, а сильні – до бензохінону:
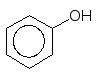
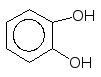
+ Н2О2 ––––––––––> + H2O
Fe
 Пірокатехін
Пірокатехін
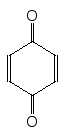
[O]
–––––––––––––––––>
K2Cr2O7, H2SO4
n–Бензохінон
При дії окисників на нафтоли окисненню піддається переважно те кільце, що містить замісник:
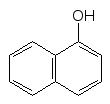
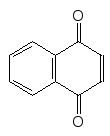
[O]
–––––––––––––––>
CrO3, H2SO4
–Нафтол 1,4–Нафтохінон
У загальному випадку одноатомні нафтоли окиснюються швидше, ніж одноатомні феноли.
 Двохатомні
феноли порівняно із одноатомними ще
легше піддаються окисненню, при якому
вони теж перетворюються у хінони
(ароматичні дикетони)
:
Двохатомні
феноли порівняно із одноатомними ще
легше піддаються окисненню, при якому
вони теж перетворюються у хінони
(ароматичні дикетони)
:
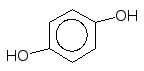
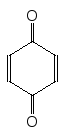
[O] [O]
–––––––––––> <–-–––––––––––
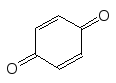
Гідрохінон Резорцин
n–Бензохінон
[O]
–––––––––––>
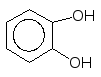
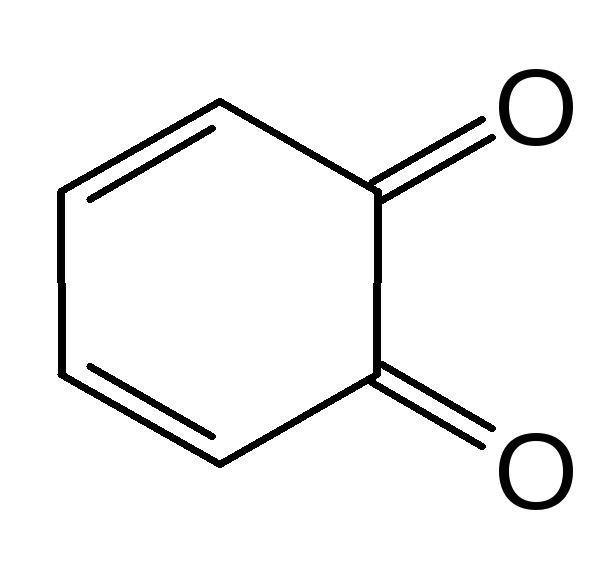
Пірокатехін о–Бензохінон
 Завдяки
відновлювальним властивостям двохатомні
феноли застосовуються як антиоксиданти
та інгібітори полімеризації, а також
як проявникі у фотосправі, наприклад:
Завдяки
відновлювальним властивостям двохатомні
феноли застосовуються як антиоксиданти
та інгібітори полімеризації, а також
як проявникі у фотосправі, наприклад:
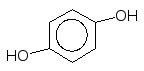
+ AgBr + NaOH –––––> + Ag + NaBr + H2O.
Гідрохінон n–Бензохінон
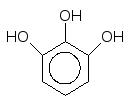 Найсильнішу
відновлювальну здатність мають триатомні
феноли, які окиснюються навіть повітрям
з руйнуванням ароматичного кільця. Ця
властивість використовується у газовому
аналізі для поглинання кисню:
Найсильнішу
відновлювальну здатність мають триатомні
феноли, які окиснюються навіть повітрям
з руйнуванням ароматичного кільця. Ця
властивість використовується у газовому
аналізі для поглинання кисню:
+ O2 ––––––––––––> продукти окиснення
NaOH, H2O
Пірогалол
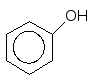
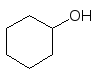
Відновлення фенолів можна провести тільки за жорстких умов у присутності каталізаторів: при їх гідруванні одержують циклогексаноли – вихідну сировину у виробництві капролактаму:
 130–1500C,
5–20 Атм
130–1500C,
5–20 Атм
+ 3Н2 ––––––––––––––––––––>
Ni
Циклогексанол

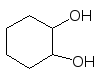
120–1500C
+ 3H2 –––––––––––––––>
Ni
Пірокатехін Циклогександиол–1,2
Перегонка з цинковим пилом перетворює фенол у бензен:
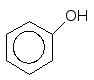
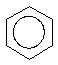
t0
+ Zn –––––––––> + ZnO
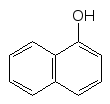
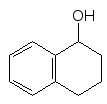
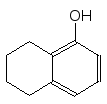 Нафтоли
при відновлювальному гідруванні
утворюють суміштетралінів
(тетрагідронафталінів)
з гідроксильною групою частково в
ароматичному, але переважно в
циклогексановому кільці:
Нафтоли
при відновлювальному гідруванні
утворюють суміштетралінів
(тетрагідронафталінів)
з гідроксильною групою частково в
ароматичному, але переважно в
циклогексановому кільці:
2000C, 50–200 Атм
+ 2H2 ––––––––––––––––––––>
Ni
Нафтол–1 1,2,3,4–Тетрагідро– 1,2,3,4– Тетрагіро–
нафтол–1 (основний продукт) нафтол–5
Як видно із порівняння умов гідрування фенолів і нафтолів, останні відновлюються складніше, ніж феноли.
