
ПОСОБИЕ по ФХОГТ
.pdf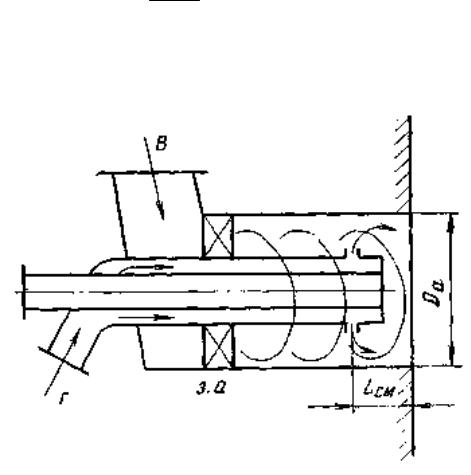
24
2.Аэродинамический параметр, характеризующий интенсивность тур-
булентного смешения, nа в в2.з , где ωв.з – действительная скорость завих-
г 2г
ренного потока воздуха, примерно равная удвоенной расходной (аксиальной)
скорости; ωв.з=2ωа. Оптимальное значение параметра nа=1÷1,2.
Рис.2.3. Схема газовой горелки с центральным вводом газа.
В – ввод горячего воздуха; Г – подвод проводного гaзa; з.а. – завихривающий аппарат.
3. Размер, форма и расположение газовых отверстий, определяемые общей конструкцией горелки.
Возможен периферийный, центральный и двусторонний ввод газовых струй в поток воздуха в горелках. На рис.2.3 показан центральный ввод газа.
2.3.Подготовка к сжиганию мазута и природного газа
Для перекачки мазута, заполнения и слива его из емкостей температура мазута должна быть не ниже 60÷70°С, что соответствует вязкости не выше
30° ВУ.
25
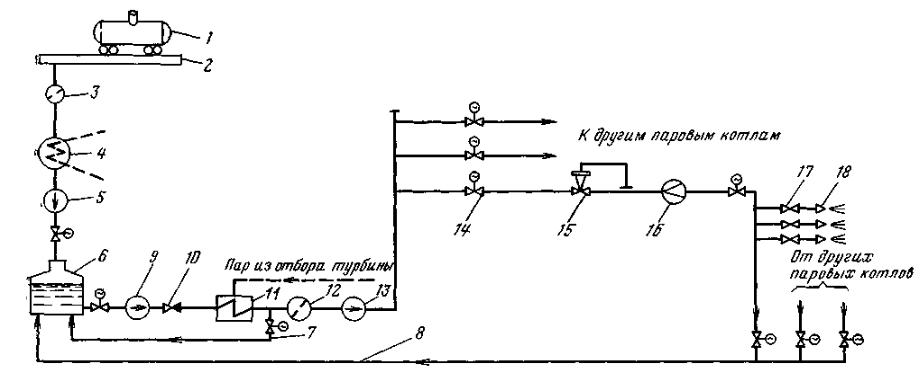
Рис.2.4. Технологическая схема подготовки мазута на электростанции.
1 – цистерна с мазутом; 2 – сливное устройство; 3 – фильтр грубой очистки; 4 – сливной резервуар с подогревом; 5
–перекачивающий насос; 6 – основной резервуар; 7, S –линии рециркуляции мазута; 9 – насос первого подъема; 10
–обратный клапан; 11– подогреватель мазута; 12 – фильтр тонкой очистки; 13– насос второго подъема; 14 – запорная задвижка; 15 – регулятор расхода; 16 – расходомер; 17 – задвижка; 18 – форсунка.
26
Технологический тракт подготовки мазута на электростанции (рис.2.4) включает: приемно–сливное устройство (сливные эстакады с желобами, приемные резервуары с погруженными перекачивающими насосами), основные резервуары для хранения постоянного запаса мазута, мазутонасосную, систему трубопроводов для мазута и пара, группу подогревателей мазута и фильтров.
Подготовка мазута перед сжиганием заключается в удалении механических примесей, повышении давления мазута и его подогреве, необходимых для снижения потерь энергии на транспорт мазута к котлам электростанции и его тонкого распыления в форсунках горелочных устройств. Температура мазута в баках поддерживается на уровне 60÷80°С в любое время года за счет циркуляционного подогрева путем возврата в бак части (до 50%) разогретого во внешних подогревателях мазута.
При высокой скорости мазута в распыливающих форсунках может иметь место сильный абразивный износ металла мазутных каналов форсунки и быстрый выход ее из строя. Кроме того, при размере каналов менее 3 мм не исключено их забивание крупными твердыми частицами или сгустками асфальтосмолистых веществ. Очистка мазута от твердых фракций происходит вначале в фильтрах грубой очистки с размером ячеек сетки 1,5Х1,5 мм, а затем в фильтрах тонкой очистки с ячейками 0,3÷0,5 мм, установленных перед насосами второй ступени на подогретом мазуте.
Повышение температуры мазута обеспечивается в паровых подогревателях до температуры, меньшей температуры вспышки паров. Для поддержания температуры мазута на нужном уровне независимо от потребления его котлом обеспечивается непрерывный расход его через линию за счет частичного возврата в бак (рециркуляция).
Газ поступает на электростанцию от магистрального газопровода или газораспределительной станции (ГРС) с давлением 0,7÷1,3 МПа. Газохранилищами электростанции не располагают. Для снижения давления поступающего газа до необходимого уровня у горелок (0,13÷0,2 МПа) предусматривается его дросселирование в газорегуляторном пункте (ГРП), который ввиду повышенной взрывоопасности и резкого шума при дросселировании газа размещают в отдельном помещении на территории ТЭС (рис.2.5).
В каждом ГРП выполняется несколько (чаще три) ниток газопровода с установкой регуляторов давления, одна из которых является резервной. Кроме того, предусматривается байпасная линия помимо регуляторов. Для очистки газа от механических примесей перед регулирующими клапанами имеются фильтры. Регулирующие клапаны поддерживают необходимое давление «после себя». Для защиты от аварийного повышения давления газа установлены предохранительные клапаны. Количество газа, прошедшего газорегулятор-
27
ный пункт, регистрируется расходомерами. Основными устройствами на газопроводе к каждому паровому котлу являются автоматический регулятор расхода газа (АРР) и отсекающий быстродействующий клапан (БК). Регулятор АРР обеспечивает необходимую тепловую мощность котла в любой момент времени. Импульсный отсекающий БК отключает подачу газа в топку парового котла в случае аварийной ситуации, когда поступление газа может создать опасность взрыва (обрыв факела, падение давления воздуха у горелок, останов электродвигателей дымососа или дутьевого вентилятора и т. п.).
Для исключения взрывоопасных ситуаций в нерабочий период газовые линии продувают воздухом через специальные отводы в атмосферу (свечи). Последние выведены за пределы здания в места, недоступные для пребывания людей. Через свечи вытесняют также газовоздушную смесь из газопроводов перед растопкой котла. Окончание продувки линии газом определяют по содержанию кислорода в пробе не выше 1 %.
Эксплуатация газового оборудования на электростанции ведется в соответствии с правилами безопасности в газовом хозяйстве Госгортехнадзора.

28
Рис.2.5. Схема газоснабжения электростанции.
1 – задвижка с ручным управлением; 2 – задвижка с электроприводом; 3 – регулятор давления газа; 4 – предохранительный клапан; 5 – регулятор расхода газа; 6 – отсекающий быстродействующий клапан; 7 – манометр; 8 – расходометр; 9 – задатчики регуляторов давления; 10 – фильтр; 11 – продувочная свеча; 12 – подвод газа к запальнику горелок; 13 – дренаж; 14 – отбор газа на анализ.
29
3.ФИЗИКО–ХИМИЧЕСКИЕ ОСНОВЫ ТЕОРИИ ГОРЕНИЯ
3.1.Основы теории топочных процессов
Горение топлива в топочной камере определяется сложными физическими и химическими процессами. Из физических явлений, подготавливающих и сопровождающих воспламенение и последующее горение, следует особо выделить процесс смесеобразования топлива и окислителя (аэродинамический фактор). К химическим факторам в первую очередь относятся температура и концентрация реагирующих веществ. В топочных устройствах приходится иметь дело со сложными полями скоростей, концентраций и температур, которые в совокупности определяют кинетику химических реакций.
Протекающие при горении топлива химические реакции совершаются с выделением теплоты. Такие реакции называют экзотермическими. К ним относятся реакции горения углерода, водорода, серы в атмосфере воздуха. В условиях высоких температур в ядре факела могут протекать и реакции, идущие с поглощением теплоты. Они являются эндотермическими реакциями. К ним, например, относятся реакция образования окислов азота: N2+O2=2NO – 180 кДж/моль или реакция восстановления двуокиси углерода до окиси на раскаленной поверхности коксовой частицы пои недостатке ки-
слорода: C+CO2=2CO – 7,25 МДж/кг. Реакция является химически обратимой, если она может идти как в прямом, так и в обратном направлении, однако внешние условия для протекания реакции в том или другом направлении могут существенно отличаться. Так, реакция образования окислов азота наблюдается только в зоне очень высоких температур, а обратная реакция их разложения на газообразные кислород и азот протекает в земной атмосфере под действием солнечной радиации. При горении топлива в топочных камерах скорость прямого процесса несоизмеримо больше скорости обратного, поэтому химическое равновесие этих реакций смещено в сторону образования конечных продуктов, и в указанных условиях эти реакции можно считать необратимыми.
Интенсивность горения характеризуется скоростью реакции. Под скоростью гомогенной реакции понимают массовое количество вещества, реагирующее в единице объема в единицу времени. Скорость реакции в этом случае измеряют по изменению концентрации одного из реагирующих веществ СА моль/м3 или г/м3, за определенный промежуток времени Δτ, с:
р СА / |
(3.1) |

30
Скорость гетерогенной реакции выражают количеством вещества Δg, г, реагирующего на поверхности твердого горючего S, м2, за период времени
Δτ, с:
Кs g/S |
(3.2) |
Скорости реакций подчиняются закону действующих масс, согласно которому в однородной среде при постоянной температуре в каждый момент времени скорость реакции пропорциональна произведению концентраций реагирующих веществ:
|
kCmCn |
, |
(3.3) |
р |
A B |
|
|
где k – константа скорости реакции, зависящая от температуры и химической природы, реагирующих веществ; CА, СВ – текущие концентрации реагирующих веществ А и В в газовой смеси; m, n – числа молей реагирующих веществ.
Поскольку в газовой смеси при постоянной температуре парциальные давления веществ пропорциональны их концентрациям, можно формулу (3.3) записать в виде (скорость гомогенной реакции):
р kpAm pBn |
(3.4) |
В условиях гетерогенного горения концентрация горючего (твердого топлива) неизменна, поэтому скорость такой реакции будет зависеть только от концентрации окислителя (кислорода) у поверхности топлива
р kCОп2 , (3.5)
где С пО2 – концентрация кислорода у поверхности топлива.
При неизменной концентрации реагирующих веществ во времени скорость реакции определяется константой скорости реакции k, которая зависит от температуры и природы вступающих в реакцию веществ. Эта зависимость
выражается законом Аррениуса: |
|
k k0e E / RT , |
(3.6) |
31
где k0 – предэкспоненциальный множитель; Е – энергия активации; R – газовая постоянная; T –абсолютная температура процесса.
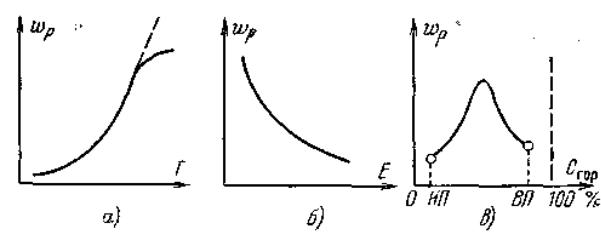
Таким образом, скорость реакции с ростом температуры быстро увеличивается (рис.3.1,а). Химическая реакция может происходить при столкновении молекул веществ между собой. Если бы все столкновения приводили к реакциям, то горение происходило бы с огромной скоростью, тогда констан-
та скорости равнялась бы k0. В действительности реакция может произойти только в том случае, когда за счет энергия соударения произойдет разрушение старых молекулярных связей и образовавшиеся осколки старых молекул могут перегруппироваться и создать молекулы новых веществ.
Рис.3.1. Зависимость скорости реакции от температуры (а), энергии активации (б) и концентрации горючего вещества (в). НП – нижний предел; ВП – верхний предел.
Энергия, достаточная для разрушения внутримолекулярных связей исходных веществ, называется энергией активации Е. Чем выше уровень энергии активации, тем труднее происходит разрушение молекулярных связей исходных молекул и медленнее скорость реакции (рис.3.1,б). Так, энергия ак-
тивации реакции С=О2=СО2 ЕСО2=140 кДж/моль, а реакции С+0,5О2=СО
ЕСО=60 кДж/моль.
Отсюда следует, что в реакциях окисления углерода кислородом скорость образования окиси углерода СО значительно выше, чем образование двуокиси СО2, и количество СО у поверхности горящего углерода будет преобладать.
В топочных устройствах горение происходит при постоянной подаче топлива и окислителя (воздуха) в зону горения и, следовательно, при практически постоянной концентрации реагирующих веществ во времени. В этих
32
условиях максимальная скорость реакция может быть достигнута при соотношении концентраций исходных веществ, близком к стехиометрическому. При избытке горючего (богатая смесь) или при малой его концентрации (бедная смесь) скорость реакции снижается ввиду уменьшения тепловыделения на единицу объема.
Горение может происходить не при любой концентрации горючего в смеси, а лишь в определенном соотношении с воздухом (окислителем). Существует нижний предел концентраций горючего (НП), ниже которого горение становится невозможным, и верхний предел (ВП), когда дальнейшее увеличение концентраций горючего в смеси также прекращает горение (рис.3.1,в). Во всем диапазоне концентраций между этими пределами горение возможно.
Если весь объем окажется заполненным готовой для горения газовоздушной смесью то при внесении источника зажигания реакция окисления распространяется с такой большой скоростью на весь объем, что происходит резкое увеличение температуры и давления. Такой характер процесса называют взрывным горением или просто взрывом. В этих случаях говорят о верхнем и нижнем пределах взрываемости смеси, имея в виду, что во всем диапазоне концентраций между верхним и нижним пределами готовая газовоздушная смесь способна к взрыву. Температура смеси, начиная с которой система способна к самоускорению реакции, называется температурой воспламенения.
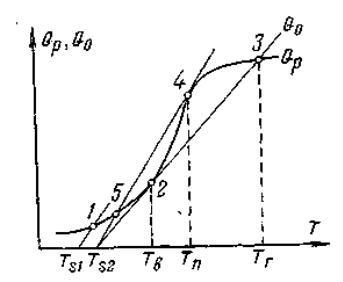
Рис.3.2. Графическое определение температуры воспламенения (Тв), горения
(Тг) и потухания (Тп) при заданной температуре поверхности теплоотвода
(Тs).
33
Соотношение тепловыделения и теплоотвода при различных уровнях температуры горючей смеси можно изобразить графически (рис.3.2). Выделение теплоты на начальном этапе химической реакции можно определить из уравнения:
Q |
k |
0 |
e E/ RTCm V q |
(3.7) |
р |
|
гор см |
|
Количество теплоты, отводимой из зоны реакции, находят по уравне-
нию:
Q0 αS T Ts |
(3.8) |
В формулах (3.7) и (3.8) Сгор–концентрация горючего вещества; Vсм – объем готовой горючей смеси; q –тепловой эффект реакции на единицу массы горючего; α – коэффициент теплоотдачи; S –поверхность охлаждающих стен; T, Ts –температура горючей смеси и охлаждающих стен.
Кривая тепловыделения на начальном этапе реакции представляет со-
бой экспоненту со значительным ростом Qp. В области высоких температур рост Qp тормозится возможностями подвода окислителя, т. е. условиями смешения. Линия теплоотвода, если принять α=const, будет представлять собой прямую с углом наклона, определяемым коэффициентом α.
Если первоначально нагреть горючую смесь в камере и окружающие ее стенки до Ts1, то за счет тепловыделения при реакции смесь примет темпера-
туру T1>Ts1 в точке Qp= Q0 и дальнейший разогрев смеси невозможен. Состояние в точке 1 характеризуется незначительным тепловыделением и низкой температурой. Эта область медленного окисления, которое может продолжаться длительно.
Повысим температуру охлаждающих стен до Ts2. Снова первоначально
Qp> Q0 и температура смеси растет. Наконец, в точке 2 Qp= Q0 однако, в отличие от точки 1 состояние здесь неустойчиво. Достаточно небольшого уве-
личения температуры, как снова Qp> Q0, и тепловыделение растет быстрее отвода теплоты. Температура в точке 2 и является температурой воспламене-
ния Тв. Далее процесс реакции быстро нарастает до состояния (точка 3) устойчивого высокотемпературного процесса окисления – горения. Этот процесс будет устойчивым, пока обеспечивается подвод горючего и окислителя. Если в последующем начать усиленный отвод теплоты (более крутая линия
Q0), то температура горения будет снижаться и затем в точке 4 высокотемпе-
ратурный процесс оборвется, так как Q0 станет больше Qp во всей области
