Результаты эксперимента
В итоге проведения
эксперимента был получен файл данных,
представляющих собой зависимость рН
раствора от длительности эксперимента.
|
Время, сек. |
pH |
Время, сек. |
pH |
Время, сек. |
pH |
|
0,009 |
6,4379248 |
126,544 |
4,5226085 |
470,308 |
4,1961342 |
|
8,963 |
6,6860453 |
171,82 |
4,4311957 |
515,584 |
4,1787222 |
|
63,236 |
4,7576701 |
180,958 |
4,4224897 |
615,049 |
4,1438983 |
|
72,374 |
4,6967282 |
235,166 |
4,3571949 |
624,187 |
4,1395453 |
|
117,613 |
4,5400205 |
244,305 |
4,3484889 |
687,514 |
4,1264863 |
Вещество: 0.01М
раствор CH3COOH.
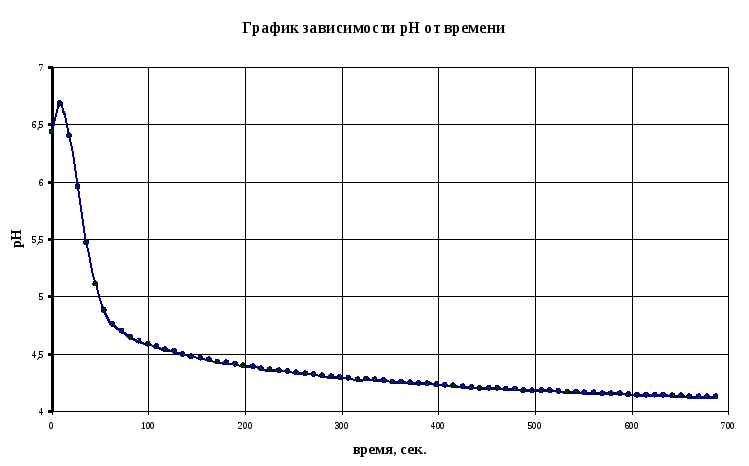
Если длительность
эксперимента умножить на скорость
подвода раствора кислоты, получим объем
введенного раствора кислоты:
Vкисл
=
q
= 600 с * 0.01894 мл/с = 11.364 [мл]
Затем следует
перейти к концентрации кислоты в
растворе:
С=Со
Vс/(Vс
+Vo)
= 0.01 моль/л * 11.364 мл / (11.364 мл + 50 мл) = 0.001852
моль/л
где Vo
-исходный объем воды в стаканчике, [мл]
Со
-концентрация соли, [моль/л]
От водородного
показателя необходимо перейти к
концентрации ионов водорода, обусловленной
диссоциацией введенной кислоты:
[H+]=
10-pH
- 10-рНо
= 10-4,1265
– 10-7
= 0.00007463 [моль/л]
где
рНо
- водородный показатель в исходном
растворе
и, наконец,
рассчитать степень диссоциации:
=
[H+]
/ С
=
0.00007463 /
0.001852
= 0.0403
Для расчета
константы диссоциации можно воспользоваться
линейной аппроксимацией зависимости
степени гидролиза от концентрации в
координатах [H+]
-
 .
.
Вид зависимости
в указанных координатах позволяет
судить о точности эксперимента и
пределах, в которых применимо приближенное
выражение для константы равновесия.
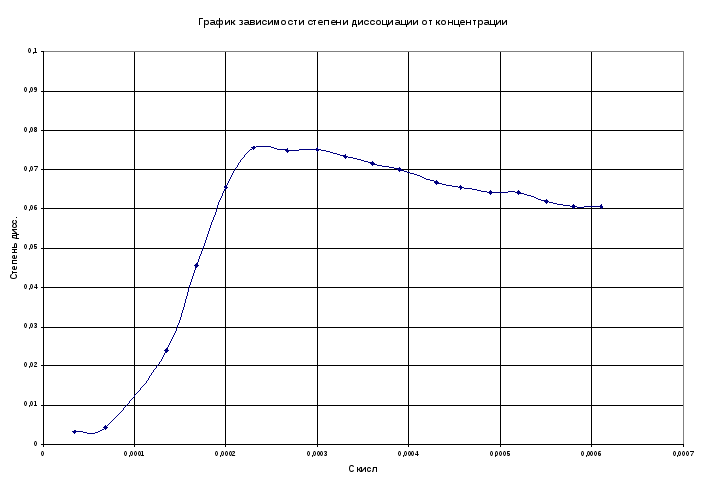
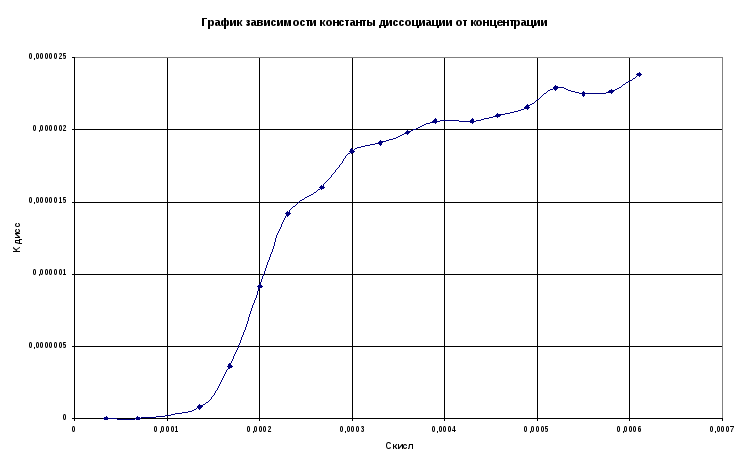
Полученное среднее
значение константы диссоциации:
К дисс = 1,5382 * 10
-6
Справочное
значение константы диссоциации:
К дисс = 1,754 * 10
-5
Вывод:
В
результате данной работы мы определили
константу и степень диссоциации уксусной
кислоты. В ходе эксперимента подтвердилось,
что степень диссоциации обратно
пропорциональна
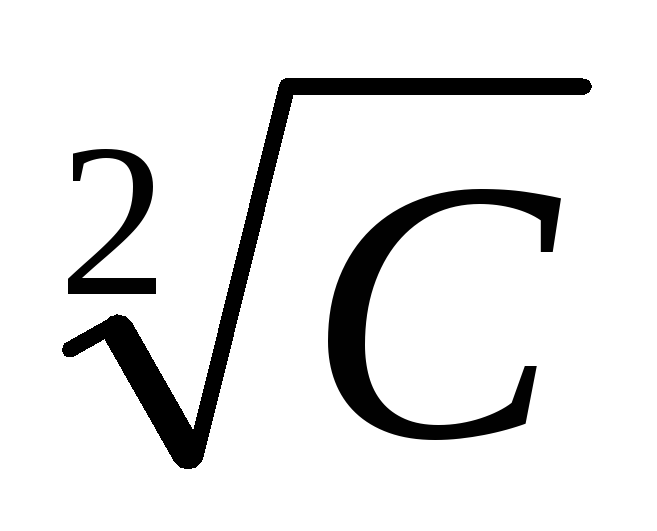 .
Различие в экспериментальной и справочной
константах диссоциации состоит в том,
что используемая в эксперименте кислота
была очень разбавленной. ( С кисл =
0.001852 моль/л )
.
Различие в экспериментальной и справочной
константах диссоциации состоит в том,
что используемая в эксперименте кислота
была очень разбавленной. ( С кисл =
0.001852 моль/л )




