
Архив ZIP - WinRAR (2) / Материаловедение Экзамен / билет 1
.docxБИЛЕТ 1
1) Диаграмма Fe-C
Основными сплавами на основе железа являются стали и чугуны – сплавы системы железо-углерод
5.1. Компоненты и фазы в системе Fe-C
Железо: Тпл=1539ºС, две модификации Feα c ОЦК-решёткой, а=0,286 нм, существует до 910ºС и Feγ с ГЦК-решеткой существует в диапазоне 910..1392ºС. Железо ферромагнитно при температурах ниже 768ºС (точка Кюри).
Углерод: элемент IV группы таблицы Д.И. Менделеева, с железом образует твердые растворы внедрения и химическое соединение Fe3C.
Фазы: жидкий раствор, феррит, аустенит, цементит, графит.
Феррит – твердый раствор углерода в Feα.
Аустенит – твердый раствор углерода в Feγ.
Цементит – Fe3С (6,67% С) – карбид
железа, решетка сложная ромбическая,
высокая твердость, хрупок, Тпл=1250˚С .
Цементит - метастабильная фаза, при
высокой температуре разлагается на
железо и графит.
.
Цементит - метастабильная фаза, при
высокой температуре разлагается на
железо и графит.
Графит – углерод в твердом состоянии. Графит – стабильная фаза, плотность - 2,5 г/см3, решетка гексагональная, слоистая, анизотропен, низкая твердость и прочность, высокая химическая стойкость. Графит присутствует в качестве самостоятельной фазы в серых чугунах
В реальных условиях охлаждения углерод в железоуглеродистых сплавах находится в метастабильной фазе в виде цементита Fe3C. Диаграмма Fe-Fe3C соответствует метастабильному равновесию системы железо-углерод.
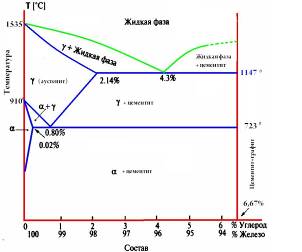
Рис. 5.1. Диаграмма состояния железо-цементит (метастабильная)
Основные критические точки и линии диаграммы (рис. 19):
точка А – температура плавления чистого железа 1539°С;
точка D – температура плавления цементита 1250°С;
точка G – 910°С (А3) – температура полиморфного α↔γ превращения железа;
точка N – 1392°С (А4) – температура полиморфного γ↔δ превращения железа;
ABCD – линия ликвидус;
AJECF – линия солидус;
ES – линия переменной растворимости углерода в аустените;
PQ – линия переменной растворимости углерода в феррите;
точка Е – предельная растворимость углерода в аустените (2,14% С);
точка Р – предельная растворимость углерода в феррите (0,02% С);
Влияние углерода и постоянных примесей на свойства стали
Чем больше содержание углерода в стали, тем выше её прочность и твёрдость, а пластичность и вязкость ниже (рис. 25). При содержании С>0,8% прочность падает из-за образования по границам зёрен хрупкой цементитной сетки (см. рис. 20 з).
Постоянные примеси попадают в сталь в процессе выплавки.
Полезные примеси: Mn от 0,3 до 0,8% и Si до 0,4%. Кремний повышает предел текучести, но снижает пластичность, марганец повышает прочность, не снижая пластичности.
Вредные примеси: сера, фосфор и газы
(О2, Н2, N2 ).
Сера вызывает красноломкость –
разрушение металла при горячей обработке
давлением (1000…1200˚С). Марганец связывает
серу в более тугоплавкое соединение
MnS, предупреждая
красноломкость. Фосфор способствует
хладноломкости стали, каждая 0,01% Р
повышает порог хладноломкости на
20…25˚С. Газы охрупчивают сталь.
).
Сера вызывает красноломкость –
разрушение металла при горячей обработке
давлением (1000…1200˚С). Марганец связывает
серу в более тугоплавкое соединение
MnS, предупреждая
красноломкость. Фосфор способствует
хладноломкости стали, каждая 0,01% Р
повышает порог хладноломкости на
20…25˚С. Газы охрупчивают сталь.
2) Отпуск стали
Отпуск – нагрев закаленной стали до температур ниже АС1, выдержка и охлаждение. Цель отпуска – получение окончательной структуры и свойств стали. Отпуск основан на превращениях мартенсита при нагреве (см. п. 6.3), в результате которых происходит изменение структуры и свойств стали (рис. 43).
Различают три вида отпуска (табл.3). Окончательная термообработка, назначаемая изделию для придания требуемых свойств, состоит из закалки и последующего отпуска. Закалку с низким отпуском применяют для деталей машин и инструмента, от которых требуются высокая твердость и износостойкость. Закалку с последующим средним отпуском – для изделий с повышенными упругими свойствами. Закалку с высоким отпуском (улучшение) – для деталей, работающих при повышенных динамических (ударных) и циклических нагрузках.
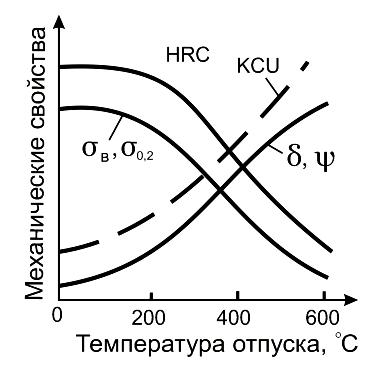
Рис. 43. Влияние температуры отпуска на механические свойства закаленной стали
Таблица 3 Характеристика видов отпуска
Виды отпуска |
Температура, °С |
Структура |
Свойства |
Применение |
Низкий |
150…250 |
Мотп |
HRC, σв |
Инструмент,подшипники, детали после ХТО и ТВЧ |
Средний |
350…500 |
Тотп |
σупр, σ-1 |
Рессоры, пружины |
Высокий |
500…680 |
Сотп |
КС |
Валы, оси, шатуны |
3) Деформируемые алюминиевые сплавы
Деформируемые алюминиевые сплавы, не упрочняемые термообработкой
К этим сплавам относятся сплавы алюминия с марганцем (АМц2), содержащие 1…1,6% Mn, и магнием (АМг2, АМг6), содержащие 2…7%Mg. Структура этих сплавов в равновесном состоянии - твердый раствор легирующих элементов в алюминии. Упрочняют сплавы путем пластической деформации (нагартовки).
Свойства:
легко обрабатываются давлением;
хорошо свариваются;
обладают высокой коррозионной стойкостью;
обработка резанием затруднена.
Применяются эти сплавы для изготовления строительных конструкций (витражи, двери, оконные рамы и т.д.), емкостей для жидкостей (баки для бензина), палубных надстроек речных и морских судов.
Деформируемые алюминиевые сплавы, упрочняемые термообработкой
Дуралюмины (Д1, Д3, Д6, Д16 и т.п.) – сплавы системы Al-Cu. Основным легирующим элементом является медь. Сплав Д1 содержит 3,8…4,8%Cu, 0,5…1,5% магния, ~0,5% марганца. Согласно диаграмме Al-Cu (рис. 9.1.) в сплавах образуются следующие фазы:
α – твердый раствор меди в алюминии, максимальная растворимость Cu в Al составляет 5,7%;
θ –твердый раствор на основе химического соединения СuAl2, содержащего 54,1%Cu.
Структура сплава Д1 в равновесном состоянии (после литья) α + θII, причем частицы θII располагаются по границам зерен и охрупчивают сплав (рис. 9.2. а).
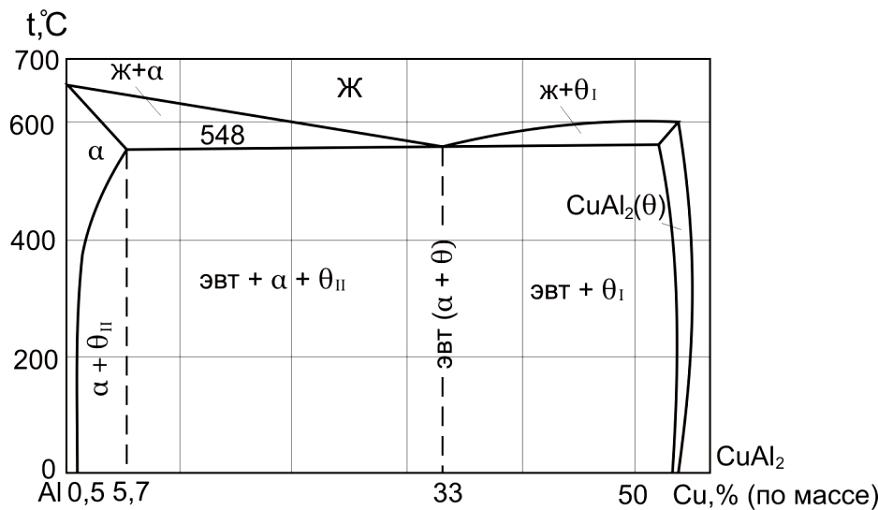
Рис.9.1. Диаграмма состояния Al-Cu.
Для упрочнения дуралюминов проводится термическая обработка: закалка + старение. Закалка заключается в нагреве до температуры ~ 500°С, при которой хрупкая избыточная θII-фаза полностью растворяется в α-твердом растворе, быстрое охлаждение фиксирует структуру пересыщенного твердого раствора меди в алюминии (рис. 9.2 б, 9.2 а).



а) б) в)
Рис.9.2. Микроструктуры дуралюмина: а – после литья (α + θII), б – после закалки (α-твердый раствор), в - после закалки и старения.
Для повышения прочности закаленного сплава проводят старение. Старение – это упрочнение закаленного сплава за счет распада пересыщенного твердого раствора и выделения избыточных вторичных фаз в мелкодисперсном виде (дисперсионное твердение).
Естественное старение заключается в выдержке закаленного сплава при комнатной температуре 5…7 суток. Искусственное старение заключается в выдержке при повышенной температуре 100…200°С в течение 10…24 часов.
Процесс старения идет в 3 стадии:
На первой стадии старения атомы меди образуют скопления в кристаллической решетке α–твердого раствора - зоны Гинье-Престона (зоны ГП) (рис. 48 б), что вызывает искажения кристаллической решетки и, следовательно, повышение прочности сплава (рис. 49).
На второй стадии старения по мере выдержки сплава при повышенных температурах образуется метастабильная θ'-фаза, близкая по составу к CuAl2, имеющая свою кристаллическую решетку, которая сохраняет когерентные связи с решеткой α-твердого раствора (рис. 48 в). Это усиливает искажения кристаллической решетки, твердость и прочность сплава повышается (рис. 9.3).
На третьей стадии старения при дальнейшей выдержке происходит срыв когерентности и выделение частиц стабильной θ–фазы (CuAl2) (рис. 9.2. г). Искажения кристаллической решетки частично снимаются, и прочность сплава понижается (рис. 49).
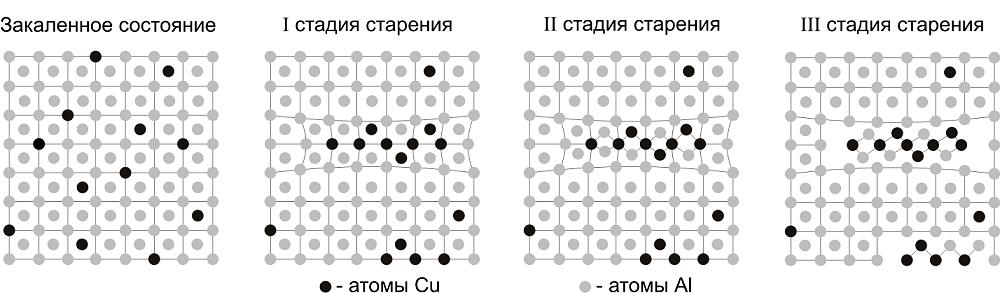
а) б) в) г)
Рис.9.3. Влияние температуры и длительности старения на прочность алюминиевых сплавов
4) Сталь 12ХН3А
По назначению – конструкционная
Состав – 0,12 % углерода, около 1 % хрома, 3% никеля, А – высококачественная
По химическому составу – легированная
По содержанию С – низкоуглеродистая, цементуемая (0,1 – 0,3% С)
По классу – перлитный
Термообработка: цементация + закалка + низкий отпуск. Структура на поверхности: Мотп+ЦII+АОСТ, твердость поверхности 58…64 HRC. Структура сердцевины зависит от химического состава стали.
