- •Нормальное ускорение
- •Полное ускорение
- •Первый закон Ньютона
- •Второй закон Ньютона
- •Третий закон Ньютона
- •5.Момент инерции. Момент импульса. Момент силы. Основной закон динамики вращательного двидения.
- •6. Термодинамические параметры. Уравнение Менделеева-Клапейрона.
- •7. Изопроцессы. Адиабатический процесс. Их уравнения и графики.
- •Изобарный процесс
- •Изохорный процесс
- •Изотермический процесс
- •Адиабатический процесс
- •8. Первое начало термодинамики и его применение к изопроцессам и адиабатическому процессу.
- •Формулировка
- •9. Теплоемкости удельная, молярная Ср и Сv. Уравнение Майера.
- •Уравнение Майера
- •10. Круговой процесс. Цикл Карно. Кпд тепловой машины.
- •11. Напряженность и потенциал электрического поля. Закон Кулона.
- •12. Электроемкость. Конденсаторы. Энергия конденсатора. Соединение конденсаторов.
- •14. Магнитное поле. Закон Био-Савара-Лапласа.
- •15. Магнитный поток. Теорема Остроградского-Гаусса для магнитного поля.
- •16. Сила Лоренца. Эффект Холла.
- •18. Диа-,ферро- и парамагнетики. Явление магнитного гистерезиса.
- •19. Гармонические колебания. Уравнение гармонических колебаний. Период колебаний математического и физического маятников и колебательного контура.
- •Виды колебаний
- •Уравнение гармонических колебаний
- •Период физического маятника — твердое тело, совершающее колебания в гравитационном поле вокруг горизонтальной оси подвеса, расположенной выше его центра тяжести.
- •20. Бегущие и стоячие волны.
- •21, Электромагнитные волны. Шкала э/м волн. Монохроматические волны. Дисперсия света.
- •Шкала электромагнитных волн
- •22. Интерференция света. Условия максимума и минимума. Кольца Ньютона.
- •23. Дифракция света. Принцип Гюйгенса-Френеля. Ход лучей на дифракционной решетке.
- •24. Поляризация света. Виды поляризации. Закон Малюса.
- •25. Закон Брюстера. Двойное лучепреломление.
- •26. Тепловое излучение и его характеристики. Законы теплового излучения.
- •Основные свойства теплового излучения
- •Основные понятия и характеристики теплового излучения
- •Общий вид закона смещения Вина
- •27. Фотоэффект. Законы фотоэффекта. Уравнение Эйнштейна.
- •28. Строение атома. Постулаты Бора. Излучение и поглощение.
- •29. Строение ядра. Закон радиоактивного распада.
7. Изопроцессы. Адиабатический процесс. Их уравнения и графики.
Изопроцессы — термодинамические процессы, во время которых количество вещества и ещё одна из физических величин — параметров состояния: давление, объёмили температура — остаются неизменными. Так, неизменному давлению соответствует изобарный процесс, объёму — изохорный, температуре — изотермический,энтропии — изоэнтропийный (например, обратимый адиабатический процесс). Линии, изображающие данные процессы на какой-либо термодинамической диаграмме, называются изобара, изохора, изотерма и адиабата соответственно. Изопроцессы являются частными случаями политропного процесса.
Изобарный процесс
Изобарный
процесс (др.-греч.
ισος, isos — «одинаковый» + βαρος,
baros — «вес») — процесс изменения
состояния термодинамической системы
при постоянном давлении (![]() )
)
![]()
Зависимость объёма газа от температуры при неизменном давлении была экспериментально исследована в 1802 году Жозефом Луи Гей-Люссаком. Закон Гей-Люссака: При постоянном давлении и неизменных значениях массы газа и его молярной массы, отношение объёма газа к его абсолютной температуре остаётся постоянным: V/T = const.
Изохорный процесс
Основная статья: Изохорный процесс
Изохорный процесс (от
греч. хора — занимаемое место) —
процесс изменения состояния
термодинамической системы при постоянном
объёме (![]() ).
Для идеальных газов изохорический
процесс описывается законом
Шарля:
для данной массы газа при постоянном
объёме, давление прямо пропорционально
температуре:
).
Для идеальных газов изохорический
процесс описывается законом
Шарля:
для данной массы газа при постоянном
объёме, давление прямо пропорционально
температуре:
![]()
Линия, изображающая изохорный процесс на диаграмме, называется изохорой.
Ещё стоит указать что поданная к газу энергия расходуется на изменение внутренней энергии то есть Q = 3* ν*R*T/2=3*V*ΔP, где R — универсальная газовая постоянная, ν количество молей в газе, T температура в Кельвинах, V объём газа, ΔP приращение изменения давления. а линию, изображающая изохорный процесс на диаграмме, в осях Р(Т), стоит продлить и пунктиром соединить с началом координат, так как может возникнуть недопонимание.
Изотермический процесс
Изотермический
процесс (от
греч. «термос» — тёплый, горячий) —
процесс изменения состояния
термодинамической системы при постоянной
температуре (![]() )(
)(![]() ).
Изотермический процесс описывается законом
Бойля — Мариотта:
).
Изотермический процесс описывается законом
Бойля — Мариотта:
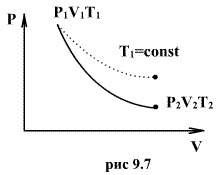
При постоянной температуре и неизменных значениях массы газа и его молярной массы, произведение объёма газа на его давление остаётся постоянным: PV = const.

![]()
Графики изопроцессов в различных системах координат
Адиабатический процесс
Адиабатический
процесс - это такое изменение состояний
газа, при котором он не отдает и не
поглощает извне теплоты. Следовательно,
адиабатический процесс характеризуется
отсутствием теплообмена газа с окружающей
средой. Адиабатическими можно считать
быстро протекающие процессы. Так как
передачи теплоты при адиабатическом
процессе не происходит, то ![]() и
уравнение I начала термодинамики
принимает вид
и
уравнение I начала термодинамики
принимает вид
|
|
(9.20) |
или
![]()
т.е. внешняя работа газа может производиться вследствие изменения его внутренней энергии. Адиабатное расширение газа (dV>0) сопровождается положительной внешней работой, но при этом внутренняя энергия уменьшается и газ охлаждается (dT<0).