
Таблица определения катионов и анионов
.pdf
|
|
КАТИОНЫ |
|
|
Таблица |
|
Реактив |
|
|
Ионы (определяемые) |
|
|
|
|
Na+ |
K+ |
|
Ag+ |
Mg+ |
Ca+ |
Пламя |
Пламя - желтое |
Пламя - фиолетовое (через |
|
|
|
Пламя- кирпично-красное |
|
|
синее стекло - пурпурно- |
|
|
|
|
|
|
красное) |
|
|
|
|
Цинкуранил-ацетат |
Подкисляют развед. CH3COOH |
|
|
|
|
|
|
– желтый кристаллический |
|
|
|
|
|
Zn (Uo2)3(CH3COOH)8 |
осадок (или зеленовато- |
|
|
|
|
|
|
желтый) |
|
|
|
|
|
|
Na Zn(UO2)3(CH3COOH) 9H2O |
|
|
|
|
|
|
Такой же результат на соли |
|
|
|
|
|
|
лития |
|
|
|
|
|
Винная кислота – |
|
В растворе CH3COONa с эта- |
|
|
|
|
C4H 6O6 |
|
нолом – белый кристалличе- |
|
|
|
|
|
|
ский осадок растворяется в |
|
|
|
|
|
|
развед. минеральных кислотах |
|
|
|
|
|
|
и растворах едких щелочей |
|
|
|
|
Кобальтинитрит натрия |
|
Удаляют соли аммония прока- |
|
|
|
|
(гексанитрокобальт |
|
ливанием. С уксусной кисло- |
|
|
|
|
натрия) |
|
той – желтый кристалличе- |
|
|
|
|
Na3 Co(NO2)6 |
|
ский осадок K2Na Co(NO2)6 |
|
|
|
|
Хлорид-ион |
|
|
C 2% раствором AgNO3 – |
|
|
|
|
|
|
белый творожистый оса- |
|
|
|
Cl- |
|
|
док AgCl, |
нерастворимый в |
|
|
|
|
|
HNO3, растворим в р-ре |
|
|
|
|
|
|
аммиака - Ag(NH3 Cl |
|
|
|
Формальдегид |
|
|
Растворяют осадок, образо- |
|
|
|
|
|
|
вавшийся от NH4OH и Ag- |
|
|
|
HCHO |
|
|
NO3, избытком NH4OH, |
|
|
|
|
|
|
добавляют формальдегид, |
|
|
|
|
|
|
нагревают – «серебряное |
|
|
|
|
|
|
зеркало» - Ag |
|
|
|
Фосфат натрия |
|
|
|
|
Mg++Na2HPO4+NH4OH |
|
|
|
|
|
|
NH4Cl MgNH4PO4 +2Na |
|
Na2HPO4 + NH4OH |
|
|
|
|
+H2O белый кристалличе- |
|
|
|
|
|
|
ский осадок |
|
Оксалат аммония |
|
|
|
|
|
Ca2++(NH4)2→CaC2O4 +2NH4+ |
(NH4)2C2O4 |
|
|
|
|
|
Белый осадок н/р в разв. |
|
|
|
|
|
|
CH3COOH, расnв. в разб. |
|
|
|
|
|
|
мин к-тах |
Продолжение таблицы (КАТИОНЫ)
Реактив |
|
|
|
|
|
|
|
|
|
|
Ионы (определяемые) |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
Zn2+ |
|
|
|
|
Hg2+ |
|
NH4+ |
|
Bi3+ |
|
Fe2+ |
|
Fe3+ |
|
|
||||
Na2S |
2+ |
→ |
ZnS +2Na |
+ |
2+ |
→ |
HgS +2Na |
+ |
|
Растворяют в развед HCl, |
2+ |
2-→ |
FeS -черный |
3+ |
2-→ |
Fe2S3 - |
|||||
Сульфид натрия |
Zn |
+Na2S |
|
Hg |
+Na2S |
|
|
к фильтрату доб.Na2S – |
Fe +S |
|
2Fe +S |
|
|||||||||
Белый осадок, н/р в развед. |
Коричнево-черный |
|
|
осадок н/р в развед мин |
черный осадок раств в |
||||||||||||||||
|
CH3COOH, л.р. в развед. |
осадок, н/р в развед |
|
|
коричнево-черный оса- |
|
к-тах |
развед мин к-тах |
|||||||||||||
|
|
HCl |
|
|
|
HNO3(в ГФXI не вклю- |
|
док Bi2S3 |
раствоим в рав- |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
ном объеме HNO3 конц. |
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
чена) |
|
|
|
|
|
|
|
|
|
|
|||
K4Fe(CN)6 ферроцианид |
Zn2++ K4Fe(CN)6 → |
|
|
|
|
|
|
|
|
|
|
|
Fe3++ K4Fe(CN)6 → |
||||||||
калия |
ZnK2Fe(CN)6+2K |
+ |
белый |
|
|
|
|
|
|
|
|
|
|
KFe Fe(CN)6 |
+ |
3K+ |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
студенистый осадок, н/р в |
|
|
|
|
|
|
|
|
|
|
синий осадок |
|
||||||||
|
|
разб. HCl |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
K3Fe(CN)6 феррицианид |
|
|
|
|
|
|
|
|
|
|
|
|
|
Fe2++ K3Fe(CN)6 →2K++ |
|
|
|
|
|
||
калия |
|
|
|
|
|
|
|
|
|
|
|
|
|
KFe Fe(CN)6 -синий |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
осадок |
|
|
|
|
|
|
NH4NCS |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Fe3++3(NH4NCS)→ |
||||
Аммоний роданистый |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3NH4 |
+Fe(NCS)3 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Красное окрашивание |
||||
KJ |
|
|
|
|
|
|
Hg2++2KJ→HgJ2+2K+ |
|
|
Переводят в сульфат, |
|
|
|
|
|
|
|
|
|||
Калия иодид (по каплям) |
|
|
|
|
|
|
Красный осадок( |
|
|
Bi3++3KJ→3K++BiJ3 черн |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
окрашивание) |
|
|
ый осадок, с избытком KJ |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
далее:HgJ2+2KJ→ |
|
|
осадок переходит в жел- |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
K2HgJ4 -бесцветный |
|
то-оранжевый раствор: |
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
BiJ3+KJ→KBiJ4 |
|
|
|
|
|
|
|
|
|
NaOH |
|
|
|
|
|
|
HgCl2+2NaOH→HgO |
NH4Cl+NaOH→NH3↑+ |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
+2NaCl+H2O |
|
NaCl+H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Желтый осадок |
|
Запах, посинение |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
красной лакмусовой |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
бумаги |
|
|
|
|
|
|
|
|
|
|
АНИОНЫ
|
|
|
|
|
|
|
|
|
|
|
|
Таблица |
|
|
Реактив |
|
|
Ионы (определяемые) |
|
|
|||||
|
|
|
|
|
|
|
|
Арсенит-ион (As3+) |
Арсенат-ион (As5+) |
Бромид-ион (Br-) |
Иодид-ион (J-) |
Хлорид-ион (Cl ) |
Ион серебра (Ag- |
Желтый осадок |
Шоколадный осадок Ag3AsO4, |
В растворе, подкисленном |
В растворе HNO3 –желтый |
C раствором AgNO3 – белый |
|||||||
|
|
|
|
NO3) |
(Ag3AsO3) раство- |
растворим в развед. HNO3 и рас- |
HNO3 – желтоватый тво- |
творожистый осадок, нерас- |
творожистый осадок AgCl, |
|||
|
|
|
|
|
|
|
|
рим в развед. HNO3 |
творе аммиака |
рожистый осадок, трудно |
творим в растворе аммиака, |
нерастворимый в HNO3, раство- |
|
|
|
|
|
|
|
|
и растворе аммиака |
|
растворим в растворе аммиака, |
HNO3 |
рим в р-ре аммиака - Ag(NH3)2 Cl |
|
|
|
|
|
|
|
|
|
|
нерастворим в р-ре HNO3 |
|
При испытании подлинности |
|
|
|
|
|
|
|
|
|
|
|
|
гидрохлоридов орг. оснований |
|
|
|
|
|
|
|
|
|
|
|
|
растворимость осадка устанавли- |
|
|
|
|
|
|
|
|
|
|
|
|
вают после отделения и промыва- |
|
|
|
|
|
|
|
|
|
|
|
|
ния его водой |
|
Хлорамин |
|
|
С р-ром HCl и ХЛФ – |
|
|
||||||
|
|
|
|
|
|
SO |
2N Cl |
|
|
хлороформный слой стано- |
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
вится желто-бурым |
|
|
||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
Na |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|||||||
Нитрит натрия |
|
|
|
С развед. H2SO4 и ХЛФ – |
|
|||||||
|
|
(NaNO2) |
|
|
|
хлороформный слой стано- |
|
|||||
(Или р-р FeCl3) |
|
|
|
вится фиолетовым |
|
|||||||
|
|
H2SO4 |
|
|
|
Нагревание с конц. H2SO4 – |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
фиолетовые пары иода |
|
Сульфид-ион (S2-) |
В развед. HCl – |
В развед. HCl после нагрева -– |
|
|
|
|||||||
|
|
|
|
|
|
|
|
желтый осадок |
желтый осадок As2S3 |
|
|
|
|
|
|
|
|
|
|
|
As2S3 |
(образующийся H2S восстанавли- |
|
|
|
|
|
|
|
|
|
|
|
нерастворим в конц. |
вает As5+ до As3+, который и дает |
|
|
|
|
|
|
|
|
|
|
|
HCl, растворим в р- |
осадок) нерастворим в конц.HCl, |
|
|
|
|
|
|
|
|
|
|
|
ре аммиака |
растворим в р-ре аммиака |
|
|
|
Молибдат аммония |
|
Не фармакопейный: |
|
|
|
|||||||
(NH4)2MoO3) |
|
В кислой среде (HNO3) с молибде- |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
новой жидкостью |
|
|
|
|
|
|
|
|
|
|
|
|
((NH4)2MoO4+NH4NO3+HNO3) – |
|
|
|
|
|
|
|
|
|
|
|
|
желтый осадок |
|
|
|
|
|
|
|
|
|
|
|
|
(NH4)3H4 As(Mo2O7)6 |
|
|
|
|
|
|
|
|
|
|
|
|
As3+ не реагирует |
|
|
|
Сульфат магния |
|
С магнезиальной смесью (NH4Cl, |
|
|
|
|||||||
|
|
(MgSO4) |
|
NH4OH, MgSO4 - белый кристал- |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
лический осадок MgNH4AsO4, |
|
|
|
|
|
|
|
|
|
|
|
|
растворим в соляной к-те. |
|
|
|
|
|
|
|
|
|
|
|
|
С As3+ осадка нет |
|
|
|
|
|
|
|
|
|
|
|
Продолжение таблицы (АНИОНЫ) |
|
|
|
Реактив |
|
|
Ионы (определяемые) |
|
|
|
|
|
|
Фосфат-ион (PO43-) |
Сульфат-ион (SO42-) |
Нитрит -ион NO2- |
Нитрат-ион NO3- |
Карбонат (бикарбонат)-ион |
|
|
|
|
|
|
|
|
CO32- (HCO3-) |
Ион серебра (AgNO3) |
|
С развед. HCl –белый |
|
|
|
|||
|
|
|
|
|
осадок, нерастворим в |
|
|
|
|
|
|
|
|
разведенных к-тах |
|
|
|
Ион серебра (AgNO3) |
В нейтральной среде – |
|
|
|
|
|||
|
|
|
|
желтый осадок (Ag3PO4), |
|
|
|
|
|
|
|
|
растворим в развед. HNO3 |
и |
|
|
|
|
|
|
|
р-ре аммиака |
|
|
|
|
|
Сульфат магния |
В буферном растворе (1 мл |
|
|
|
|||
|
|
(MgSO4) |
р-ра NH4Cl и 1 мл р-ра |
|
|
|
|
|
|
|
|
|
NH4OH) - белый кристал- |
|
|
|
|
|
|
|
|
лический осадок |
|
|
|
|
|
|
|
|
MgNH4PO4, растворимый в |
|
|
|
|
|
|
|
|
уксусной к-те и разведенных |
|
|
|
|
|
|
|
|
минеральных кислотах |
|
|
|
|
|
Молибдат аммония |
В кислой среде (развед. |
|
|
|
|
||
|
(NH4)2MoO3) |
HNO3) –желтый кристал- |
|
|
|
|||
|
|
|
|
лический осадок |
|
|
|
|
|
|
|
|
(NH4)3PO4 12MoO3, раство- |
|
|
|
|
|
|
|
|
рим в р-ре аммиака |
|
|
|
|
|
|
|
H2SO4 |
|
|
Желто-бурые пары NO↑ и |
|
С р-ром H2SO4 выделяется CO2, с |
|
|
|
|
|
|
NO2↑ |
|
известковой водой CO2 дает: бе- |
|
|
|
|
|
|
|
|
лый осадок CaCO3 |
|
Фенолфталеин |
|
|
|
|
Красное окрашивание (в отличие |
||
|
|
|
|
|
|
|
|
от HCO3-) |
|
Дифениламин |
|
|
Синее окрашивание |
Синее окрашивание |
|
||
|
|
|
KMnO4 |
|
|
Обесцвечивание р-ра KMnO4, |
|
|
|
|
|
|
|
|
подкисленного H2SO4 |
|
|
Cu с конц.H2SO4 |
|
|
Бурые пары NO2 |
|
|
|||
|
|
|
CH3 |
|
|
Зеленое окрашивание (отли- |
|
|
O |
N |
N |
CH3 |
|
|
чие от NO3-) |
|
|
|
|
|
|
|
|
|
||
|
|
|
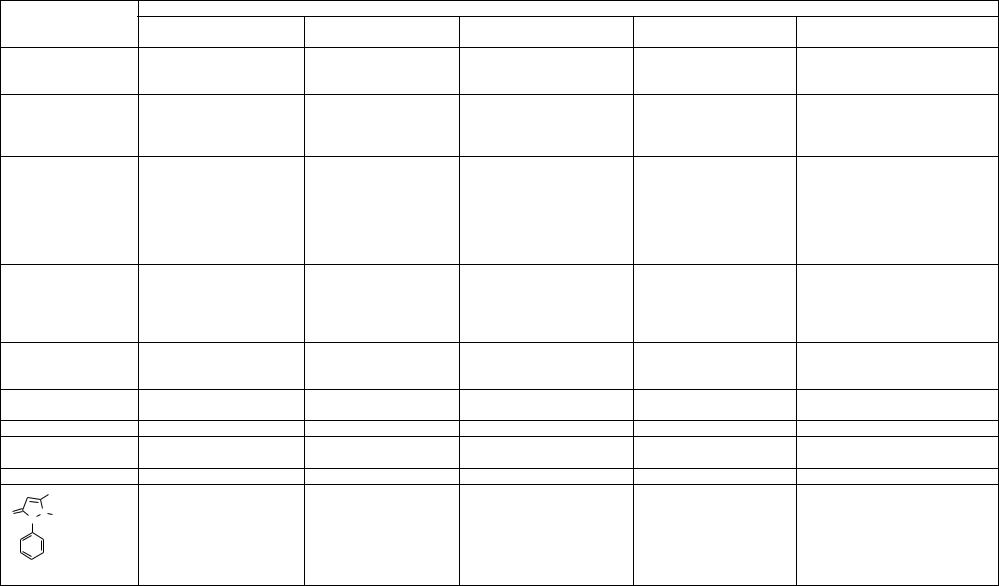
Антипирин |
|
|
|
|
|
в развед HCl |
|
|
|
|
|
|||
