
- •Квантовая химия Библиографический список
- •Семинарские занятия
- •Практические (компьютерные) занятия
- •Конспект лекций по квантовой химии
- •Конспект лекций по квантовой химии
- •1.1 Принципы квантовой механики
- •1.2 Вариационный принцип. Решение уравнения Шредингера
- •1.3 Приближение независимых частиц
- •1.4 Метод самосогласованного поля
- •1.5 Приближение центрального поля
- •1.6 Атомные орбитали и их характеристики
- •1.7 Антисимметричность электронной волновой функции
- •1.8 Детерминант Слейтера
- •1.9 Метод Хартри-Фока
- •1.10 Ограниченный и неограниченный методы Хартри-Фока
- •1.11 Квантовохимическая трактовка решений уравнений Хартри-Фока
- •1.12 Электронные конфигурации атомов с точки зрения квантовой химии
- •2. Квантовая химия молекул
- •2.1 Введение
- •2.2 Приближение Борна-Оппенгеймера
- •2.3 Метод Хартри-Фока для молекул
- •2.4. Приближение мо лкао. Уравнения Рутана.
- •2.5 Ограничения метода хф
- •2.5 Ограничения метода хф
- •2.7 Метод конфигурационного взаимодействия
- •2.8 Метод многоконфигурационного взаимодействия. Теорема Бриллюэна
- •2.9 Теория возмущений
- •2.10 Метод валентных связей
- •2.11 Точность учета электронной корреляции
- •2.12. Расчет энергии диссоциации химических связей
- •2.13. Иерархия методов квантовой химии
- •2.14 Неэмпирическая квантовая химия
- •2.15 Базисные функции для неэмпирических расчетов
- •2.15.1 Вид аналитических базисных функций
- •2.15.2. Номенклатура базисных наборов
- •2.15.3 Минимальный базисный набор
- •2.15.4 Расширенный базисный набор
- •2.15.5 Поляризационные и диффузные функции
- •2.15.6 Базисные наборы Попла
- •2.17. Роль базисных функций в описании свойств молекул
- •2.16. Полуэмпирическая квантовая химия
- •2.17. Метод Полного Пренебрежения Дифференциальным Перекрыванием (ппдп или cndo).
- •2.18. Метод Частичного (или Промежуточного) Пренебрежения Дифференциальным Перекрыванием (indo).
- •2.19 Метод Модифицированного Частичного (или Промежуточного) Пренебрежения Дифференциальным Перекрыванием (mindo).
- •2.20. Метод Модифицированного Пренебрежения Дифференциальным Перекрыванием (mndo).
- •2.21 Разделение - и -электронов. -электроннное приближение
- •2.22. Метод Парризера-Попла-Парра
- •2.23. Метод мо Хюккеля
- •2.24 Расширенный метод Хюккеля
- •2.25 Точность квантовохимических расчетов химических свойств молекул
- •3.1. Орбитальная картина химической связи
- •3.1.1. Конструктивная и деструктивная интерференция орбиталей
- •3.1.2. Молекулярные орбитали и их симметрийная классификация.
- •3.1.3. Электронные конфигурации двухатомных молекул
- •3.1.4. Анализ заселенностей орбиталей по Малликену. Понятие о зарядах и порядках связей.
- •3.2. Пространственное распределение электронной плотности
- •3.2.1. Деформационная электронная плотность
- •3.2.2.Топологическая теория
- •3.3. Электростатический и энергетический аспекты описания химической связи
- •3.4. Многоатомные молекулы
- •3.4.1. Локализация и гибридизация орбиталей
- •3.4.2.Модель отталкивания электронных пар Гиллеспи и строение молекул
- •3.5.Химическая связь в координационных соединениях
- •3.5.1.Теория кристаллического поля и теория поля лигандов
- •3.5.2. Спектрохимический ряд
- •3.5.4 Комплексы сильного и слабого полей. Магнитные свойства комплексов
- •3.5.4. Энергия стабилизации кристаллическим полем
- •3.5.5. Теория поля лигандов
- •Электронные заселенности орбиталей Сr в Сr(со)6
- •3.5.6. Правило 18 электронов
- •Эффект Яна-Теллера
- •Химические реакции в газовой фазе
- •Путь химической реакции.
- •Теория переходного состояния химической реакции.
- •Квантовохимическое описание химических реакций в жидкой и твердой фазе
- •Роль орбитальной симметрии
- •Индексы реакционной способности.
- •Метод граничных орбиталей. Теория жестких и мягких кислот и оснований.
- •Абсолютная жесткость и абсолютная мягкость молекулярных систем.
- •Функции Фукуи.
- •Энергия диссоциации химической связи в молекулярной системе.
- •Орбитальные модели взаимодействия молекул с поверхностью. Хемосорбция
- •Квантовая химия каталитических реакций
- •Квантовая химия каталитических реакций
- •5 Электронная структура твердых тел
- •Одноэлектронные волновые функции в бесконечных периодических кристаллах и методы их расчета
- •Кластерные методы
- •Квантовая химия атома
- •Лекции по курсу "Квантовая химия"
2.22. Метод Парризера-Попла-Парра
Объединение нулевого дифференциального перекрывания и -электронного приближения приводит к методу Парризера-Попла-Парра, дающего прекрасные результаты для -электронных систем. Матричные элементы оператора Фока для этого метода приведены в табл. 2.16. U равно потенциалу ионизации атома в соответствующем валентном состоянии, взятому с обратным знаком: - I . Одноцентровые кулоновские интегралы оцениваются по формуле Паризера-Парра (2.66). Величины I и A , необходимые для расчета U и определяют из спектроскопических данных для валентных состояний атомов, используя модель локализованных связей. Двухцентровые интегралы AB рассчитывают по формулам (2.67)-(2.68). Величины h считаются параметрами и выбираются по разному для расчета свойств основного (метод Попла) и возбужденных (метод Парризера-Парра) состояний.
Для основного состояния h являются резонансными интегралами = kS , где k подбирается так, чтобы наилучшим образом воспроизводить теплоты образования в представительном круге соединений (существует и ряд других параметризаций).
2) Для возбужденных состояний следует учесть, что волновая функция молекулы должна быть суммой волновых функций основного 0 и возбужденных i k состояний: = 0 + аi k i k. Обычно учитывают несколько однократно возбужденных электронных конфигураций заданной мультиплетности и ищут коэффициенты аi k вариационным методом. Матричные элементы ( 0 h 0) дают энергию основного состояния Е0, а элементы ( i k h j l) имеют вид:
( i k h j l) h i k, j l = kl k - ij i +2(jk li)-(jk il). (2.70)
В приближении НДП
h i k, j l = ij kl ( k - i) + [2(1-R)с j с l c i с k - с j с i с k c l], (2.71)
где R=0 для синглетных состояний и R=1 – для триплетных.
 Расчет
проводится методом ССП, причем вначале
определяют МО для основного состояния,
а затем, используя их, строят волновые
функции возбужденных состояний.
Расчет
проводится методом ССП, причем вначале
определяют МО для основного состояния,
а затем, используя их, строят волновые
функции возбужденных состояний.
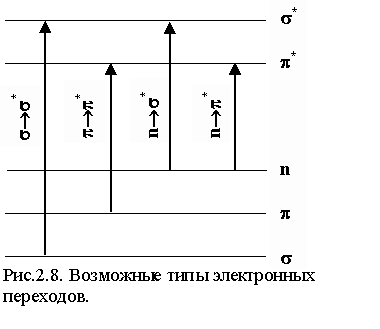
Метод Парризера-Попла-Парра включает в себя метод КВ и очень хорошо зарекомендовал себя как при определении геометрии, потенциалов ионизации и сродства к электрону, так и при расчетах оптических спектров поглощения сопряженных органических молекул. Спектр поглощения состоит из нескольких полос, связанных с определенными электронными переходами. Для плоских молекул МО можно разделить на три группы: , и n* . Наболее вероятное относительное расположение соответствующих энергетических уровней и разрешенные правилами отбора типы электронных переходов показаны на рис. 2.8. Диагонализизация матрицы h i k, j l называемой матрицей конфигурационного взаимодействия, дает энергии спектральных переходов и веса возбужденных конфигураций аi k. Ориентированный на -электроны, метод ППП хорошо описывает - * переходы (рис. 2.9.): точность оценки синглет-синглетных переходов составляет 0,1-0,2 эВ или 3-5% .
 Интенсивность
полосы поглощения f определяется
квадратом дипольного момента перехода
и равна f =К
аi
k c
i с
k
x
2.
Она оценивается методом ППП с ошибкой
40-50%.
Интенсивность
полосы поглощения f определяется
квадратом дипольного момента перехода
и равна f =К
аi
k c
i с
k
x
2.
Она оценивается методом ППП с ошибкой
40-50%.
