
- •ХИМИЯ И ФИЗИКА ПОЛИМЕРОВ
- •1.1. ВОПРОСЫ ДЛЯ ДОПУСКА К ЛАБОРАТОРНЫМ РАБОТАМ
- •ЛИТЕРАТУРА
- •1.5.ПЛАН КОЛЛОКВИУМА:
- •ЛИТЕРАТУРА
- •2.ПОЛУЧЕНИЕ ПОЛИМЕРОВ
- •2.1.ВОПРОСЫ ДЛЯ ДОПУСКА К ЛАБОРАТОРНЫМ РАБОТАМ
- •ЛИТЕРАТУРА
- •Таблица 2
- •Таблица 3
- •2.4.ПЛАН КОЛЛОКВИУМА
- •ЛИТЕРАТУРА
- •3.ФИЗИКА ЭЛАСТОМЕРОВ.
- •3.1.ВОПРОСЫ ДЛЯ ДОПУСКА К ЛАБОРАТОРНЫМ РАБОТАМ.
- •ЛИТЕРАТУРА
- •Длина образца, мм
- •Относительное удлинение, %
- •3.5. ПЛАН КОЛЛОКВИУМА
- •ЛИТЕРАТУРА
- •4.ИЗУЧЕНИЕ ПРОЦЕССА ОКИСЛЕНИЯ ЭЛАСТОМЕРОВ
- •4.1.ВОПРОСЫ ДЛЯ ДОПУСКА К ЛАБОРАТОРНЫМ РАБОТАМ.
- •ЛИТЕРАТУРА
- •4.4.ПЛАН КОЛЛОКВИУМА
- •ЛИТЕРАТУРА
- •5.ИССЛЕДОВАНИЕ ПРОЦЕССА ВУЛКАНИЗАЦИИ ЭЛАСТОМЕРОВ
- •5.1.ВОПРОСЫ ДЛЯ ДОПУСКА К ЛАБОРАТОРНЫМ РАБОТАМ.
- •ЛИТЕРАТУРАа
- •5.2.ЛАБОРАТОРНАЯ РАБОТА ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ СВОБОДНОЙ И СВЯЗАННОЙ СЕРЫ.
- •Таблица 11Константы для расчета Мс
- •ЛИТЕРАТУРА
- •5.4.ПЛАН КОЛЛОКВИУМА
- •ЛИТЕРАТУРА
|
|
|
|
|
32 |
|
|
|
|
|
|
замещения |
в |
эластомерах: взаимодействие |
полимеров |
с |
соединениями, |
||||||
содержащими сульфгидрильную группу; с соединениями,содержащими кратные |
|||||||||||
связи; |
реакции |
эластомеров |
с |
галогеноводородами,галогенами,водородом. |
|||||||
Химические |
превращения эластомеров |
под |
влиянием |
физических |
воздействий |
||||||
(тепла,механических напряжений,световой энергии,ионизирующих излучений). |
|||||||||||
3.Кинетика |
и |
механизм |
окисления |
|
эластомеров |
молек |
|||||
кислородом.Факторы,влияющие на процесс окисления.Катализаторы и |
|
|
|||||||||
ингибиторы |
окисления,механизм |
их |
действия.Структурные |
|
превращен |
||||||
эластомеров при окислении.Влияние структуры эластомера и условии окисления |
|||||||||||
на |
направление |
|
процесса |
окисления.Пластикация |
как |
механохимичес |
|||||
деструкция каучука. |
|
|
|
|
|
|
|
|
|
||
ЛИТЕРАТУРА |
|
|
|
|
|
|
|
|
|
||
1.Кулезнев В. |
Н. |
Химия и |
физика полимеров. /В. |
Н. |
Кулезнев, В. |
А. |
|||||
Шершнев. - М: Высшая школа, 1988. - 312с 2.Догадкин Б. А. Химия эластомеров. /Б. А. Догадкин, А. А. Донцов, В. А.
Шершнев. - М.: Химия, 1981. - 376с.
3.Тугов И. И. Химия и физика полимеров. /И. И, Тугов, Г. И. Кострыкина. -
М.: Химия, 1989. - 432с.
4.Тагер А. А. Физикохимия полимеров. - М.: Химия, 1978. - 544с.
5.ИССЛЕДОВАНИЕ ПРОЦЕССА ВУЛКАНИЗАЦИИ ЭЛАСТОМЕРОВ
Основой процесса вулканизации является изменение структуры эластомера, связанное с образованием пространственной сетки. В процессе вулканизации эластомер приобретает типичные свойства вулканизатов: эластичность, отсутствие растворимости, термическую устойчивость.
Вулканизация приводит к существенному увеличению прочности эластомера, повышению напряжения при заданном удлинении(модуля); уменьшаются
остаточные деформации, относительное удлинение |
и гистерезисные |
потери |
||||
эластомера. |
|
|
|
|
|
|
Наиболее распространенным способом вулканизации является серная. |
|
|||||
В |
процессе |
вулканизации |
происходит |
весьма |
сложное |
химиче |
взаимодействие активных групп эластомера с компонентами вулканизующей системы. В результате этого взаимодействия образуются поперечные связи
различной |
плотности (длина |
молекулярных |
цепей |
между |
уз |
вулканизационной сетки различна) и различного |
химического |
соста, |
ва |
||
частности, поперечные связи различаются по степени сульфидности. Структура вулканизата, сформировавшаяся в процессе вулканизации, определяет свойства вулканизата. Наилучшим комплексом свойств характеризуются вулканизаты с широким набором связей (-S-, -S-S-, -SX-, -C-C-).
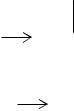
Существует несколько способов изучения процесса вулканизации. К химическим методам относятся различные способы определения скорост присоединения вулканизующего агента, например, серы в процессе вулканизации.
33
Скорость изменения числа поперечных связей в процессе вулканизации характеризует скорость вулканизации и может быть измерена по изменению равновесной степени набухания.
При вулканизации наряду с процессами сшивания молекулярных цепей протекают процессы деструкции. Скорость процессов деструкции и сшивания при вулканизации можно оценить методом золь-гель анализа.
5.1.ВОПРОСЫ ДЛЯ ДОПУСКА К ЛАБОРАТОРНЫМ РАБОТАМ.
1.Понятие о процессе вулканизации.
2.Изменение свойств каучука при вулканизации.
3.Кинетика присоединения серы к каучуку.
4.Методы определения степени вулканизации.
ЛИТЕРАТУРАа
1.Догадкин Б.А. и др. Химия эластомеров.-М.:Химия,1981. - 376с. 2.Кулезнев В. Н. Химия и физика полимеров. /В. Н. Кулезнев, В. А. Шершнев. - М.: Высшая школа,1982. - 312с.
5.2.ЛАБОРАТОРНАЯ РАБОТА ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ СВОБОДНОЙ И СВЯЗАННОЙ СЕРЫ.
Сера, не вступившая в реакцию, носит название свободной. Определение свободной серы в резиновых изделиях имеет большое значение для установления степени вулканизации резин. Зная общее содержание серы в резиновой смеси и
содержание свободной |
серы в вулканизате, можно по разности |
определить |
||||
процент связанной серы. |
|
|
|
|
|
|
Метод основан на извлечении свободной серы из резины раствором сульфита |
||||||
натрия, адсорбции |
активированным |
углем |
ускорителей |
и |
продуктов |
|
разложения с последующим йодометрическим титрованием раствора. |
|
|
||||
Очевидно, при кипячении сера взаимодействует с сульфитом по реакции: S + Na2SO3  Na2S2O3
Na2S2O3
Образовавшийся гипосульфит оттитровывается йодом
I2 + 2Na2S2O3  Na2S4O6 + 2NaI
Na2S4O6 + 2NaI
Для связывания избытка сульфита натрия добавляется формалин
OSO2Na
Na2SO3 + H2CO + H2O |
H2C-OH + NaOH |
Выделившийся едкий натр нейтрализуют уксусной кислотой
NaOH + CH3COOH |
CH3COONa H2O |

34
Методика работы.
2 г резины ,измельченной до 1-3 мм, помещают в колбу и заливают100 мл свежеприготовленного 5-%-ного раствора сульфита натрия. Раствор с навеской нагревают до кипения в колбе с обратным холодильником и выдерживают при температуре кипения в течение2-х часов. Затем по охлаждении раствора добавляют 3 г активированного угля и колбу с содержимым периодически встряхивают в течение 30 минут.
После обработки углем раствор фильтруют через бумажный фильтр. Колбу и
содержимое |
воронки промывают |
дистиллированной водой( 3 раза по 10 |
мл).Затем к |
фильтрату добавляют5 мл 40%-ного раствора формалина и через5 |
|
минут приливают 1-2 капли раствора |
фенолфталеина,10 мл 20%-ной уксусной |
|
кислоты (до кислой реакции и обесцвечивания индикатора) и тотчас титруют 0,1- н раствором йода в присутствии крахмала до появления быстро исчезающего синего окрашивания. Одновременно с проведением анализа ставят"холостой" опыт (как указано выше, но без навески резины).
Обработка результатов
Содержание свободной серы вычисляют по формуле
Sсвоб = (a - b)× K ×0,003206 ×100 , %
H
H
где а- количество 0,1н раствора йода, израсходованного на титрование навески, мл.
b- количество 0,1н раствора йода, израсходованного на "холостой" опыт, мл, Н- навеска резины,г.
К- фактор 0,1н раствора йода, 0,003206количество г серы, соответствующее 1 мл 0,1н раствора йода.
Результаты опыта оформляются в виде табл. 10.
Таблица 10.
Определение содержания свободной и связанной серы
Шифр |
Время |
Навеска |
Количество |
Количество |
Общее |
Содержа |
Содер |
образца, |
вулкани |
резины, |
йода, |
йода, |
содержание |
ние |
жание |
состав |
зации |
г |
пошедшее |
пошедшее |
серы в |
свобод- |
связан |
смеси |
|
|
на |
на |
резиновой |
ной |
ной |
|
|
|
холостой |
титрование |
смеси, % |
серы, |
серы, |
|
|
|
опыт (b), |
, (а), мл |
|
|
% |
|
|
|
мл |
|
|
|
|
|
|
|
|
|
|
|
|
35
Строится график зависимости содержания свободной и связанной серы в вулканизате от времени вулканизации.
Литература
1.Хераскова Е. П. Определение свободной серы в резинах различными методами.// Методы анализа сырья и материалов, применяемых в резиновой промышленности: Сб. - М.: 1959. - с.4-6.
5.3.ЛАБОРАТОРНАЯ РАБОТА "ОПРЕДЕЛЕНИЕ ЧИСЛА ПОПЕРЕЧНЫХ СВЯЗЕЙ МЕТОДОМ РАВНОВЕСНОГО НАБУХАНИЯ".
По величине равновесного набухания вулканизата можно судить о степени вулканизации резин. В отличие от невулканизованного каучука, растворяющегося
вопределенных растворителях, для пространственных полимеров характерно ограниченное набухание, т.е. увеличение массы и объема вулканизата до определенного значения (так называемого максимума набухания). На величину максимума набухания влияет густота молекулярной сетки, так как с увеличением
ввулканизате мостичных связей молекулам растворителя труднее проникать между молекулами каучука. Таким образом ,чем больше степень сшивания, тем меньше максимум набухания эластомера.
|
|
Методика работы |
|
|
|
|
|
Для |
определения |
степени |
равновесного |
набухания |
из |
вулкан |
|
вырезаются образцы ( по два для параллельного опыта) размером 10х10х2мм и |
|||||||
взвешиваются на аналитических весах. Взвешенные образцы помещаются в бюкс, |
|||||||
наливаются соответствующим растворителем |
и |
оставляются |
для набухания. |
||||
После |
достижения |
равновесной |
степени |
набухания(масса |
образца |
не |
|

36
изменяется)образец вынимается из растворителя, высушивается фильтровальной бумагой и взвешивается в закрытом бюксе. Равновесная степень набухания рассчитывается по уравнению:
Q = rk × Pнаб - Pнач ,
rр × Pнач × F
где rk , rр -плотность растворителя и каучука соответственно, г/см3 ;
Pнач, Pнаб -начальная масса и масса набухшего образца, г ;
F -относительное содержание углеводорода каучука в образце, содержащим нерастворимые в применяемом растворителе ингредиенты(по рецепту). Вычисляется по уравнению
100масс.ч.
F =
сумма ингредиентов в рецепте, масс. ч.
Объемную долю каучука в набухшем вулканизате определяют по формуле
1
Vk = 1 + Qравн
где Q равн.-равновесная степень набухания.
Между средней молекулярной массой отрезка молекулярной (Мc),заключенного между двумя поперечными связями и объемной долей каучука (Vк) существует следующая зависимость:
M c |
= - |
rr ×Vr × (Vk 13 |
- 0,5 ×Vk ) |
|
|
|
2 + 2,303 ×lg(1 -Vk |
) |
|||
|
Vk + m ×Vk |
||||
где Мc - cредняя молекулярная масса отрезка цепи между двумя соседними связями ,г/моль,
rк - плотность каучука, г/см3 ,
Vр - молярный объем растворителя ,см3/моль ,
m - параметр, характерезующий взаимодействие между каучуком и средой, в которой происходит набухание.
Константы rк, Vр, m находятся в таблице 11.
Количество поперечных связей ,приходящихся на 1 см3 вулканизата, рассчитывается по формуле
nc = 6,023 ×1023 ×rk 2 × M c
Результаты испытаний оформляются в виде таблиц и графиков.
