
- •Метрология
- •Рекомендуемая литература
- •Internet-ресурсы
- •Теоретическая часть Содержание компонента в пробе вещества объекта анализа
- •Концентрация компонента в жидком и газообразном веществе
- •Измерение концентрации – специфический вид измерений в метрологии
- •Способы сравнения с эталоном при измерения концентрации компонента
- •Вещество сравнения
- •Стандартные растворы
- •Градуировочные растворы
- •Экспериментальная часть
- •Порядок выполнения работы
Способы сравнения с эталоном при измерения концентрации компонента
Согласно основным положениям науки об измерениях – метрологии, измерение физической величины есть ничто иное, как сравнение размера величины с эталоном этой величины, размер которой принят за единицу измерения, и получение значения этой величины.
Узнать неизвестное содержание компонента А (провести химический анализ) в пробе анализируемого вещества можно только путем сравнения с эталоном – с пробой вещества сравнения, в котором содержание определяемого компонента А или какого-либо другого компонента известно с наивысшей точностью, и желательно, схожим по составу с анализируемым веществом.
Реализовано два способа сравнения количества частиц определяемого компонента с эталоном числа частиц (с единицей измерения числа частиц 1 моль):
– химический способ, реализованный в химических методах химического анализа;
– физический способ, реализованный в физических методах химического анализа.
Химический способ реализован в способе сравнения с эталоном единицы величины количества частиц компонента, построенном на использовании законов сохранения массы или количества компонента при химических взаимодействиях и законе постоянства химического состава. Химические взаимодействия основаны на химических свойствах химических частиц. Для определения искомого компонента в пробе анализируемого вещества проводят химическую реакцию, отвечающую определенным требованиям, и измеряют массу (методы гравиметрии) или объём (методы титриметрии) компонентов, участвующих в данной химической реакции. Количественные отношения получают из закона сохранения массы элементов (гравиметрия) или закона эквивалентов компонентов (методы титриметрии) для данной химической реакции.
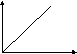
Физический способ реализован в способе сравнения с эталоном единицы величины количества частиц компонента путем измерения физического свойства компонента А, зависящего от его химической природы и содержания в пробе анализируемого вещества. Экспериментально устанавливают функциональную зависимость «Интенсивность физического свойства – содержание компонента А в пробе вещества сравнения» путем градуировки средства измерения этого физического свойства по определяемому компоненту А. Количественные отношения получают из градуировочного графика, построенного в координатах: «интенсивность физического свойства – концентрация определяемого компонента А», рис.1.
 I
I
Ix--- -- --- -- I
I
I
C(А)x C(А)
Рис.1. Вид типичного градуировочного графика
в физических методах химического анализа
Множество анализируемых веществ и широкий диапазон измеряемых концентраций обусловили возникновение многочисленных и чрезвычайно разнообразных методов измерений, основанных на использовании различных физико-химических явлений и свойств вещества.
Физические методы химического анализа веществ основаны на измерении оптических, рентгеновских, радиоактивных, радиоволновых, электрических, магнитных, электромагнитных, теплофизических, механических, акустических свойствах компонентов.
