
- •5. Определение компонентного состава газов методом хроматографии
- •5.1. Физические основы и аппаратная реализация метода газовой хроматографии
- •Принципиальная схема хроматографа
- •Система подготовки газа-носителя
- •Дозирующие устройства
- •Хроматографические колонки
- •Детекторы
- •Система термостатирования
- •Программирование температуры
- •Регистрация результатов анализа
- •Газ-носитель
- •Неподвижная фаза
- •5.2. Хроматографический метод определения компонентного состава газов
- •Аппаратура
- •Отбор и хранение проб
- •Отбор проб газа на анализ
- •Подготовка и проведение анализа
- •Обработка результатов
- •Точность метода
- •5.3. Задание для самостоятельной работы
- •5.4. Расчетная часть
- •5.4.1. Способы выражения состава смесей и связь между ними [21]
- •5.4.2. Расчет свойств газа по компонентному составу [21]
- •5.5. Приложение
- •Контрольные вопросы
5.3. Задание для самостоятельной работы
По рассчитанному из хроматограммы объемному (мольному) составу газа, вычислить:
состав газа в массовых единицах;
молярную массу смеси газов;
плотность смеси газов при нормальных и стандартных условиях тремя способами;
относительную плотность смеси газов при нормальных и стандартных условиях;
рассчитать и построить температурную зависимость плотности газа, считая его идеальным, при давлении 2 МПа и температурах 0, 10, 20, 40, 50 °С;
рассчитать и построить температурную зависимость плотности газа, считая его реальным, при давлениях 2 и 20 МПа и температурах 0, 10, 20, 40, 50 °С;*
сделать вывод по влиянию учета состояния (идеальный, реальный) газа на величину его плотности.
* – Температурные зависимости плотности для идеального и реального газов при давлении 2 МПа построить на одном графике.
Полученные результаты по расчету свойств газа представить в сводной табл. 5.6.
Таблица 5.6
Свойства исследованного газа
|
Свойства |
Размерность |
Значение | |
|
Плотность |
при н.у. |
кг/м3 |
|
|
при с.у. |
кг/м3 |
| |
|
Относительная плотность |
- |
| |
|
Молекулярная масса |
г/моль |
| |
Расчет температурной зависимости плотности газа представить в виде отдельных таблиц (табл. 5.9, 5.10).
5.4. Расчетная часть
5.4.1. Способы выражения состава смесей и связь между ними [21]
Массовая доля– массаi-го компонента, отнесенная к общей массе системы:
 (5.7)
(5.7)
Молярная (мольная) доля– число молейi-го компонента, отнесенное к общему числу молей в системе:
 (5.8)
(5.8)
Моль– количество вещества в граммах, численно равное его молекулярной массе.
Число молейравно массе веществаmi, деленной на молекулярную массуMi:
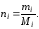 (5.9)
(5.9)
Тогда:
 (5.10)
(5.10)
 (5.11)
(5.11)
 (5.12)
(5.12)
Объемная доля– отношение объемаi-го компонента в системе к общему объему системы:
 (5.13)
(5.13)
Тогда:
 (5.14)
(5.14)
 (5.15)
(5.15)
По закону Авогадро при одинаковых давлении и температуре 1 мольлюбого газа занимает одинаковый объем:
при н.у. – 273 К и 0,101 МПа – 22,414 л, при с.у. – 293 К и 0,101 МПа – 24,055 л.
Поэтому для газовых смесейобъемный состав является и молярным составом:
 . (5.16)
. (5.16)
5.4.2. Расчет свойств газа по компонентному составу [21]
5.4.2.1.Средняя молекулярная масса газовой смесиможет быть вычислена по составу:
 (5.17)
(5.17)
где уi=viилиNi в долях единицы и по формуле:
 (5.18)
(5.18)
где yi=viилиNi в процентах.
Тогда весовая доля компонента:
 (5.19)
(5.19)
Кроме того:
 (5.20)
(5.20)
 (5.21)
(5.21)
5.4.2.2. Плотность газовой смеси, как аддитивное свойство, можно рассчитать по составу газа и плотности каждого компонента:
 (5.22)
(5.22)
где yi=Niилиvi в долях единицы;ρi– плотность компонента.
Плотность компонентов газа можно взять из справочников (табл. 6.11) или рассчитать через молярный объем – объем 1 моля газа. Тогда плотность смеси газов:
при нормальных условиях (н.у.):
 (5.23)
(5.23)
при стандартных условиях (с.у.):
 (5.24)
(5.24)
при условиях отличных от н.у. или с.у., например, в условиях сепаратора, трубопровода и т. д., плотность может быть определена из уравнения состояния реальных газов с учетом коэффициента сверхсжимаемостиZ:
 (5.25)
(5.25)
где Ро,То– давление (Па) и температура (К) при нормальных условиях,Р,Т– давление и температура при рабочих условиях.
Коэффициент сверхсжимаемости Zхарактеризует отклонение свойств реального газа от свойств идеального газа при одинаковых давлении и температуре.
6.4.2.3. Относительная плотность газапредставляет собой отношение массы газа к массе такого же объема воздуха:
 (5.26)
(5.26)
где 1,293 и 1,205 – плотность воздуха, кг/м3, при н.у. и с.у., соответственно.
5.4.2.4. Коэффициенты сверхсжимаемости реальных газовопределяют экспериментально или с определенной степенью точности они могут быть взяты из графика (рис. 5.15).
Чтобы воспользоваться графиком, необходимо иметь данные о приведенных псевдокритических значениях давления и температуры [30]. Для этого сначала определим псевдокритические (средние критические) давление и температуру:
 (5.27)
(5.27)
 (5.28)
(5.28)
где Pr и Tr – псевдокритические давление и температура, соответственно; yi – объемное или мольное содержание компонента в смеси; PCi и TCi – критические давления и температуры компонентов газа (табл. 5.12).
Затем находим величины приведенныхпсевдокритическихзначений давления и температуры по соотношениям:
 (5.29)
(5.29)
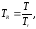 (5.30)
(5.30)
где PRиTR– соответственно значения приведенных псевдокритических давления и температуры;PиT– абсолютные значения давления, Па, и температуры,К, при которых находится газ.
На основании найденных значений PRиTRпо графику (рис. 5.15) определим величину коэффициента сверхсжимаемостиZ.

Рис. 5.11. Зависимость коэффициента сжимаемости углеводородного газа от приведенных псевдокритических давлений и температур: цифры на кривых – значения приведенной псевдокритической температуры
Таблица 5.7
Таблица для записи результатов расчета свойств исследованного газа
|
Компоненты |
Объемная доля компонента, vi |
Молярная масса компонента, Mi |
Вклад компонента в молярную массу смеси |
Плотность компонента, кг/м3 |
Вклад компонента в плотность смеси, кг/м3 |
Относительная плотность смеси | |||||
|
при н.у. |
при с.у. |
при н.у. |
при с.у. |
при н.у. |
при с.у. | ||||||
|
Метан и неуглев. компоненты |
|
|
|
|
|
|
|
|
| ||
|
Диоксид углерода |
|
|
|
|
|
|
| ||||
|
Этан |
|
|
|
|
|
|
| ||||
|
Пропан |
|
|
|
|
|
|
| ||||
|
i-Бутан |
|
|
|
|
|
|
| ||||
|
n-Бутан |
|
|
|
|
|
|
| ||||
|
i-Пентан |
|
|
|
|
|
|
| ||||
|
n-Пентан |
|
|
|
|
|
|
| ||||
|
i-Гексан |
|
|
|
|
|
|
| ||||
|
n-Гексан |
|
|
|
|
|
|
| ||||
|
Сумма (свойство) |
|
|
|
|
|
|
|
|
| ||
Таблица 5.8
Таблица для записи результатов расчета коэффициента сверхсжимаемости для реального газа
|
Компоненты |
Объемная доля компонента, vi |
Критическое давление компонента, Pc i, МПа |
Вклад компонента в Pc смеси, МПа |
Критическая температура компонента, Tc i, К |
Вклад компонента в Tc смеси, K |
Давление смеси, МПа |
Приведенное псевдокритическое давление смеси |
Приведенная псевдокритическая температура смеси при температуре газа, оС | ||||
|
0 |
10 |
20 |
40 |
50 | ||||||||
|
Метан и неу/в комп. |
|
|
|
|
|
2 |
|
|
|
|
|
|
|
Диоксид углерода |
|
|
|
|
| |||||||
|
Этан |
|
|
|
|
|
Коэффициент сверхсжимаемости Z | ||||||
|
Пропан |
|
|
|
|
| |||||||
|
i-Бутан |
|
|
|
|
|
|
|
|
|
| ||
|
n-Бутан |
|
|
|
|
| |||||||
|
i-Пентан |
|
|
|
|
|
20 |
|
|
|
|
|
|
|
n-Пентан |
|
|
|
|
| |||||||
|
i-Гексан |
|
|
|
|
|
Коэффициент сверхсжимаемости Z | ||||||
|
n-Гексан |
|
|
|
|
|
|
|
|
|
| ||
|
Сумма (свойство) |
|
|
|
|
| |||||||
Таблица 5.9
Таблица для записи результатов расчета температурной зависимости плотности идеального газа
|
Давление смеси, МПа |
Плотность смеси при н.у., кг/м3 |
Ро, МПа |
То, К |
Температура смеси, оС |
Температура смеси, К |
Плотность, кг/м3 |
|
2 |
|
|
|
0 |
|
|
|
10 |
|
| ||||
|
20 |
|
| ||||
|
40 |
|
| ||||
|
50 |
|
|
Таблица 5.10
Таблица для записи результатов расчета температурной зависимости плотности реального газа
|
Давление смеси, МПа |
Плотность смеси при н.у., кг/м3 |
Ро, МПа |
То, К |
Температура смеси, оС |
Температура смеси, К |
Z |
Плотность, кг/м3 | |
|
2 |
|
|
|
0 |
|
|
| |
|
10 |
|
|
| |||||
|
20 |
|
|
| |||||
|
40 |
|
|
| |||||
|
50 |
|
|
| |||||
|
20 |
|
|
|
0 |
|
|
| |
|
10 |
|
|
| |||||
|
20 |
|
|
| |||||
|
40 |
|
|
| |||||
|
50 |
|
|
| |||||

