
- •Экология нефтедобывающих комплексов
- •Введение
- •Охрана атмосферы
- •1. Определение основных свойств наружной и внутренней среды
- •2. Расчеты выбросов в атмосферу загрязняющих веществ из различных источников
- •2.1. Расчет количества вредных веществ, поступающих из газового объема трубопроводов и оборудования, находящихся под давлением
- •2.2. Расчет количества вредных веществ, поступающих в атмосферный воздух при «большом» и «малом дыхании» аппарата
- •2.2.1. Расчет количества вредных веществ, поступающих в атмосферный воздух при “большом дыхании” аппарата
- •2.2.2. Расчет количества вредных веществ, поступающих в атмосферный воздух при «малом дыхании» аппарата
- •3. Расчеты элементов факельной системы и рассеивания загрязняющих веществ в атмосфере
- •3.1. Элементы факельной системы
- •3.1.1. Расчет диаметра факельной трубы
- •3.1.2. Расчет высоты факельной трубы
- •3.2. Расчет загрязнения атмосферы выбросами одиночного точечного источника
- •3.2.1. Максимальное значение приземной концентрации вредных веществ
- •3.2.2. Расстояние, на котором достигается максимальная концентрация вредных веществ
- •3.2.3. Опасная скорость ветра
- •3.2.4. Максимальное значение приземной концентрации вредных веществ с учетом скорости ветра
- •3.2.5. Расстояние, на котором достигается максимальная концентрация вредных веществ с учетом скорости ветра
- •3.2.6. Приземная концентрация вредных веществ в атмосфере по оси факела выброса
- •3.2.7. Приземная концентрация вредных веществ в атмосфере по перпендикуляру к оси факела выброса
- •3.3. Концентрация газа в воздушном пространстве вблизи поврежденного газопровода
- •II. Охрана водных ресурсов
- •4. Определение необходимой степени очистки производственных сточных вод
- •4.1. Расчет необходимой степени очистки производственных сточных вод по содержанию загрязняющих веществ
- •4.2. Расчет необходимой степени очистки производственных сточных вод по взвешенным веществам
- •4.3. Очистные сооружения для нефтесодержащих стоков
- •4.3.1. Методы очистки нефтесодержащих стоков
- •4.3.2. Подбор нефтеловушки
- •5. Оценка возможности загрязнения пресных подземных вод нижезалегающими минерализованными водами
- •6. Оценка возможности подтягивания загрязненных нефтепродуктами подземных вод к водозаборным сооружениям
- •III. Охрана литосферы
- •Способы уменьшения загрязнения и очистки грунтов
- •8. Индивидуальные задания
- •Литература
Введение
Практикум представляет собой учебное пособие к теоретическому курсу «Экология нефтедобывающих комплексов». Основное его назначение – дать возможность приложить полученные студентами знания к решению практических задач и, с другой стороны, проверить насколько усвоен теоретический материал. Примеры, собранные в данном пособии, ценны и сами по себе, поскольку служат методическим пособием по решению реальных экологических задач.
Весь материал в учебном пособии разделен на три части соответственно компонентам окружающей среды: атмосфера, воды, поверхностные и подземные, и недра. В материал каждого раздела включена справочная часть, в которой приведены основные формулы, необходимые коэффициенты, и типовые примеры, иллюстрирующие методику решения данного класса задач.
В конце практикума содержится Приложение, где представлены физико-химическая характеристика и константы некоторых химических веществ.
Для выполнения расчетов и построения графиков рекомендуется использовать EXCEL.
Охрана атмосферы
1. Определение основных свойств наружной и внутренней среды
Для расчетов количеств вредных веществ, выделяющихся из технологического оборудования в атмосферный воздух, необходимо знать основные свойства химических соединений и их смесей.
В Приложении приведены характеристические константы чистых веществ, которые используются для расчета свойств химических соединений и их смесей.
При температуре, отличающейся от 20 оС, плотность жидкости рассчитывается по формуле:
![]() (1.1)
(1.1)
где i – коэффициент температурного расширения, выражающий относительное увеличение объема жидкости при увеличении температуры на 1 оС.
Коэффициент температурного расширения капельных жидкостей незначителен. Для практических расчетов количеств вредных веществ, выделяющихся из оборудования и трубопроводов для жидкостей можно принять:
tж = ож.
Плотность газа или пара при t = 0 оC и Pо = 100 кПа рассчитывают по следующей формуле:
![]() , кг/м3
(1.2)
, кг/м3
(1.2)
где М – относительная молекулярная масса вещества, кг/(кмоль);
22,4 – объем 1 кмоля газа или пара при НУ, м3.
Для
определения плотности газа или пара
при температуре
![]() оC
и давлении
оC
и давлении
![]() кПа
используют уравнение Клапейрона:
кПа
используют уравнение Клапейрона:
![]() (1.3)
(1.3)
Динамическую
вязкость газов и паров при
![]() оC
рассчитывают по формуле:
оC
рассчитывают по формуле:
![]() (1.4)
(1.4)
где Sat – константа Сатерленда (Приложение).
В
практических расчетах для расчета
динамической вязкости жидкости tж
при
![]() оC
при определении количества вредных
веществ, выделяющихся через неплотности
соединений трубопроводов и оборудования,
можно использовать формулу Пуазейля:
оC
при определении количества вредных
веществ, выделяющихся через неплотности
соединений трубопроводов и оборудования,
можно использовать формулу Пуазейля:
![]() (1.5)
(1.5)
Изменение динамической вязкости с изменением температуры является существенным. Так, с увеличением температуры от 0 до 100 оС вязкость воды уменьшается в 7 раз.
Кинематическая вязкость (м2/с) связана с динамической вязкостью соотношением:
![]() (1.6)
(1.6)
где - динамическая вязкость, Па·с; - плотность, кг/м3.
Коэффициент диффузии, который необходим для расчетов количества выделяющихся вредных веществ из оборудования, можно рассчитать по следующей зависимости:
![]() (1.7)
(1.7)
где Dо – коэффициент диффузии при t = 0 оС и Рo = 100 кПа.
Коэффициент
диффузии при
![]() и
и![]() кПа определяют по формуле:
кПа определяют по формуле:
![]() (1.8)
(1.8)
где Ро = 100 кПа; Tо = 273 К;
Р и Т – давление и температура в оборудовании или трубопроводе.
Чтобы найти коэффициент диффузии при любой температуре, используют формулу:
![]() (1.9)
(1.9)
Часто на практике встречаются не чистые вещества, а их смеси. Состав среды в оборудовании или трубопроводе задается в массовых, объемных или мольных долях.
Мольная доля компонента:
![]() (1.10)
(1.10)
Массовые доли компонентов пересчитывают в мольные - по формуле:
![]() (1.11)
(1.11)
где Ni – мольная доля компонента;
ai – массовая доля компонента;
Мi – молекулярная масса компонента.
Когда в трубопроводе или оборудовании находится смесь жидкостей, плотность этой смеси определяют по выражению:
![]() (1.12)
(1.12)
где iж – плотность компонента.
Динамическая вязкость смеси нормальных жидкостей определяется из выражения (Па·с):
![]() (1.13)
(1.13)
где Ni – мольная доля компонента в смеси;
iж – соответствующий коэффициент динамической вязкости.
Если в трубопроводе или оборудовании находится смесь газов или парогазовоздушная смесь, то вязкость газовых (паровых) смесей можно вычислить по приближенной формуле:
![]() (1.14)
(1.14)
где Мсм,г, Мi – молекулярные массы смеси газов и отдельных компонентов;
vi – объемные (молярные) доли компонентов в смеси (viг = Niг),
см г, i - коэффициенты динамической вязкости смеси газов и отдельных компонентов.
![]() (1.15)
(1.15)
Кинематическая вязкость газовой смеси:
![]() (1.16)
(1.16)
или
![]() (1.17)
(1.17)
где i – кинематическая вязкость компонента газовой смеси.
Плотность смеси газов определяется по формуле (кг/м3):
![]() (1.18)
(1.18)
где Ni – мольные доли компонентов газовой смеси;
iг – плотность соответствующих компонентов.
При расчете количеств вредных веществ, выделяющихся со свободной поверхности жидкости, необходимо помнить, что они состоят из смеси веществ, состав которых зависит от температуры, давления, а так же от объемной (мольной) доли каждого вещества в растворе.
Давление газовой смеси над раствором равно:
![]() (1.19)
(1.19)
где Рi – парциальное давление компонента смеси.
Согласно закону Рауля парциальное давление компонента, входящего в состав смеси, определяется по формуле:
![]() (1.20)
(1.20)
где Ni – мольная доля компонента в растворе;
Рiн – давление насыщенного пара вещества над чистым компонентом при заданной температуре.
Зависимость давления насыщенного пара чистого вещества от температуры описывается уравнением:
![]() мм
рт ст (1.21)
мм
рт ст (1.21)
или
![]() (1.22)
(1.22)
значения эмпирических коэффициентов А, В, С (константы Антуана) для чистых веществ приведены в Приложении.
Парциальное давление насыщенных водяных паров в наружной среде (т.е. в газовой фазе) определяется по формуле:
![]() (1.23)
(1.23)
где t – температура наружной среды, оС.
Парциальное давление водяных паров при заданной влажности наружной среды определяется по формуле:
![]() (1.24)
(1.24)
где - влажность наружной среды, %.
Зная объемный или массовый состав смеси в оборудовании и данные о давлении насыщенных паров веществ, составляющих смесь, можно определить количественный состав газовой смеси над поверхностью жидкости. Концентрацию насыщенных паров компонента, выраженную в единицах давления, можно пересчитать в объемную концентрацию по следующей формуле:
![]() (1.25)
(1.25)
где Рi – парциальное давление компонента газовой смеси при заданной температуре и давлении, Па;
Мi – молекулярная масса данного вещества; 1 мм рт ст = 133,322 Па.
Пример 1.1. Определить параметры среды в производственном помещении.
Исходные данные: влажность в помещении φ = 60%; концентрация дихлорэтана в воздухе СД =5 мг/м3; температура t = 16 оC; давление среды В = 101,3 кПа.
Решение. Относительные молекулярные массы составляющих среды:
![]() =
28,96;
=
28,96;
![]() =
18,015;
=
18,015;![]() 98,97.
98,97.
Давление насыщения водяных паров в воздухе производственного помещения:
lg![]()
lg![]()
![]() мм
рт. ст. или 1653 Па.
мм
рт. ст. или 1653 Па.
Давление водяных паров при заданной влажности в помещении:
![]()
![]() Па.
Па.
Парциальное давление примеси (дихлорэтана):
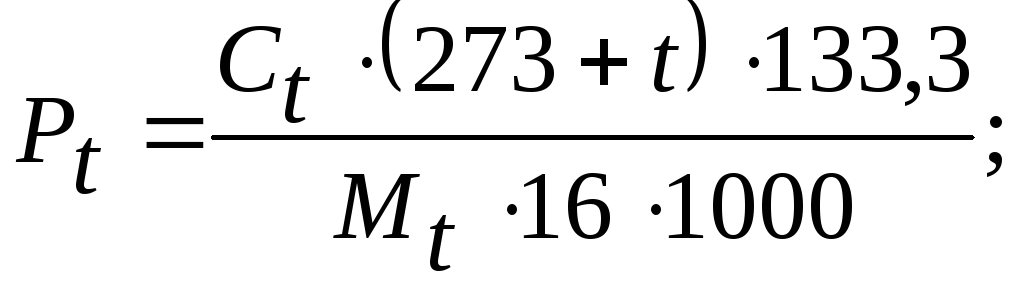
![]() Па.
Па.
Парциальное давление основного компонента наружной среды – воздуха:
![]()
![]() Па.
Па.
Мольные доли составляющих наружную среду:
![]()
NД
= 100333/101325 =
0,9902;
![]() 993/101325
= 0,00979;
993/101325
= 0,00979;
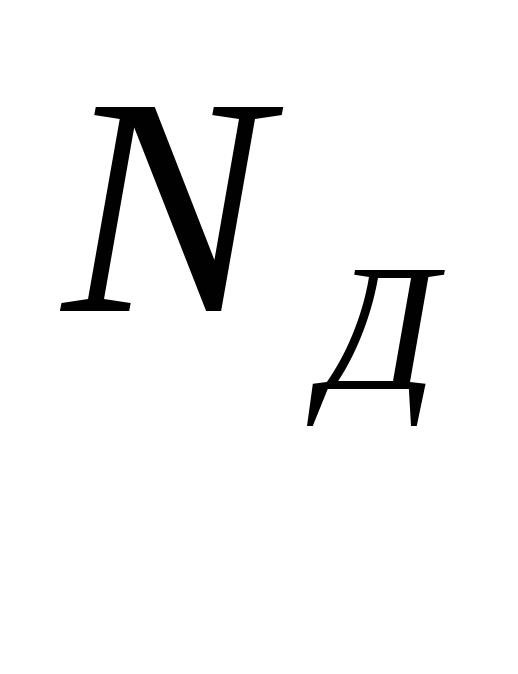 =
0,12/101325 = 0,00001
=
0,12/101325 = 0,00001
![]()
Концентрация составляющих наружной среды, мг/м3:
![]()
![]()
![]()
![]() .
.
Произведение NiPi для газовых составляющих наружной среды, мг/м3 (кг/м3):
![]() (1,207);
(1,207);
![]() (0,0074).
(0,0074).
Плотность наружной среды:
![]()
![]() =1,207+0,0074+0,000005
=1,207+0,0074+0,000005![]() 1,214
кг/м3 .
1,214
кг/м3 .![]()
Динамическая вязкость газовых составляющих при t = 0 оС, Пас, (Приложение):
![]()
![]() ;
;
![]()
Константы Сатерленда (Приложение):
![]()
![]()
![]()
![]()
![]()
Динамическая вязкость газовых составляющих при t = 16 оC, Пас;
![]()
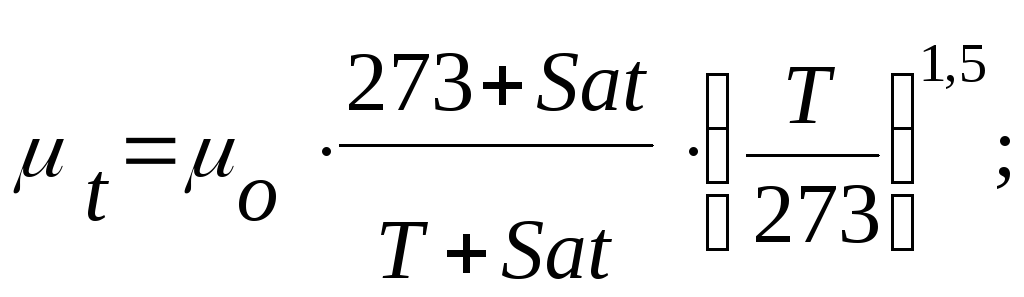
![]()
![]()
![]()
Относительная молекулярная масса смеси газов наружной среды:
![]()
![]()
![]()
![]() Динамическая
вязкость смеси газов наружной среды:
Динамическая
вязкость смеси газов наружной среды:

![]()
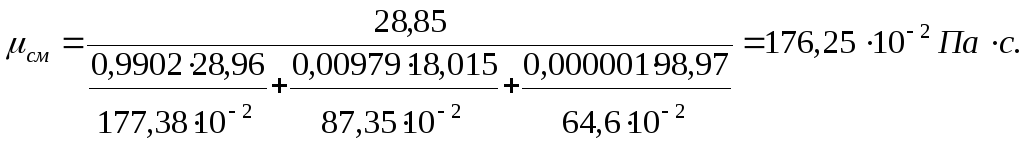
Кинематическая вязкость смеси газов наружной среды:
![]()
![]() .
.
Коэффициент диффузии компонентов наружной среды при t = 0 оC и Р = 101308 Па, м2/ч:
![]()
![]()
![]()
![]()
Коэффициент диффузии компонентов наружной среды при t = 16 оC и Р=В=101325 Па, м2/ч:
![]()
![]()
![]()
![]()
Пример 1.2. Определить параметры внутренней среды в трубопроводе, транспортирующем газовую смесь.
Исходные данные. Давление наружной среды В = 101325 Па; состав смеси, % масс.: водород 58,9, αН2 = 0,589; оксид углерода 7,1, αСО = 0,071; метан 34, αСН4 = 0,34. Температура газовой смеси t = 50 оС. Избыточное давление в трубопроводе Ризб = 101325 Па.
Решение. Молекулярные массы составляющих газовой смеси: МН2 = 2; МСО = 28; МСН4 = 16.
Объемные доли составляющих газовой смеси:
![]()

Абсолютное давление газовой смеси в трубопроводе:
![]()
Парциальное давление составляющих газовой смеси, Па:

Концентрации составляющих газовой смеси, мг/м3:

Произведение Ni∙ρi для составляющих газовой смеси, мг/м3 (кг/м3):

Плотность газовой смеси в трубопроводе:
![]()
![]()
Динамическая вязкость составляющих газовой смеси при t = 0 oC и Рo = 101308 Па, Па·с:
![]()
Константы Сатерленда:
![]()
Динамическая вязкость составляющих газовой смеси при t = 50 oC, Па∙с:
![]()
![]()
![]()
![]()
Молекулярная масса смеси газов в трубопроводе:
![]()
![]()
Динамическая вязкость смеси газов в трубопроводе:
![]()
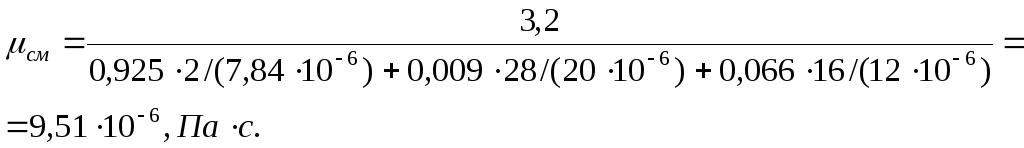
Кинематическая вязкость смеси газов в трубопроводе:
![]()
![]()
Коэффициенты диффузии составляющих газовой смеси при t = 0 oC и Рo = 101308 Па, м2/ч:
![]()
![]()
![]()
Коэффициенты диффузии составляющих газовой смеси при t = 50 oC и Р = 202650 Па, м2/ч:
![]()
![]()
![]()
![]()
Пример 1.3. Определить параметры среды над открытой поверхностью жидкости в наружной среде.
Исходные данные. Давление наружной среды В = 101325 Па. Состав жидкости, % масс.: вода 40, Н2О = 0,4; бензол 30, Б = 0,3; дихлорэтан 30, Д = 0,3. Температура жидкости t = 40 oC. Наружная среда – воздух. Влажность воздуха = 60 %. Температура воздуха t = 16 оС.
Молекулярные массы составляющих среды: МН2О = 18,02; МБ = 78,1;МД = 98,97; МВ = 28,96.
Решение
Мольные доли составляющих компонентов жидкости:
![]()
![]()
![]()
![]()
Из Приложения находим эмпирические коэффициенты А, В, С для каждого компонента смеси:
|
Вода |
А = 7,9608; |
В = 1678,0; |
С = 230,0; |
|
Бензол |
А = 6,9120; |
В = 1214,6; |
С = 221,2; |
|
Дихлорэтан |
А = 7,1840; |
В = 1358,5; |
С = 232,0. |
Давление насыщенного пара чистого вещества при заданной температуре:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Парциальное давление паров компонента над смесью жидкостей:
![]()
![]()
![]()
![]()
Парциальное давление основного газового компонента – воздуха:
![]()
Объемные (мольные) доли газовых составляющих над жидкостью:
![]()
![]()
![]()
![]()
![]()
Концентрации составляющих газовой смеси над жидкостью:
![]()
![]()
![]()
![]()
Произведение
![]() для составляющих газовой смеси над
жидкостью, мг/м3
(кг/м3):
для составляющих газовой смеси над
жидкостью, мг/м3
(кг/м3):
![]()
![]()
Плотность газовой смеси над жидкостью (с учетом температуры жидкости):
![]()
![]()
Динамическая
вязкость составляющих газовой смеси
над жидкостью при
![]() (Приложение),
Па∙с:
(Приложение),
Па∙с:
![]()
![]()
Константы Сатерленда (Приложение):
![]()
Динамическая
вязкость составляющих газовой смеси
над жидкостью при
![]() ,
Па·с:
,
Па·с:
![]()
![]()
![]()
![]()
![]()
Молекулярная масса смеси газов над жидкостью:
![]()
![]()
Динамическая вязкость смеси газов над жидкостью, Па·с:


Кинематическая вязкость смеси газов над жидкостью, м2/с:
![]()
![]()
Коэффициенты диффузии компонентов газовой смеси над жидкостью при t = 0 oC и Рo = 101 308 Па, м2/ч:
![]()
![]()
![]()
Коэффициенты диффузии компонентов газовой смеси над жидкостью при t = 40 oC и Р = 101 325 Па, м2/ч:
![]()
![]()
![]()
![]()
![]()
