
му по химии / Дергачева химия полимеров
.PDF
7. Биополимеры
Биополимеры – это класс полимеров, встречающихся в природе и входящие в состав живых организмов: белки, нуклеиновые кислоты, полисахариды.
Белки, или протеины (от греч. «протос» – «первый»), – это природные органические соединения, которые обеспечивают все жизненные процессы любого организма.
Биополимеры состоят из одинаковых (или разных) звеньев – мономеров. Мономеры белков – это аминокислоты, нуклеиновых кислот –
нуклеотиды, в полисахаридах – моносахариды.
Выделяют два типа биополимеров – регулярные (некоторые полисахариды) и нерегулярные (белки, нуклеиновые кислоты, некоторые полисахариды).
Уровни организации белков
первичная структура; вторичная структура; третичная структура; четвертичная структура.
Первичная структура определяется последовательностью мономеров, вторичная задаѐтся внутри- и межмолекулярными взаимодействиями между мономерами, обычно при помощи водородных связей.
Третичная структура зависит от взаимодействия вторичных структур, четвертичная, как правило, образуется при объединении нескольких молекул с третичной структурой.
Вторичная структура белков образуется при взаимодействии аминокислот с помощью водородных связей и гидрофобных взаимодействий. Основными типами вторичной структуры являются α- спираль, когда водородные связи возникают между аминокислотами в одной цепи, β-листы (складчатые слои), когда водородные связи образуются между разными полипептидными цепями, идущими в разных направлениях (антипараллельно, неупорядоченные участки.
Третичная структура или «фолд» образуется при взаимодействии вторичных структур и стабилизуется не ковалентными, ионными, водородными связями и гидрофобными взаимодействиями. Белки, выполняющие сходные функции обычно имеют сходную третичную структуру.
Примером фолда является β-баррел (бочка), когда β-листы располагаются по окружности. Третичная структура белков определяется с помощью рентгеноструктурного анализа.
50
Молекула белка может состоять не из одной, а из нескольких полипептидных цепей. Каждая такая цепь представляет собой самостоятельную пространственную структуру – субъединицу. Например, белок гемоглобин состоит из четырѐх субъединиц, которые образуют единую молекулу, располагаясь в вершинах почти правильного тетраэдра. Субъединицы «прилипают» друг к другу благодаря тем же самым силам, что стабилизируют третичную структуру. Это гидрофобные взаимодействия, солевые мостики и водородные связи.
Если белок состоит из нескольких субъединиц, говорят, что он обладает четвертичной структурой. Такая структура представляет собой высший уровень организации белковой молекулы. В отличие от первых трѐх уровней четвертичная структура есть далеко не у всех белков. Приблизительно половина из известных на сегодняшний день белков еѐ не имеют.
Важный класс полимерных белков составляют фибриллярные белки, самый известный из которых коллаген.
Коллаген – это фибриллярный белок, составляющий основу соединительной ткани организма (сухожилие, кость, хрящ, дерма и т. п.) и обеспечивающий ее прочность и эластичность. Коллаген присутствует во всех организмах – от вирусов до многоклеточных.
Коллагеновые структуры не обнаружены только у растений. Молекула коллагена представляет собой правозакрученную спираль из трѐх α-цепей.
Связи, поддерживающие пространственную структуру белка, довольно легко разрушаются. Происходит это из-за разрушения пространственной структуры белков альбумина в яичном белке и казеина (от лат. caseus – «сыр») в молоке. Такой процесс называется денатурацией. В первом случае еѐ вызывает нагревание, а во втором – значительное увеличение кислотности (в результате жизнедеятельности обитающих в молоке бактерий). При денатурации белок теряет способность выполнять присущие ему в организме функции (отсюда и название процесса: от лат. denaturare – «лишать природных свойств»). Денатурированные белки легче усваиваются организмом, поэтому одной из целей термической обработки пищевых продуктов является денатурация белков. Денатурация может быть и обратимой. После устранения денатурирующего фактора многие белки способны вернуть естественную форму, т.е. ренатурировать.
Основа всех белков – это аминокислоты
Белковые полимеры построены из 20 α-аминокислот. Остатки аминокислот связаны в макромолекулы белка пептидными связями, возникающими в результате реакции карбоксильных и аминогрупп.
51

Аминокислоты (аминокарбоновые кислоты) – это органические соединения, в молекуле которых одновременно содержатся карбоксильные и аминные группы.
Основные 20 аминокислот: аланин, аргинин, аспарагин, валин, гистидин, глицин, глутамат, глутамин, изолейцин, лейцин, лизин, метионин, пролин, серин, тирозин, треонин, триптофан, фенилаланин, цистеин.
Общим признаком аминокислот, входящих в состав белка (исключение составляет пролин), является наличие свободной карбоксильной группы и свободной незамещенной аминогруппы у альфа-углеродного атома. Незаменимые аминокислоты: валин, изолейцин, лейцин, лизин, метионин, треонин, триптофан, фенилаланин, тирозин, цистеин. Потребность в них составляет 250-1100 мг/сут. Заменимые аминокислоты: аланин, аспарагин, аспартат, гидроксилизин, гидроксипролин, глицин, глутамат, глутамин, пролин, серин. Полунезаменимые: аргинин, гистидин.
Аминокислоты находят широкое применение в качестве пищевых добавок. Например, лизином, триптофаном, треонином и метионином обогащают корма сельскохозяйственных животных, добавление натриевой соли глутаминовой кислоты (глутамата натрия) придает ряду продуктов мясной вкус. В смеси или отдельно аминокислоты применяют в медицине, в том числе при нарушениях обмена веществ и заболеваниях органов пищеварения, при некоторых заболеваниях центральной нервной системы (g-аминомасляная и глутаминовая кислоты).
Аминокислоты используются при изготовлении лекарственных препаратов, красителей, в парфюмерной промышленности, в производстве моющих средств, синтетических волокон и пленки.
Значение белков в живой природе трудно переоценить. Это строительный материал живых организмов, биокатализаторы – ферменты, обеспечивающие протекание реакций в клетках, и энзимы, стимулирующие определѐнные биохимические реакции, т.е. обеспечивающие избирательность биокатализа. Кроме того, белки служат питательными веществами.
52
В семенах многих растений (пшеницы, кукурузы, риса и др.) содержатся пищевые белки. К ним относятся также альбумин – основной компонент яичного белка и казеин – главный белок молока. При переваривании в организме человека белковой пищи происходит гидролиз пептидных связей. Белки «разбираются» на отдельные аминокислоты, из которых организм в дальнейшем «строит» новые пептиды или использует для получения энергии. Отсюда и название: греческое слово «пептос» означает «переваренный». Интересно, что гидролизом пептидной связи управляют тоже белки – ферменты. Участвуют в регуляции клеточной и физиологической активности. К подобным белкам относятся многие гормоны (от греч. «гормао» – «побуждаю»), такие, как инсулин, регулирующий обмен глюкозы, и гормон роста. Белки наделяют организм способностью изменять форму и передвигаться. За это отвечают белки актин и миозин, из которых построены мышцы. Белки выполняют опорную и защитную функции, скрепляя биологические структуры и придавая им прочность. Кожа представляет собой почти чистый белок коллаген, а волосы, ногти и перья состоят из прочного нерастворимого белка кератина. Наши мышцы, волосы, кожа состоят из волокнистых белков.
Белок крови, входящий в состав гемоглобина, способствует усвоению кислорода воздуха, другой белок – инсулин – ответственен за расщепление сахара в организме и, следовательно, за его обеспечение энергией.
7.1. Полисахариды: крахмал, целлюлоза, инулин
Полисахариды являются высокомолекулярными соединениями, содержащими сотни и тысячи остатков моносахаридов. Наиболее известные полисахариды: гликоген, крахмал, целлюлоза, хитин, амилоза, амилопектин, стахилоза, инулин, декстрин, пектин, галактоманнаны.
Общим для строения полисахаридов является то, что остатки моносахаридов связываются за счет полуацетального гидроксила одной молекулы и спиртового гидроксила другой и т.д. Каждый остаток моносахарида связан с соседними остатками гликозидными связями. Полигликозиды могут содержать разветвленные и неразветвленные цепи.
Остатки моносахаридов, входящие в состав молекулы, могут быть одинаковыми или разными.
Наибольшее значение из высших полисахаридов имеют крахмал,
гликоген (животный крахмал), клетчатка (или целлюлоза). Все эти три полисахарида состоят из молекул глюкозы, по-разному соединенных друг с другом. Состав всех трех соединений можно выразить общей формулой:
(С6Н10О5)n.
53

Моносахариды как составные части полисахаридов Моносахариды – это дифункциональные соединения, так как в составе
каждой молекулы содержатся несколько гидроксильных групп и одна карбонильная.
В зависимости от природы карбонильной группы (альдегидная или кетонная) моносахариды делятся на альдозы и кетозы.
Так, моносахарид гексоза существует в виде двух структурных изомеров – альдогексозы (I) (глюкоза) и кетогексозы (II) (фруктоза):
Моносахариды, как и другие соединения с асимметрическими атомами углерода, существуют в виде двух оптических изомеров – D- и L-форм.
Отнесение к D- и L-формам производят по расположению гидроксильной группы у атома углерода, соседнего с первичной спиртовой группировкой:
Все моносахариды существуют в виде двух таутомерных форм: открытой, или ациклической, и закрытой, или циклической. Циклическая форма образуется в результате внутримолекулярного взаимодействия альдегидной (кетонной) группировки с одним из гидроксидов.
Наибольшей устойчивостью обладают шести- и пятичленные циклы, называемые соответственно пиранозными и фуранозными циклами.
Схема образования пиранозного цикла:
54

Атом водорода гидроксильной группы присоединяется к атому кислорода альдегидной группировки. При этом образуется так называемый полуацетальный или гликозидный гидроксил. После переноса атома водорода от гидроксильной группы на альдегидную атом кислорода соединяется с атомом углерода с образованием цикла. В результате циклизации в молекуле моносахарида появляется дополнительный асимметрический атом углерода.
Образующиеся циклические формы отличаются друг от друга расположением полуацетального гидроксила, располагающийся над или под плоскостью кольца.
Отдельные моносахариды
Глюкоза – бесцветное кристаллическое вещество, сладкое на вкус, хорошо растворимое в воде. В организме человека и животных глюкоза подвергается ферментативному окислению, конечными продуктами которого являются оксид углерода (IV) и вода.
Фруктоза – структурный изомер глюкозы. Кристаллическое вещество, хорошо растворимое в воде, более сладкое, чем глюкоза. В свободном виде содержится в мѐде и фруктах. Химические свойства фруктозы обусловлены наличием кетонной и пяти гидроксильных групп.
Дезоксирибоза – бесцветное кристаллическое вещество, хорошо растворимое в воде. В виде фуранозной формы входит в состав ДНК. Как и другие моносахариды, дезоксирибоза в растворе существует в ациклической и циклической формах, способна образовывать простые и сложные эфиры, принимает участие в ОВР и реакциях комплексообразования.
Рибоза – бесцветное кристаллическое вещество, хорошо растворимое в воде. В виде фуранозной формы входит в состав РНК. Химические свойства рибозы обусловлены наличием альдегидной и гидроксильных групп.
55
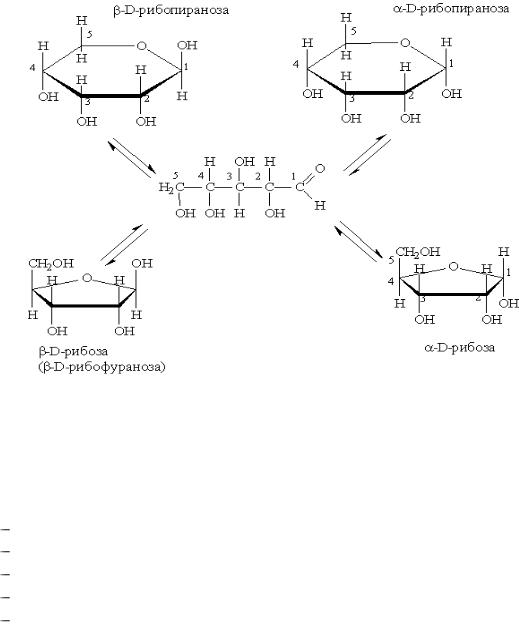
Олигосахариды
Наиболее изученными олигосахаридами являются дисахариды, которые широко распространены в природе. Они содержатся во многих плодах и овощах, сахарной свекле, сахарном тростнике, меде. Наиболее известные дисахариды:
сахароза
лактоза
мальтоза
целлобиоза ксилобиоза.
Дисахариды получают из природных источников: сахарозу из сахарной свеклы или сахарного тростника, мальтозу – ферментативным гидролизом крахмала, лактозу – из коровьего молока, целлобиозу – гидролизом целлюлозы.
Различают два вида дисахаридов.
1. Простые эфиры (гликозиды), образующиеся за счет взаимодействия полуацетального гидроксила одной из молекул моносахарида и одного из спиртовых гидроксилов (чаще всего у четвертого атома углерода) другой молекулы:
56
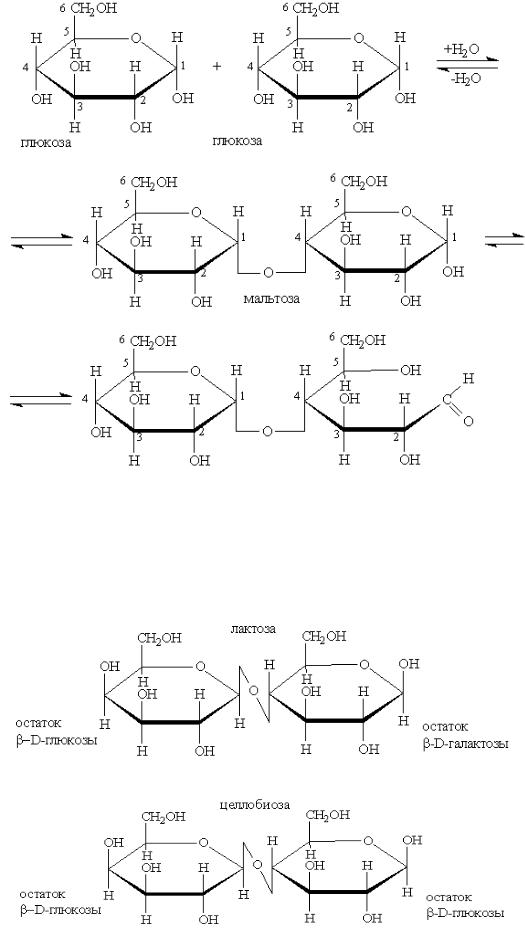
Молекула образующегося при этом дисахарида содержит один полуацетальный гидроксил и способна переходить в ациклическую альдегидную форму. Подобные дисахариды способны восстанавливать такие вещества, как Ag2O, Cu(OH)2, за что их называют восстанавливающими сахарами. К восстанавливающим сахарам относятся также целлобиоза и лактоза:
57

2. Простые эфиры образуются за счет взаимодействия двух полуацетальных гидроксилов:
Крахмал
Крахмал относится к полисахаридам. Молекулярная масса этого вещества точно не установлена, но известно, что очень велика (порядка 100000) и для разных образцов может быть различна. Поэтому формулу крахмала, как и других полисахаридов, изображают в виде (С6Н10О5)n. Для каждого полисахарида n имеет различные значения.
Крахмал представляет собой безвкусный порошок, нерастворимый в холодной воде. В горячей воде набухает, образуя клейстер.
Крахмал широко распространен в природе. Он является для различных растений запасным питательным материалом и содержится в них в виде крахмальных зерен. Наиболее богато крахмалом зерно злаков: риса (до 86%), пшеницы (до 75%), кукурузы (до 72%), а также клубни картофеля (до 24%). В клубнях картофеля крахмальные зерна плавают в клеточном соке, а в злаках они плотно склеены белковым веществом клейковиной. Крахмал является одним из продуктов фотосинтеза.
Из растений извлекают крахмал, разрушая клетки и отмывая его водой. В промышленном масштабе его получают главным образом из клубней картофеля (в виде картофельной муки), а также из кукурузы.
Крахмал состоит из двух фракций: амилозы (15–25%) амилопектина (75–85%).
Амилоза представляет собой линейный биополимер, состоящий из остатков глюкозы, соединенных через кислородные атомы в положении 1 и Молекулярная масса амилозы от 150 000 до 500 000 а. е. м. в зависимости от вида растения.
58

Амилопектин – это биополимер, состоящий из остатков глюкозы, соединенных через кислородные атомы в положении 1–4 и 1–6. Молекулярная масса амилопектина составляет порядка миллиона.
Химические свойства крахмала
При действии ферментов или при нагревании с кислотами (ионы водорода служат катализатором) крахмал, как и все сложные углеводы, подвергается гидролизу.
При этом сначала образуется растворимый крахмал, затем менее сложные вещества – декстрины.
Конечным продуктом гидролиза является глюкоза. Можно выразить суммарное уравнение реакции следующим образом:
(С6 Н10О5 )п |
пН2О |
Н2SO4 |
,t |
nC6 H12O6 |
|
|
|
|
|||
(C6 H10O5 )n |
(C6 H10O5 )m |
|
xC12H22O11 |
nC6 H12O6 |
|
Крахмал |
декстрины |
|
мальтоза |
глюкоза |
|
Происходит постепенное расщепление макромолекул.
Крахмал не дает реакции «серебряного зеркала», но ее дают продукты его гидролиза. Макромолекулы крахмала состоят из многих молекул циклической -глюкозы.
Процесс образования крахмала можно выразить так (реакция поликонденсации):
Характерной реакцией является взаимодействие крахмала с растворами йода. Если к охлажденному крахмальному клейстеру добавить раствор йода, то появляется синее окрашивание. При нагревании клейстера оно исчезает, а при охлаждении появляется вновь.
59
