
Болятко Основы екологии и охраны окружаюсчей 2008
.pdf
интересующей области, что означает отсутствие радиоактивного распада, химических реакций или бактериального разложения.
Рис. 2.1. Диаграмма баланса вещества в исследуемой области
Для такого консервативного случая слагаемое «скорость распада» также обращается в нуль. Примером консервативных веществ служат растворенные в воде твердые вещества или углекислый газ в воздухе.
Простейшими для анализа будут системы, находящиеся в стационарном состоянии, а интересующее нас вещество является консервативным. В таких случаях уравнение (2.1) переходит в следующее:
скорость |
скорость |
(2.2) |
|
проникновен |
вывода |
||
|
Рассмотрим отдельные члены уравнения (2.1). Пусть проникающим компонентом будет поток воды или воздуха
мощностью QS (объем/время) с концентрацией загрязнителя CS
(масса/объем). Тогда член «скорость проникновения» будет иметь |
|
вид |
(QS CS +S), где S – мощность источника загрязнения |
(скорость образования) внутри исследуемой области. Если имеется несколько источников проникновения, то вместо члена QS CS
51

n |
|
|
|
|
следует рассматривать |
Qi |
C i |
(n – |
число источников). Тогда, |
|
S |
S |
|
|
i 1 |
|
|
|
|
например, для (2.2) можно записать: |
|
|||
n |
|
|
|
|
QSi |
CSi |
|
Q C , |
(2.3) |
i 1 |
|
|
|
|
полагая при этом полное перемешивание загрязнений в рассматриваемом объеме V .
Во многих случаях вещества являются неконсервативными. Распад неконсервативных веществ обычно рассматривается как реакция первого порядка, т.е. полагается, что скорость убывания
концентрации описывается уравнением: |
|
|
dC dt |
K C , |
(2.4) |
где K – коэффициент скорости реакции. |
|
|
Решение этого уравнения имеет вид: |
|
|
C C(0) e K t , |
(2.5) |
|
где С(0) – начальная концентрация при t 0 . |
|
|
Поскольку полная |
масса неконсервативного |
загрязнителя |
равномерно распределенного в объеме, равняется C V , то можно написать выражение для «скорости распада»:
d (C V ) |
V |
dC |
K C V . |
(2.6) |
|
dt |
dt |
||||
|
|
|
В нестационарном случае член «скорость накопления» в уравнении (2.1) отличен от нуля, и для равномерно распределенного
по объему загрязнителя массой C V уравнение примет вид:
V |
dC |
QS Cs |
S Q C K C V . |
(2.7) |
|
dt |
|||||
|
|
|
|
||
Решение для стационарного случая (равновесного состояния) |
|||||
легко найти, положив dC dt |
0 : |
|
|||
C( ) |
Qs |
Cs S |
|
(2.8) |
|
Q |
K V . |
||||
|
|||||
|
52 |
|
|
||

Уравнение (2.7) можно решить с помощью перехода к новой переменной:
|
Qs Cs +S |
|
=[C −C(∞)], |
|
|
C' = C − |
|
(2.9) |
|||
|
|||||
|
Q +K V |
|
|
|
|
|
|
|
|
где C(∞) есть концентрация загрязнителя для равновесного состояния. Тогда решение уравнения (2.7) будет иметь вид:
|
|
Q |
|
|
|
C(t) =[C(0) −C(∞)] exp − K + |
|
t |
+C(∞) , |
(2.10) |
|
|
|||||
|
|
V |
|
|
|
где C(0) – начальная концентрация.
Изложенный подход рассматривает однокамерную модель, включающую всю исследуемую область. Такую простую модель, схематически показанную на рис. 2.1, можно применить, например, для оценки качества воздуха в помещении. Однокамерная модель помещения приведена на рис. 2.2.
Рис. 2.2. Однокамерная модель для расчета загрязнения воздуха в помещении
Пусть проникновение воздуха в помещение и его вывод
характеризуются величиной I V , где I – скорость воздухообмена. Тогда уравнение (2.7) примет следующий вид:
V |
dC |
= S +CS I V −C I V − K C V , |
(2.11) |
|
dt |
||||
|
|
|
53

где CS и C – концентрации загрязнителя вне и внутри помещения
соответственно. Решение этого уравнения для стационарного состояния имеет вид:
C( ) |
S V |
CS |
I |
. |
(2.12) |
I |
K |
|
|||
|
|
|
|
Решение для нестационарного случая имеет вид (2.10), где Q I V . Такие загрязнители воздуха, как CO и NO, могут считаться консервативными ( K 0 ). Тогда, если начальная концентрация в помещении C(0) 0 , и можно пренебречь
концентрацией загрязнителя |
|
вне |
помещения |
CS 0 , то |
||
нестационарное решение примет вид: |
|
|
||||
C(t) |
S |
[1 |
exp( |
I t)] . |
(2.13) |
|
I V |
||||||
|
|
|
|
|
||
Оно может быть использовано, в частности, для определения концентрации CO в помещении при использовании различных нагревателей.
2.2. Общие закономерности биогеохимических круговоротов
Основой динамического равновесия и устойчивости биосферы являются круговороты веществ и превращение энергии. Живое вещество, используя солнечную энергию, организует процессы преобразования окружающей среды на основе динамических замкнутых круговоротов веществ. Большая часть поступающей от Солнца энергии рассеивается и теряется безвозвратно, за исключением той небольшой части, которая ассимилируется растениями и производит биомассу, небольшая часть энергии запасается в виде карбонатных отложений и мертвого органического вещества.
Потоки вещества, в свою очередь, являются замкнутыми и образовывают круговорот (или цикл). Речь идет о циклическом движении химических элементов и соединений, которое протекает внутри разных экосистем, при этом химические элементы попадают из окружающей среды в организм и обратно.
54

Подвижность химических элементов зависит от формы их нахождения в природе и от той роли, которую они выполняют в живых организмах. Так, миграционная способность продуктов выветривания и почвообразования определяется степенью дисперсности материала и его растворимостью. Растительные и животные организмы удерживают в своих тканях миллиарды тонн минеральных веществ. Чем больше биогенное значение химического элемента, тем в большей степени он захватывается живыми организмами и, следовательно, оказывается защищенным от выноса из почв грунтовыми и речными водами.
Рис.2.3. Схема геологического круговорота вещества континентальной земной коры
Рассмотрим самый масштабный из круговоротов – геологический, который имел место и на безжизненной планете, но с возникновением биосферы направляется совместным действием геохимических и биологических факторов (рис. 2.3). Заметим, что
55
интенсивность геологического круговорота невелика (постоянная времени составляет миллионы лет).
Океан и почвы представляют собой геохимически сопряженные планетарные суперландшафты. В настоящее время суша в целом является элювиальной системой, океан – аккумулятивной системой. Земная кора, кора выветривания почвы отдают в океан растворы, механические осадки, органическое вещество. В этом процессе участвуют наземные, подпочвенные и подземные воды. За счет этого океан получает ежегодно огромное количество механических осадков. Часть этих компонентов океан различными путями возвращает на сушу (инфильтрация, приливы, цунами и др.).
Таким образом, круговорот веществ в системе «суша – океан – верхняя мантия» обогащает океан химическими элементами. В табл. 2.1 приведен химический состав почв и океанических вод по степени их содержания.
Таблица 2.1
Сравнение химического состава почв и океанических вод, %
Почва |
|
Океан |
||
O |
|
49 |
O |
85,6 |
Si |
|
33 |
H |
10,7 |
Al |
|
7,3 |
Cl |
1,89 |
Fe |
|
3,8 |
Na |
1,0 |
C |
|
2,0 |
Mg |
0,14 |
Ca |
|
1,37 |
S |
8,8∙10-2 |
K |
|
1,36 |
Ca |
4∙10-2 |
H |
|
1,0 |
K |
3,8∙10-2 |
Na, Mg |
|
0,6 |
N |
6,7∙10-5 |
N |
|
0,1 |
Si |
5∙10-5 |
Mn, S |
|
0,09 |
Fe, P |
5∙10-6 |
P |
|
0,08 |
C |
2∙10-6 |
Cl |
|
0,01 |
Al |
1∙10-6 |
56

Видно, что химическую основу океана составляют «аквафилы»: H, O, Cl, Na, Mg. В почве аккумулируются такие жизненно важные элементы, как Si, Al, Fe, C, P, K, N, Ca.
Суша и океан находятся в состоянии непрерывного циклического обмена и с нижними слоями атмосферы – тропосферой. Они поставляют в атмосферу аэрозольные частицы и получают их обратно с осадками и в виде сухих выпадений.
С поверхности суши, в основном, выносятся пылевидные и илистые частицы почвы горных пород, вулканического пепла. Среди аэрозольных частиц морского происхождения преобладают растворимые в воде соли.
Можно выделить три типа биогеохимических круговоротов: круговорот воды; круговорот газов (газообразные элементы);
круговорот элементов в твердой или осадочной фазе.
2.2.1. Круговорот воды
Важнейшим среди круговоротов является, безусловно, круговорот воды. Вода играет большую роль в нашей жизни, на использовании воды основано существование биосферы и человека.
Вода покрывает около 70% территории планеты и обладает физическими и химическими свойствами, которые резко отличают ее от других известных жидкостей. Например, она увеличивается в объеме при охлаждении, имеет максимальную плотность при 4 C. Значения температуры замерзания и кипения имеют большую разницу, что позволяет воде оставаться жидкой в большинстве областей Земли.
Среди существующих в природе жидкостей вода обладает наибольшей теплопроводностью, составляющей 4,18 кДж/(кг К). Это предопределяет ее большое влияние на климат. Основным терморегулятором климата являются воды океанов и морей: накапливая тепло летом, они отдают его зимой. Благодаря влиянию океанов на значительной части земного шара обеспечивается перевес осадков на суше над испарением, и растения и животные получают нужное для жизни количество воды.
57
Именно из-за уникальных свойств воды появилась и поддерживается жизнь на Земле, содержание воды в живых организмах достигает 80% (биомасса в среднем на 2/3 состоит из воды).
Если представить, что вода равномерно распределена по поверхности земного шара в виде сферического слоя, то для отдельных составляющих мировых запасов воды толщина этого слоя составит:
Мировой океан, м |
2700 |
Ледники, м |
100 |
Подземные воды, м |
15 |
Пресные воды,м |
0,4 |
Атмосферная влага, м |
0,03 |
Таким образом, 96% воды сосредоточено в океанах, а доступная для использования человеком пресная вода составляет лишь 0,6% от общих запасов. Это - пресные подземные воды, вода
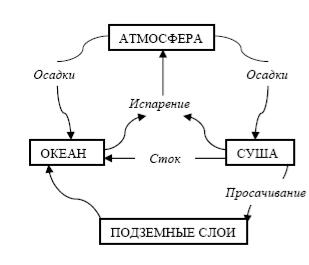
пресных озер и рек. Схема гидрологического цикла показана на рис. 2.4.
Рис. 2.4. Схема гидрологического цикла
В круговороте воды можно выделить три важнейших процесса: выпадение осадков и последующие испарение,
58
поверхностный сток воды в моря и озера, просачивание воды в подземные слои с образованием подземных вод.
Около половины достигающей земную поверхность солнечной энергии расходуется на испарение воды. Испарение с поверхности Земли дает за год такое количество воды, которое могло бы покрыть земной шар слоем толщиной один метр. При этом около 80% воды испаряется из океана с образованием облаков, но, в то же время на сушу выпадает больше осадков. Разница в выпадении осадков над сушей и океаном возвращается в океаны в виде стока рек и грунтовых вод. Половина осадков, выпадающих на сушу, попадают в атмосферу за счет испарения, а другая половина или стекает в океан (в виде ручьев и рек) или становится грунтовыми водами.
Сток является возобновляемым источником пресной воды, в настоящее время человеком используется более 10% от его объема. По континентам ресурсы речных вод распределены неравномерно: в Европе и Азии, где проживает 70% населения планеты, сосредоточено лишь 40% мировых запасов речных вод.
В пределах экосистемы происходит четыре процесса, включающиеся в общий круговорот воды.
 Перехват – процесс, при котором растения перехватывают часть выпадающей в осадках воды до того, как она достигнет почвы, и испаряют ее в атмосферу. Этот процесс максимален при слабом дожде и достигает в умеренных широтах 25% общей суммы осадков.
Перехват – процесс, при котором растения перехватывают часть выпадающей в осадках воды до того, как она достигнет почвы, и испаряют ее в атмосферу. Этот процесс максимален при слабом дожде и достигает в умеренных широтах 25% общей суммы осадков.
 Инфильтрация – процесс, при котором часть воды, просачиваемая в почву, используется растениями, другая часть по капиллярам поднимается на поверхность и затем испаряется.
Инфильтрация – процесс, при котором часть воды, просачиваемая в почву, используется растениями, другая часть по капиллярам поднимается на поверхность и затем испаряется.
 Транспирация – испарение воды растениями, биологическое испарение воды (не дождевой). Количество транспирированной воды велико: одна береза в день испаряет около 75 л воды. При этом на фотосинтез уходит доли процента от общего количества прокачиваемой воды.
Транспирация – испарение воды растениями, биологическое испарение воды (не дождевой). Количество транспирированной воды велико: одна береза в день испаряет около 75 л воды. При этом на фотосинтез уходит доли процента от общего количества прокачиваемой воды.
 Сток – потери воды, вызванные этим процессом, увеличиваются с крутизной склонов и при уменьшении плотности растительного покрова.
Сток – потери воды, вызванные этим процессом, увеличиваются с крутизной склонов и при уменьшении плотности растительного покрова.
59
Время обновления воды в различных компонентах гидросферы очень различно: для океана время полного оборота воды составляет две с половиной тысячи лет, в реках и озерах – 1 год, в атмосфере – около 80 сут. В процессе круговорота значительное количество воды попадает в живые растения, и в результате фотосинтеза за два миллиона лет происходит полное расщепление воды.
2.3.Биогеохимические циклы важнейших
химических элементов
Наибольший интерес представляют циклы биологически значимых элементов. В биомассе господствуют лишь четыре элемента – углерод, кислород, водород и азот. Причем наибольшая доля (около 80%) в составе живого вещества приходится на кислород и водород. Эти же элементы, как это видно из табл. 2.1, являются основными составляющими океанических вод и почвы. Заметная доля принадлежит фосфору и сере, являющимися важнейшими компонентами белка, хотя присутствуют в биомассе в меньших количествах (0,1 – 1,0%). Следующую группу элементов, содержание которых в организме колеблется в пределах 0,01 – 0,1%, составляют калий, натрий, магний и кальций. В микроконцентрациях всем организмам необходимы так называемые микроэлементы (медь, железо, алюминий, цинк, кремний, кобальт и др.). На сегодня установлена биологическая роль примерно двадцати двух элементов.
Одним из важных показателей биологической значимости является время круговорота химического элемента, которое определяется как отношение биомассы (живого и мертвого вещества) к годичной продукции.
2.3.1.Круговорот углерода
Круговорот углерода, показанный на рис. 2.5, является самым интенсивным из всех важных биогеохимических циклов.
Время круговорота углерода в биосфере составляет примерно
30 лет.
60
