
Карцев В.Г.Избранные методы с-за и модифик. гетероциклов т.2 , 2003
.pdf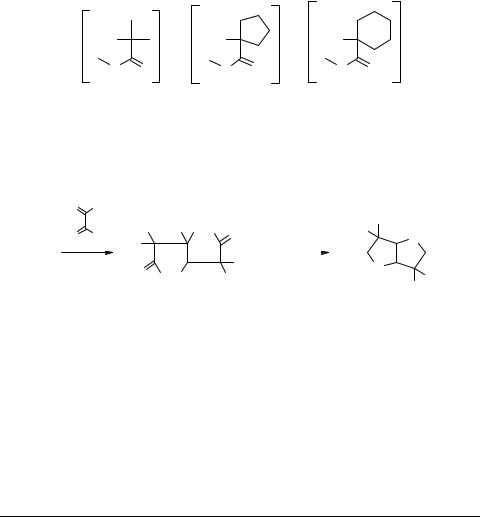
Синтез замещенных 3а-арилтетрагидро- фуро[3,2-b]фуран-2,5-дионов
Щепин В.В., Кириллов Н.Ф., Фотин Д.В.
Пермский государственный университет 614990, Пермь, ул. Букирева, 15
Нами изучено взаимодействие модельных реактивов Реформатского 1–3, полученных из метиловых эфиров 2-бром-2-метилпропановой кислоты, 1-бромциклопен- тан-, 1-бромциклогексанкарбоновых кислот и цинка, с арилглиоксалями [1].
BrZn |
BrZn |
BrZn |
O O |
O O |
O O |
1 |
2 |
3 |
Установлено, что реакция протекает по обеим карбонильным группам арилглиоксалей с образованием интермедиатов 4–6, которые самопроизвольно трансформируются в конечные продукты – замещенные 3а-арилтетрагидрофуро[3,2-b]- фуран-2,5-дионы 7–9.
O |
H |
|
R |
|
BrZn |
|
|
|
|
|
|
|
|
R Ar |
||||||
|
|
|
|
Ar |
|
|
|
|
|
|
|
|
|
|
||||||
O |
Ar |
O O |
O |
|
|
|
|
R |
||||||||||||
|
|
|
|
|
|
O |
||||||||||||||
R |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
1−3 |
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
O |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
R |
|
−2MeOZnBr |
|
|
|
|
|||||
|
|
O |
|
|
|
|
|
|
|
|
|
O |
||||||||
|
|
O O |
|
|
|
R |
|
|
|
|
|
|
R R |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
ZnBr |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
7−9 |
||||||||
|
|
|
|
|
4−6 |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
R = Me (4, 7); R+R = (CH2)4 (5, 8), (CH2)5 (6, 9)
1.Щепин В.В., Фотин Д.В., Недугов А.Н. и др., ЖОрХ 2002 38 (2) 278.
Генеральный спонсор и организатор – InterBioScreen Ltd. |
231 |
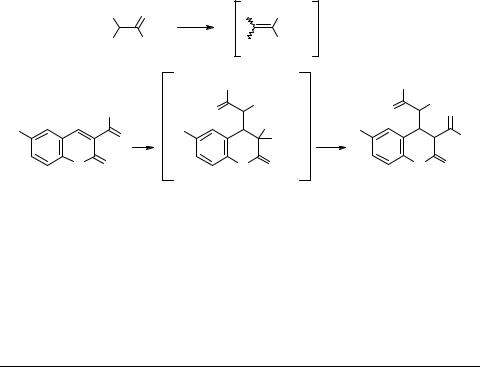
Реакции цинк-енолятов, образованных из 1-арил- 2-бромалканонов и цинка, с метиловым эфиром 6-бром-2-оксохромен-3-карбоновой кислоты и с 3-ацил-6-бромхромен-2-онами
Щепин В.В., Корзун А.Е., Русских Н.Ю.
Пермский государственный университет 614990, Пермь, ул. Букирева, 15
Производные хромен-2-она с карбонилсодержащей группой в положении 3 способны взаимодействовать с нуклеофильными реагентами тремя нуклеофильными центрами – атомами С(2) и С(4) гетероцикла и атомом углерода карбонилсодержащей группы [1].
Нами установлено, что цинк-еноляты 2, генерируемые из 1-арил-2-бромалка- нонов 1, региоспецифично атакуют атом С(4) метилового эфира 6-бром-2-оксо- хромен-3-карбоновой кислоты 3 или 3-ацетил(3-ароил)-6-бромхромен-2-онов 4(5), образуя через интермедиаты 6–8 метиловые эфиры 6-бром-4-(2-арил-2-оксо-1- R-этил)-2-оксохроман-3-карбоновой кислоты 9 или 3-ацетил(3-ароил)-6-бром-4-(2- арил-2-оксо-1-R-этил)хроман-2-оны 10(11).
|
R |
O |
Zn |
R |
OZnBr |
|
|
|
Br |
R' |
|
H |
R' |
|
|
|
1 |
|
|
|
2 |
|
|
|
|
|
|
R' |
|
|
R' |
|
R'' |
|
O |
R |
ZnBr |
O |
R O |
Br |
O |
2 |
Br |
|
Br |
R'' |
|
|
COR'' |
||||||
|
|
|
HCl |
||||
|
O O |
|
|
O |
O |
|
O O |
|
3−5 |
|
|
6−8 |
|
|
9−11 |
R" = OMe (3, 6, 9), Me (4, 7, 10), Ar (5, 8, 11);
R = Me, Et, i-Pr; R' = Ar
По данным спектров ПМР соединения 9–11 выделяются в виде одного диастереомера, находящегося в кетонной форме. В растворе соединений 10 в ДМСО-d6 наблюдается присутствие кетонной и енольной форм.
1.Cottan J., Livingstone R., Walshaw M., et al., J. Chem. Soc. 1965 (oct.) 5261.
232 |
Стендовые доклады |

Новый метод синтеза 6-гетарил-5,5-диалкил- 3,3-диметил-2,3,5,6-тетрагидропиран-2,4-дионов на основе реакции Реформатского
Щепин В.В., Корзун А.Е., Сажнева Ю.Х.
Пермский государственный университет 614990, Пермь, ул. Букирева, 15
Соединения, имеющие в своем составе тетрагидропиран-2,4-дионовый цикл, проявляют биологическую активность и входят в состав природных продуктов [1]. На основе реакции Реформатского нами разработан новый способ синтеза замещенных тетрагидропиран-2,4-дионов, содержащих в положении 6 цикла гетарильный радикал.
R |
O |
|
R |
|
O |
R |
O |
|
Zn, HetCHO |
|
|
|
|||
R |
|
R |
|
|
R |
|
|
Br |
O O |
|
Het |
|
O O |
−EtOZnBr Het |
O O |
|
|
BrZn |
O |
H |
|||
|
Et |
|
|
Et |
|
|
|
R = Me, Et |
|
|
|
|
|
|
|
В результате были получены новые типы дигетероциклических систем, в которых тетрагидропиран-2,4-дионовый цикл связан с гетероциклом фурана, тиофена, пиррола, индола, пиридина.
|
O |
|
|
O |
|
O |
|
O |
O |
|
O O |
|
O O |
O |
1 |
|
S |
2 |
N |
3 |
|
|
|
|
|||
|
O |
|
|
O |
|
OH |
|
O |
O |
|
O O |
|
O O |
N |
|
N |
N |
|
NO2 |
O |
O |
|
|
||
|
4 |
|
5 |
1.Kende A.S., Koch K., Dorey G., et al., J. Am. Chem. Soc. 1993 115 (21) 9842.
Генеральный спонсор и организатор – InterBioScreen Ltd. |
233 |
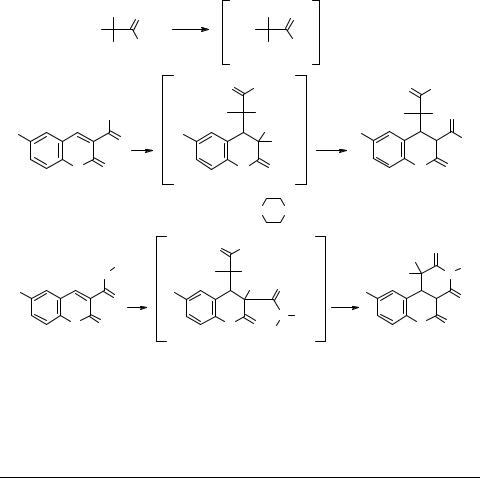
Реакции реактивов Реформатского, образованных из алкиловых эфиров 2-бромалкановых кислот и цинка с производными 2-оксохроменкарбоновой кислоты
Щепин В.В., Фотин Д.В.
Пермский Государственный Университет, 614990, Пермь, ул. Букирева, 15
Изучение реакции реагентов, образованных из алкиловых эфиров 2-бромуксусной, 2-бромпропионовой, 2-бромизомаслянной кислот и цинка, с метиловым эфиром 3 и амидами 6-бром-2-оксохромен-3-карбоновой кислоты 4, 5 показало, что на первой стадии реактив Реформатского 2 присоединяется к С(4) углеродному атому гетероцикла, давая интермедиаты 6–8. Гидролиз интермедиатов 6, 7 дает алкиловые эфиры 9 и морфолиды 10 6-бром-4-(2-алкокси-2-оксо-1-R-1-R'-3-этил)-2-оксохро- ман-3-карбоновой кислоты.
|
R' |
O |
Zn |
|
R |
O |
|
|
|
R |
|
BrZn |
|
OMe |
|
|
|
|
Br |
OMe |
|
R' |
|
|
||
|
1 |
|
|
|
2 |
|
|
|
|
|
|
O |
OMe |
|
O |
OMe |
|
|
R'' |
|
R' |
R |
|
R' |
R O |
|
|
|
|
|
|
ZnBr |
|
|
|
Br |
O |
2 |
Br |
|
COR'' HCl Br |
|
R'' |
|
O |
O |
|
|
O |
O |
|
O |
O |
3, 4 |
|
|
6, 7 |
|
|
9, 10 |
||
|
|
|
R" = OMe (3, 6, 9), O |
N (4, 7, 10) |
|
|
||
|
|
|
O |
OMe |
|
R' |
O |
|
|
HN Ar |
|
R' |
R |
|
|
N Ar |
|
|
|
|
|
R |
||||
Br |
O |
2 |
Br |
ZnBr O |
HCl Br |
|
O |
|
|
|
|
||||||
O |
O |
|
O |
|
N |
ZnBr |
O |
O |
|
OAr |
|
||||||
5 |
|
|
8 |
|
|
|
11 |
|
Иначе ведут себя интермедиаты 8, в которых кислый атом водорода в связи N–H присоединяет частицу ZnBr. В результате присоединения неорганической частицы возрастает основность атома азота и происходит самопроизвольная циклизация [1], которая дает 3-арил-9-бром-1-R-1-R'-4a,10b-дигидро-1H-хромен[3,4-c]- пиридин-2,4,5-трионы 11.
1.Щепин В.В., Фотин Д.В., Недугов А.Н. и др., ЖОХ 2002 38 (2) 278.
234 |
Стендовые доклады |
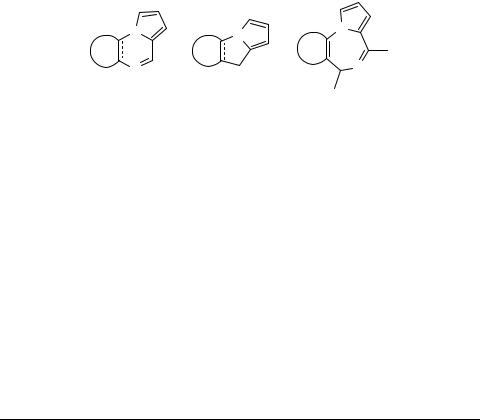
Polyfused heterocycles via the Clauson–Kaas reaction
El-Kashef H.S.
Chemisry Department, Faculty of Science,
Assiut University, Assiut, 71516 Egypt
Pyrrolo[1,2-a][1,4]benzodiazepines (PBDs) are a family of antitumor antibiotics derived from various Streptomyces species. This well-known family include anthramycin, totamycin, and neothramycins A, B. Their antitumor activity is based on their ability to form covalent adducts in the minor groove of DNA [1].
As part of our ongoing synthetic program directed toward the synthesis of new classes of triand tetracyclic heterocycles of possible antineoplastic activity, this communication concerns the synthesis of three different classes of polyfused heterocycles. These are the sulfur containing heterocycles fused to the pyrrolopyrazine (1), pyrrolopyrrolozine 2 or pyrrolodiazepine 3 moieties. The Clauson–Kaas reaction has been utilized as an excellent method for preparing the intermediates needed in these syntheses.
|
N |
N |
N |
S |
S |
|
S |
|
N |
|
N |
1 |
2 |
|
3 |
1.Thurston D.E., Bose S., Chem. Rev. 1994 (2) 433.
2.Geies A.A., Bakhite E.A., El-Kashef H.S., Pharmazie 1998 53 686.
3.El-Emary T.I., Kamal El-Dean A.M., El-Kashef H.S., Farmaco 1998 53 383.
4.Radwan Sh.M., El-Kashef H.S., Farmaco 1998 53 113.
5.El-Kashef H.S., El-Emary T.I., Gasquet M., et al., Pharmazie 2000 55 572.
6.Bakhite E.A., Geies A.A., El-Kashef H.S., Phosphorous, Sulfur Silicon Relat Elem.
2002 177 303.
Генеральный спонсор и организатор – InterBioScreen Ltd. |
235 |
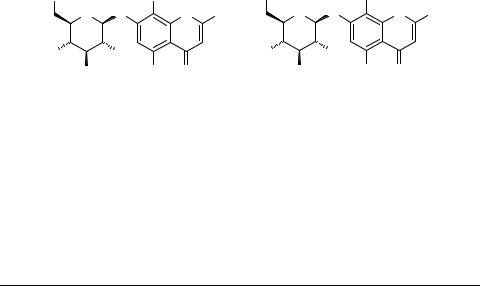
Флавоноиды Scutellaria immaculata и Scutellaria ocellata
Юлдашев М.П.1, Каримов А.2
1Институт химии растительных веществ им. акад. С.Ю. Юнусова, АН РУз 700170, Ташкент, пр. Х. Абдуллаева, 77 2Наманганский Государственный Университет 716000, Наманган, ул. Уйчи, 316
Продолжая исследование растений рода Scutellaria L. (сем. Lomiaceae) нами были изучены флавоноиды Scutellaria immaculata Nevski (шлемник незапятнанный) и Scutellaria ocellata Juz (шлемник глазковый). Из корней и надземной части S. immaculata наряду с известными флавоноидами (±)-5,2'-дигидрокси-6,7,6'-триметок- сифлаваноном, (−)-5,2'-дигидрокси-6,7,8,6'-тетраметоксифлаваноном, хризином, вогонином, апигенином, изоскутеллареином, скутеллареином, хризин-7-О-β-D- глюкуронидом, байкалеин-7-О-β-D-глюкозидом, ороксилозидом, скутеллареин- 7-О-β-D-глюкозидом, космосиином, вогонозидом выделены два новых флавоноида, относящихся к производным флавона, а из надземной части S. ocellata были выделены известные флавоноиды: ороксилин А, вогонин, апигенин, 3,4',7-тригид- роксифлавон, 5,7-дигидрокси-6,8-диметоксифлавон, цинарозид, байкалин и вогонозид.
На основании изучения продукта кислотного гидролиза, ацетилирования, а также по данным ИК, УФ, масс и ПМР спектров, установлено строение новых соединений – иммакулозида (5,8-диметокси-7-О-β-D-глюкопиронозилфлавон) 1 и вогонин-7-О-β-D-глюкопиранозида 2.
OH |
|
OMe |
OH |
OMe |
|
|
O |
O |
O Ph |
O |
O |
O |
Ph |
HO |
OH |
|
HO |
OH |
|
|
OH |
|
OMe O |
OH |
OH |
O |
|
|
1 |
|
|
2 |
|
|
236 |
Стендовые доклады |

Функционализация 3,5-дигалоген-6H-6-оксоантра- [1,9-cd]изоксазолов аминокислотами
Юносова О.Н., Дружинина В.Л., Лаврикова Т.И., Горностаев Л.М.
Красноярский государственный педагогический университет 660049, Красноярск, ул. Лебедевой, 89
Известно [1], что галогенантрахиноны 1 реагируют с аминокислотами лишь в жестких условиях, причем в ряде случаев аминирование сопровождается декарбоксилированием и циклизацией в пирролантроны 2.
O Cl |
O |
N |
|
||
N |
OH |
|
H |
|
|
Cu, ∆ |
|
|
O |
|
O |
1 |
|
2 |
Между тем, интерес представляют производные антрахинона, содержащие в качестве заместителей именно остаток аминокислоты, поскольку некоторые из подобных аминокислот и их амидов обладают биологической, в том числе антиопухолевой активностью.
Найдено, что 3,5-дибром-6H-6-оксоантра[1,9-cd]изоксазол 3 реагирует с солями α-, β-, γ-, δ-аминокислот без катализаторов в довольно мягких условиях, причем нуклеофильному аминированию подвергается преимущественно несколько более активное положение 5.
O |
N |
|
|
O |
N |
|
|
|
Br |
|
O |
|
|
Br |
|
|
+ |
H2N |
( )n |
OH |
|
O |
|
|
|
|
|
|
|||
O |
|
|
|
|
|
|
|
Br |
|
|
O |
HN |
( )n |
OH |
|
3 |
|
n = 1−4 |
4 |
|
|||
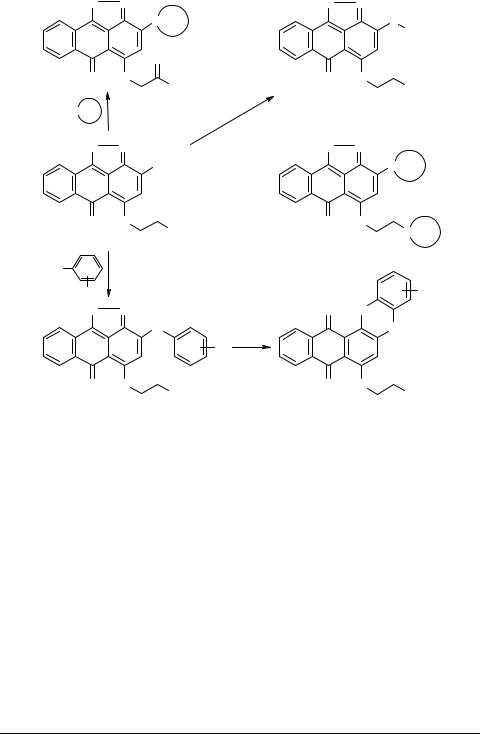
Соединения 4 представляют интерес в качестве промежуточных продуктов, поскольку они могут быть модифицированы как за счет нуклеофильного замещения брома, так и путем функционализации карбоксильной группы.
Генеральный спонсор и организатор – InterBioScreen Ltd. |
237 |
O N
N |
|
O |
|
O HN ( )n |
OH |
HN |
RSH |
O N
Br
 ..
.. 
O
O 4 HN ( )n
 OH
OH
HO
R
O N
O
R
O
O HN ( )n
 OH
OH
O N
S R
O
O HN ( )n
 OH
OH
O N
N
O O HN ( )n
 N
N
R
O HN
O
O
O HN ( )n
 OH
OH
1.Methoden der Organischen Chemie (Houben-Weyl), Stuttgart: Thieme, 1979, Bd. 7/3c.
238 |
Стендовые доклады |
Биологическая активность функционально замещенных нитропроизводных бензофуроксана
Юсупова Л.М.1, Спатлова Л.М.1, Фаляхов И.Ф.1, Гарипов Т.В.2, Шиндалла М.2
1Казанский государственный технологический университет 420015, Казань, ул. Маркса, 68 2Казанская государственная академия ветеринарной медицины 420074, Казань, Сибирский тракт, 35
До настоящей работы системные исследования биологической активности в ряду бензофуроксанов не проводились. Нами впервые систематически изучено эмпирическим путем на тест-объектах влияние строения производных бензофуроксана на фунгицидную, бактерицидную, акарицидную и другие виды активности и выявлена зависимость биологической активности в зависимости от структуры.
В связи с высоким интересом к препаратам, подавляющим грибы Aspergilius niger, исследования в этом направлении являются первоочередными. Исследования позволили установить высокую биологическую активность in vitro по отношению к плесневым грибам 4,6-дихлор-5-нитробензофуроксана 1 (100% гибель грибов при конц. 0.003%).
Cl
O2N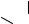 N
N
O
Cl N
N
1 O
Установлено, что немаловажное значение для фунгицидной активности имеет количество атомов галогена. Это подтверждается на примере, когда один атома хлора в 4,6-дихлор-5-нитробензофуроксана заменен на азидную группу, где фунгицидная активность понижается на порядок по сравнению с исходным 4,6-ди- хлор-5-нитробензофуроксаном. Замечено, что активность зависит и от природы заместителя. При введении оксигруппы вместо галогенов соединение становится нейтральным по отношению к грибам.
Нами установлено влияние на фунгицидную активность и количества нитрогрупп. Показано, что с увеличением количества нитрогрупп в структуре фунгицидная активность понижается. 5,7-Дихлор-4,6-динитробензофуроксан 2 проявляет значительно меньшую активность по отношению к грибам Aspergilius niger, чем 4,6-дихлор-5-нитробензофуроксан (100% гибель грибов при конц. 0.25%).
Генеральный спонсор и организатор – InterBioScreen Ltd. |
239 |

NO2
Cl N
O
O2N N
Cl
O
2
Результаты представлены в таблице 1.
Таблица 1. Фунгицидная активность соединений бензофуроксанового ряда
Соединение |
Кон- |
Торможение роста мицелия грибов, |
|||
|
цент- |
|
% к контролю |
|
|
|
рация, |
Asper. niger |
Coniofora |
R. Solani |
H. Sativum |
|
% |
|
cerebella |
|
|
|
|
|
|
|
|
4,6-дихлор-5-нитро- |
0.0001 |
22 |
– |
17 |
32 |
бензофуроксан |
0.0005 |
40 |
– |
39 |
40 |
|
0.001 |
50 |
– |
50 |
50 |
|
0.003 |
100 |
– |
100 |
100 |
|
0.006 |
100 |
– |
100 |
100 |
|
0.01 |
100 |
16 |
– |
– |
|
0.05 |
100 |
100 |
– |
– |
5,7-дихлор-4,6-динит- |
0.001 |
– |
67 |
– |
– |
робензофуроксан |
0.003 |
– |
100 |
– |
– |
|
0.005 |
– |
100 |
– |
– |
|
0.007 |
– |
100 |
– |
– |
|
0.01 |
83 |
100 |
– |
– |
|
0.02 |
95 |
100 |
– |
– |
|
0.03 |
100 |
100 |
– |
– |
|
0.05 |
100 |
100 |
– |
– |
4-азидо-6-хлор-5-нит- |
0.01 |
57 |
78 |
– |
– |
робензофуроксан |
0.02 |
83 |
– |
– |
– |
|
0.03 |
100 |
100 |
– |
– |
|
0.05 |
100 |
100 |
– |
– |
5-хлор-4,6-динитро- |
0.01 |
0 |
0 |
– |
– |
бензофуроксан |
0.05 |
0 |
0 |
– |
– |
5-гидрокси-4,6-динит- |
0.01 |
0 |
30 |
– |
– |
робензофуроксан |
0.05 |
45 |
50 |
– |
– |
5,7-дибром-4,6-ди- |
0.01 |
0 |
100 |
– |
– |
нитробензофуроксан |
0.05 |
45 |
100 |
– |
– |
5,7-дигидрокси-4,6-ди- |
0.01 |
5 |
32 |
– |
– |
нитробензофуроксан |
0.05 |
36 |
62 |
– |
– |
Эталон-каменно- |
0.01 |
– |
91 |
– |
– |
угольная смола |
0.02 |
– |
100 |
– |
– |
|
0.003 |
90–100 |
– |
– |
– |
240 |
Стендовые доклады |
