
RCL_11
.pdfРаздел 6. Разное |
261 |
|
|
риска развития коагулопатии. Данное исследование проверяет гипотезу об отсутствии увеличения кровопотери и потребности в трансфузиях при коррекции волемии 6% ГЭК 130/ 0,4 в дозе до 50 мл/кг (приблизительно в 1,5 раза превышает дозу, рекомендованную производителем) в сравнении с 6% ГЭК 200/0,5 (средняя молекулярная масса 200 кД, степень замещения 0,5) в дозе до 33 мл/кг при плановом АКШ.
Материалы и методы
Пациенты
Исследование было проведено в период с августа 2000 по апрель 2001 года в университетской больнице на 1400 коек. После получения согласия от этического комитета медицинского факультета Кельнского университета (Кельн, Германия) 120 пациентов, готовившихся к плановой операции АКШ, дали письменное информированное согласие на свое участие в исследовании. Пациенты считались подходящими для исследования, если их возраст был в пределах 40-75 лет и индекс массы тела 19-30 кг/м2. Критериями исключения были следующие: фракция выброса левого желудочка мене 40%, недавний (< 7 дней) или текущий прием препаратов, влияющих на свертываемость крови, нарушение показателей коагуляционного теста (протромбиновое время [международное нормализованное отношение] > 1,2, активированное частичное тромбопластиновое время > 40 сек., содержание тромбоцитов < 100 х 109 /л), концентрация плазменного креатинина более 1,5 мг/дл, а также установленный факт аллергической реакции на ГЭК.
Протокол
Путем рандомизации пациенты были разделены на две группы: получающие либо до 50 мл/кг 6% ГЭК 130/0,4 (Волювен; Fresenius Kabi, Bad Homburg, Германия) или до 33 мл/кг 6% ГЭК 200/0,5 (6% HAES-steril; Fresenius Kabi) с целью возмещения внутрисосудистого объема во время операции и в течение последующих 24 часов. Рандомизация была основана на коде, генерированном компьютером. Оба раствора ГЭК размещались в идентично выглядящих последовательно пронумерованных пластиковых упаковках, содержащих в соответствии с кодом рандомизации либо 6% ГЭК 130/0,4, либо 6% ГЭК 200/0,5. Первые 33мл/кг ГЭК назначались при двойном слепом контроле. В дальнейшем препарат рассекречивался для исследователя с целью возможности использования ГЭК в соответствующей максимальной дозировке. Пациент оставался в неведении относительно используемого препарата в течение всего периода исследования. В обеих группах при достижении максимальных соответствующих доз ГЭК дальнейшая коррекция волемии при необходимости проводилась 4% раствором желатина полисукцината (Gelafundin; B.Braun, Melsungen, Германия). Необходимость использования коллоидных растворов и их объем определялись лечащим врачом, а не диктовались требованиями протокола. Основным показанием к использованию коллоидных препаратов была гиповолемия, предполагаемая при низком давлении наполнения сердца, значительном колебании формы волны артериального давления, при гипотензии, тахикардии и низкой скорости диуреза.
Всем пациентам проводилось стандартное анестезиологическое пособие с использованием суфентанила, пропофола и панкурония. После интубации трахеи вентиляция осуществлялась с использованием полуоткрытого контура и 50 %-го кислорода. Дыхательный объем и частота вентиляции подбирались таким образом, чтобы поддерживать парциальное напряжения углекислого газа в артериальной крови в пределах 36-44 мм рт.ст., за исключением периода полного искусственного кровообращения (ИК). Состояние гипокоагуляции достигалось использованием гепарина в начальной дозе 300 Ед/кг путем его внутривенного введения перед канюляцией аорты. Дополнительное введение гепарина осуществляли при значении активированного времени свертывания менее 600 сек. ИК осуществляли неокклюзирующим роликовым насосом и волоконным мембранным оксигенатором (Quadrox; Jostra, Hirrlingen, Германия). Контур заправлялся 1000 мл ГЭК (6% ГЭК 130/0,4 или 6% ГЭК 200/0,5, в зависимости от группы исследования), 1000 мл раствора Рингера лактата, 50 мл бикарбоната
262 |
Освежающий курс лекций. 11-й выпуск |
|
|
натрия и 2000 Ед гепарина. У всех пациентов использовался стандартный режим применения апротинина (2 х 106 калликреин инактивирующих единиц [КИЕ] в контур АИК, 2 х 106 КИЕ в виде внутривенной болюсной инъекции перед началом ИК с последующей непрерывной инфузией 5 х 105 КИЕ/ч до окончания ИК). Насосный поток поддерживался на уровне 2,4 л/ мин/м2 на фоне умеренной гипотермии (температура в мочевом пузыре > 30°С). Остановка сердца осуществлялась введением 20 мл/кг холодного кардиоплегического кристаллоидного раствора (раствор Bretschneider, Кустодиол; Dr.Franz Koehler Chemie, Alsbach-Haenlein, Германия). При необходимости поддержания давления наполнения в контур АИК добавлялся раствор Рингера лактата. Эритроцитарная масса вводилась при уровне гемоглобина менее 70 г/л. После согревания пациента до 37°С и прекращения ИК 80% накопленной дозы гепарина нейтрализовывалось внутривенным введением протамина гидрохлорида. Нейтрализация гепарина считалась адекватной, если активированное время свертывания после протамина не отклонялось более 10% от первоначального значения (перед введением гепарина). Дополнительная доза протамина вводилась, если активированное время свертывания после введения расчетной дозы протамина не достигало 10%-го интервала первоначального значения. Остаточная кровь из контура АИК пропускалась через устройство, сохраняющее эритроциты (Brat2; Cobe Cardiovascular, Inc.,Arvada, CO), которые во всех случаях возвращались пациенту.
В послеоперационном периоде пациенты переводились в отделение интенсивной терапии, где продолжалась искусственная вентиляция легких до достижения гемодинамической стабильности и прекращалась при отсутствии значительного кровотечения. Значимым кровотечение считалось при сбросе по дренажу более 200 мл/ч в течение 2 последовательных часов. Инфузионная терапия в отделении интенсивной терапии основывалась на использовании кристаллоидных растворов (40-60 мл/ч). Дополнительная инфузия назначалась при необходимости, по усмотрению дежурного врача. Эритроцитарная масса переливалась при уровне гемоглобина менее 90 г/л. Свежезамороженная плазма и тромбоконцентрат, соответственно, переливались для коррекции микрососудистого кровотечения (сброс по дренажу > 200 мл/ч в течение 2 последовательных часов) при наличии ненормальных показателей коагуляционного теста (протромбиновое время [международное нормализованное отношение] > 1,5, активированное частичное тромбопластиновое время (АЧТВ) > 60 сек., уровень фибриногена < 1 г/л, содержание тромбоцитов < 50 х 109 /ë).
Объем отделяемого по дренажной трубке регистрировался в течение 24 часов после операции. Регистрация осуществлялась на 6, 12, 18 и 24 часа после операции лицом, не принимающим непосредственное участие в исследовании и не осведомленным о группе, в которую включен пациент. Спустя 2 и 6 часов после операции из дренажной трубки забирали образец отделяемой жидкости для определения уровня гематокрита. Необходимость использования компонентов крови регистрировали в течение 7 дней послеоперационного периода. Образцы крови для лабораторных тестов забирались до индукции в анестезию, при переводе в ОИТ, спустя 24 часа от поступления в ОИТ и на 7 день после операции. Лабораторные тесты включали определение уровня гемоглобина, содержания тромбоцитов, протробинового времени, АЧТВ, плазменной концентрации фибриногена и плазменный уровень креатинина. У последних 40 пациентов (20 пациентов каждой группы) также определяли активность VIII фактора, антиген фактора вон Виллебранда и активность кофактора ристоцетина.
Статистический анализ
Основным фактором сравнения была величина послеоперационной кровопотери, которая определялась по величине сброса по дренажной трубке в течение первых 24 часов после операции.
Результаты представлены в виде среднего значения ± стандартное отклонение и медианы (межквартельных интервалов) для параметрически и непараметрически распределенных данных, соответственно. Характеристики пациента и данные относительно оперативного вмешательства сравнивались t тестом Стьюдента. Лабораторные показатели сравнивались с помощью дисперсионного анализа для повторных измерений. Объемы инфузий, объемы сброса по дренажным трубкам, гематокрит дренажной жидкости и периоперационная
Раздел 6. Разное |
263 |
|
|
потребность в препаратах крови сравнивались U тестом Манна-Уитни. Пропорции сравнивались с помощью точного теста Фишера и теста хи-квадрат. Все тесты были двусторонними с p < 0,05, выбранным в качестве критерия значимости различий.
Результаты
Сто двадцать пациентов были включены в исследование, и у 117 пациентов (ГЭК 130/0,4, 59 пациентов; ГЭК 200/0,5, 58 пациентов) исследование было завершено согласно протоколу. Трое пациентов (ГЭК 130/0,4, 1 пациент; ГЭК 200/0,5, 2 пациента) потребовали повторного обследования в связи с кровотечением, которое было связано с локальным гемостазом, а не генерализованным кровотечением. В связи с тем, что эти пациенты потребовали повторного хирургического обследования в течение 24 часов после операции, то основной показатель сравнения (дренажный сброс за 24 часа) не был получен у данных пациентов. Таким образом, данные пациенты были исключены из анализа. Демографические показатели и базовые лабораторные показатели, полученные у 117 пациентов, значимо не отличались между группами (таблицы 1 и 2).
Средняя доза ГЭК, введенных пациентам во время операции и в течение последующих 24 часов, составила 49 (межквартельный разброс 21-53) мл/кг и 33 (29-40) мл/кг в группах ГЭК 130/0,4 и ГЭК 200/0,5, соответственно (p < 0,001). Пациенты в группе ГЭК 130/0,4 потребовали меньшую дозу препаратов желатина в дополнение к ГЭК, чем пациенты группы ГЭК 200/0,5(7 [0-60] против 20 [0-58] мл/кг, p < 0,001). Двадцать один пациент (36%) группы ГЭК 130/0,4 против 3 пациентов(5%) группы ГЭК 200/0,5 (p < 0,001) не потребовали дополнительного введения препаратов желатина. Общий объем коллоидных препаратов (комбинация ГЭК и желатина), введенных пациентам за время операции и в течение последующих 24 часов, значимо не различался между группами (таблица 3).
Объем отделяемого по дренажной трубке в первые 24 часа после операции варьировал от 380 до 1440 мл в группе ГЭК 130/0,4 и от 330 до 1750 мл в группе ГЭК 200/0,5 (различие между медианами: 45 мл, p = 0,60; таблица 4). У 9 пациентов группы ГЭК 130/0,4 и 10 пациентов группы ГЭК 200/0,5 (p = 0,77) сброс по дренажной трубке за 24 часа составил более 1000 мл. Гематокрит отделяемого по дренажной трубке при измерении его спустя 2 и 6 часов после операции значимо не отличался между группами (таблица 4).
Периоперационная потребность в переливании эритроцитов была схожей в обеих группах (таблица 4). Десяти пациентам группы ГЭК 130/0,4 и 19 пациентам группы ГЭК 200/0,5 (p = 0,056) переливали в среднем 2 единицы свежезамороженной плазмы. Общий объем перелитой свежезамороженной плазмы составил 24 и 41 единицу в группах ГЭК 130/0,4 и ГЭК 200/0,5, соответственно. Ни один пациент обеих групп не потребовал переливания тромбоконцентрата иликриопреципитата.Количествопациентов,потребовавшихпереливаниякакого-либокомпонента крови (исключая эритроциты, сохраненные из АИК), значимо не различалось между группами (33 против 37 пациентов в группах ГЭК 130/0,4 и ГЭК 200/0,5, соответственно, p = 0,45).
Результаты коагуляционных тестов и уровня плазменного креатинина значимо не различались между группами в течение всего периода исследования. Двум пациентам группы ГЭК 130/0,4 и 3 пациентам группы ГЭК 200/0,5 проводилась продленная веновенозная гемофильтрация в течение 4 дней с целью лечения острой почечной недостаточности. Зарегистрировано по одному внутрибольничному летальному исходу в каждой группе (ГЭК 130/0,4: сердечная недостаточность; ГЭК 200/0,5: септический шок). Все развившиеся серьезные осложнения и летальные исходы расценены как возможные естественные осложнения операций на открытом сердце.
Обсуждение
Мы установили, что возмещение внутрисосудистого объема с помощью 6% раствора ГЭК 130/0,4 в средней дозе 49 мл/кг не увеличивает послеоперационную кровопотерю и потребность в гемотрансфузиях при плановых операциях АКШ в сравнение с 6% раствором
264 |
Освежающий курс лекций. 11-й выпуск |
|
|
ГЭК 200/0,5, используемого в дозах, рекомендуемых производителем (33мл/кг). В связи с тем, что максимальная доступная доза ГЭК 200/0,5 ниже, пациентам группы ГЭК 200/0,5 проводили инфузию препаратов желатина почти в 3 раза больше, чем пациентам группы ГЭК 130/0,4. Данное обстоятельство может свидетельствовать о вероятной склонности к меньшей кровопотере в группе ГЭК 200/0,5, т.к. считается, что желатин не влияет на коагуляцию (по крайней мере, при использовании в не очень высоких дозах). К тому же, установлено, что комбинация ГЭК с желатином нарушает коагуляцию в меньшей степени, чем ГЭК изолированно. Так же важно отметить, что общий объем коллоидов значимо не различался между ГЭК 130/0,4 и ГЭК 200/0,5 группами.
В одном из предыдущих исследований отмечено, что возмещение объема 6% раствором ГЭК 130/0,4 в дозе 31 мл/кг в сравнение с 6% раствором ГЭК 200/0,5 в дозе 31 мл/кг может уменьшить величину кровопотери при АКШ. В данном исследовании объем отделяемого по дренажной трубке был на 390 мл меньше в группе ГЭК 130/0,4, чем в группе ГЭК 200/0,5, однако различие (800 ± 486 против 1192 ± 1225 мл) было незначимым. Мы установили, что объем отделяемого по дренажной трубке оказался фактически одинаковым в обеих группах. Учитывая, что в нашем исследовании ГЭК 130/0,4 инфузировался в дозе в 1,5 раза большей, чем ГЭК 200/0,5, возможным объяснением может быть меньший относительный риск кровотечения при инфузии ГЭК 130/0,4 в сравнение с ГЭК 200/0,5. Другим возможным объяснением может быть схожий эффект двух растворов ГЭК на послеоперационную кровопотерю, не зависящий от дозы. Так как в нашем исследовании не было группы «без ГЭК», то также возможно, что оба раствора ГЭК повышают кровопотерю в сравнение с другими типами растворов.
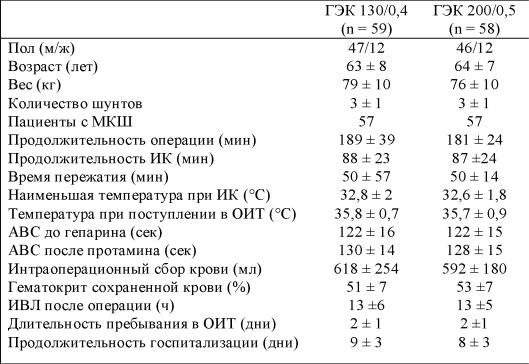
Таблица 1. Пациенты и манипуляции
Данные приведены в виде среднего значения ± стандартное отклонение, либо в виде абсолютных чисел. Не отмечено каких-либо значимых различий между группами.
АВС – активированное время свертывания; ГЭК – гидроксиэтилкрахмал; ИК – искусственное кровообращение; МКШ – маммаро-коронарное шунтирование; ОИТ – отделение интенсивной терапии; ИВЛ – искусственная вентиляция легких.

Раздел 6. Разное |
265 |
|
|
Некоторые ограничения в нашем исследовании должны быть учтены при интерпретации результатов. Во-первых, данное исследование не имело полный двойной слепой контроль.
В данном контексте может оказаться полезным недавнее исследование, в котором показано отсутствие различий в объеме дренажного отделяемого и показателях коагуляции между группами пациентов, которым вводили 40 мл/кг 6% ГЭК 130/0,4 либо желатина с целью возмещения внутрисосудистого объема во время плановой кардиооперации и в течение последующих 24 часов. Авторы пришли к выводу, что в отношении коагуляционного гемостаза возмещение объема у кардиохирургических пациентов 6% раствором ГЭК 130/0,4 является сходным по безопасности с раствором желатина.
Таблица 2. Лабораторные показатели
Данные приведены в виде среднего значения ± стандартное отклонение.
Нормальные значения: гемоглобин, мужчины: 13,5-18 г/дл, женщины: 12-16 г/дл; содержание тромбоцитов: 150-400 х 109/л; протромбиновое время (международное нормализованное отношение [МНО]): ≤1,2; активированное частичное тромбопластиновое время (АЧТВ): ≤38 сек., фибриноген: 1,8-3,5 г/л; креатинин, мужчины: 0,5-1,1 мг/дл, женщины: 0,5-0,9 мг/дл, фактор VIII: C: 50-200%, антиген фактора вон Виллебранда: 50-150%, ристоцетиновый кофактор: 50-150%.

266 |
Освежающий курс лекций. 11-й выпуск |
|
|
Базовые данные – до индукции в анестезию; ГЭК – гидроксиэтилкрахмал; 24ч в ОИТ – спустя 24 часа от момента перевода в отделение интенсивной терапии; НВ – тест не выполнялся.
Рассекречивание группы исследования происходило после инфузии 33 мл/кг ГЭК с целью принятия решения о дальнейшей инфузии препарата. Во-вторых, в условиях отсутствия контрольной группы «без ГЭК», невозможно сделать выводы относительно влияния ГЭК на послеоперационную кровопотерю в сравнение с другими типами внутривенных растворов. Мы надеемся, что не придерживаясь строгих протоколов коллоиды войдут в рутинную клиническую практику. К счастью, общий инфузируемый объем коллоидов значимо не различался между группами, что свидетельствует о сходстве критериев применения коллоидных препаратов у всех пациентов.
В заключении, мы выявили, что возмещение внутрисосудистого объема с помощью 6% раствора ГЭК 130/0,4 в средней дозе 49 мл/кг не увеличивает послеоперационную кровопотерю и потребность в гемотрансфузиях при плановых операциях АКШ в сравнение с 6% раствором ГЭК 200/0,5, используемого в рекомендуемой производителем дозировках 33мл/кг. Основываясь на данных, полученных в данном исследовании, производитель недавно получил согласие руководства Европейского Сообщества на увеличение максимальной рекомендованной доза для 6% ГЭК 130/0,4 с 33мл/кг в день до 50 мл/кг в день.
Таблица 3. Периоперационная инфузия
Данные представлены в виде медианы (межквартельных интервалов)
Раздел 6. Разное |
267 |
|
|
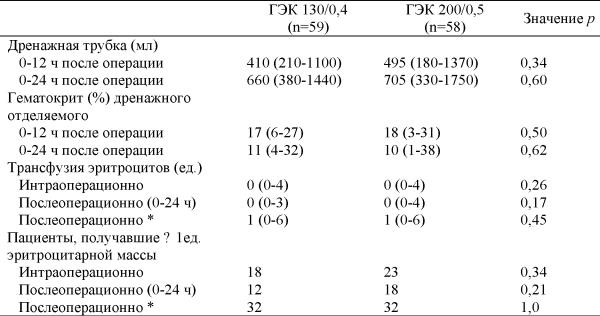
Таблица 4. Сброс по дренажной трубке и потребность в переливании эритроцитарной массы
Данные представлены в виде медианы (межквартельных интервалов) или в виде абсолютных чисел.
* От момента индукции в анестезию и до 7 дней после операции.
268 |
Освежающий курс лекций. 11-й выпуск |
|
|
ПАРЕНТЕРАЛЬНЫЙ L-АЛАНИЛ-L-ГЛУТАМИН УЛУЧШАЕТ ОТДАЛЕННЫЕ ИСХОДЫ У ПАЦИЕНТОВ, НАХОДЯЩИХСЯ В КРИТИЧЕСКОМ СОСТОЯНИИ
Ê.ГОТЕРС, А. ВЕНН, Н. МЕРТЕС, К. ВЕМП, Х. ВАН АНКЕН,
Ï.СТЕЛ, Г. Д. БОН (г. Мюнстер, Германия)
Цели исследования: глутамин является условно незаменимой аминокислотой. Цель настоящего исследования – установить, влияет ли дополнительное введение L-аланил-L-глута- мина в состав парентерального питания на результаты лечения пациентов отделения интенсивной терапии.
Дизайн: проспективное открытое рандомизирированное исследование.
Условия: университетская клиника, ОИТ общехирургического профиля для пациентов, перенесших оперативное вмешательство.
Пациенты: пациенты отделения интенсивной терапии обоих полов с наличием показаний к парентеральному питанию и предположительным сроком пребывания в ОИТ 5 дней и более.
Методы: пациенты были случайно разделены в 2 группы: стандартного парентерального питания и парентерального питания с дополнительным введением L-аланил-L-глутамина (0,3 г/кг массы тела в сутки). Общая доза вводимых парентерально аминокислот составила 1,5 г/ кг массы тела в сутки. Калорическая поддержка осуществлялась под контролем уровня глюкозы и триглицеридов плазмы. Целевой уровень энергетической поддержки рассчитывался по формуле 3 г/кг массы тела углеводов и 1г/кг массы тела липидов в сутки.
Результаты: проводимая медикаментозная терапия, энтеральное и парентеральное питание, витальные функции и данные биохимического мониторинга фиксировались в протоколе исследования. Клинические результаты оценивались по средней продолжительности периода пребывания пациента в отделении интенсивной терапии, общему сроку госпитализации, летальности в отделении интенсивной терапии, летальности в течение 30-дней и 6 месяцев с момента включения в исследование. В общей сложности в исследование были включены 144 пациента: 95 из них находились в ОИТ в течение 5-8 суток, и 68 – в течение 9 и более суток. В группе энтерального питания с добавлением L-аланин-L-глутамина, плазменная концентрация глутамина достоверно повышалась в период с 6-х по 9-е сутки. Выживаемость за период 6 месяцев была значительно выше в группе пациентов, которые получали L-аланин-L-глута- мин в течение 9 суток и более (66,7% по сравнению с 40% в контрольной группе).
Заключение: результаты исследования подтверждают гипотезу, что устранение дефицита глутамина у пациентов ОИТ способствует снижению летальности, которая связана с неадекватным парентеральным питанием (Crit Care Med 2002; 30:2032-2037).
Ключевые слова: глутамин, полное парентеральное питание, интенсивная терапия; исходы.
У пациентов отделения интенсивной терапии часто наблюдается состояние, характеризующееся преобладанием катаболизма в течение продолжительного времени с развитием недостаточности питания. Даже усиленная питательная поддержка не способна предотвратить потерю тощей массы тела и может усугублять метаболические нарушения. Тяжелое состояние, которое не разрешается в течение нескольких дней, требует продленного пребывания в ОИТ, и значительно увеличивает стоимость лечения и нагрузку на персонал. Полиорганная недостаточность и сепсис сопровождаются высокой летальностью. При таких критических состояниях часто наблюдаются недостаточность функции ЖКТ, которая выражается в нарушении усвоения энтерального питания. Данные факторы приводят к удлинению сроков пребывания в ОИТ и увеличивают летальность [1]. Часто возникает необходимость в проведении парентерального питания. Методы интенсивной терапии пациентов, находящихся в кри-
Раздел 6. Разное |
269 |
|
|
тическом состоянии, варьируют незначительно. Маловероятно, что изменение проводимой питательной поддержки существенно повлияет на высокую летальность, которая наблюдается в первые несколько недель заболевания, в течение среднего периода госпитализации [2]. Исход в ранний период, в основном, определяется тяжестью основного заболевания, наличием сопутствующей патологии и возрастом пациента. Однако стратегия питательной поддержки может свести к минимуму потерю тощей массы тела, и, таким образом, способствовать восстановлению пациента и снизить отдаленную летальность.
Глутамин является аминокислотой, которая в свободном состоянии наиболее часто встре- чается в организме человека. У пациентов, находящихся в критическом состоянии, глутамин считается условно незаменимой аминокислотой вследствие того, что потребности в данном соединении превышают синтетические возможности организма [3]. Глутамин является не только субстратом и регулятором синтеза протеинов, но также участвует во многих метаболических и биосинтетических процессах, поддерживает функции быстро пролиферирующих клеток, включая лимфоциты и энтероциты, является переносчиком азота во внеклеточном пространстве.
Растворы аминокислот для парентерального питания, существовавшие до 1995 года, не содержали глутамин, что связано с физико-химическими свойствами данной аминокислоты. Данная проблема была решена за счет синтетических дипептидов, содержащих глутамин. Несколько клинических исследований продемонстрировали, что глутамин или дипептиды, содержащие глутамин, улучшают азотистый баланс в послеоперационном периоде [4-9], поддерживают функцию иммунной системы [10] и ЖКТ [11, 12], повышают скорость синтеза протеинов [5], укорачивают период госпитализации и снижают летальность [6-9, 13-17].
Опыт применения дипептидов, содержащих глутамин, у пациентов ОИТ ограничен. Нет опубликованных данных о применении глутамина у пациентов отделения интенсивной терапии, требующих проведения парентерального питания. Парентеральное введение глутамина у пациентов, находящихся в критических состояниях, было исследовано в 2 работах [14, 17]. Однако в данных исследованиях раствор L-глутамина был добавлен к смесям для парентерального питания. Основная цель настоящего открытого проспективного рандомизированного исследования – изучить влияние добавления L-аланил-L-глутамина на клинические исходы пациентов, находящихся в послеоперационный период в ОИТ в течение 5 дней и более и получающих стандартную терапию. Период лечения 5 дней и более был выбран на основании данных других клинических исследований [7-9]. Был заранее запланирован анализ подгруппы пациентов, которые находились в ОИТ 9 дней и более, для определения эффектов глумина на отдаленные исходы, так как Griffiths [14] и соавторы наблюдали значительное повышение летальности у пациентов, требующих длительного парентерального питания. Результаты терапии оценивались исходя из среднего срока госпитализации и периода пребывания в ОИТ, госпитальной летальности и летальности в ОИТ, а также в течение 30 суток и 6 месяцев с начала заболевания.
Пациенты и методы
Исследование было одобрено этическим комитетом института, который не требовал получения информированного согласия от пациента, так как глутамин обладает потенциально положительным эффектом, о его неблагоприятных эффектах не известно. Пациенты, поступающие в ОИТ, были случайно распределены в 2 группы лечения: стандартное парентеральное питание и парентеральное питание с добавление аланил-глутамина. Для того, чтобы избежать некорректного распределения пациентов, план рандомизации для 4 категорий был составлен заранее отдельно для пациентов травматологического профиля, после операций на внутренних органах, на сердце и сосудах и после прочих операций. Мы определили следующие критерии включения: рандомизация не позднее 3 суток с момента поступления пациента в ОИТ и до начала сбалансированной питательной поддержки, наличие показаний для полного парентерального питания (неэффективность или противопоказания к энтеральному пита-
270 |
Освежающий курс лекций. 11-й выпуск |
|
|
нию), ожидаемый срок пребывания пациента в ОИТ 5 суток и более. Установлены следующие критерии исключения: возраст младше 16 лет, беременные или кормящие женщины, врожденные расстройства метаболизма аминокислот. Перевод пациента из ОИТ или смерть до момента завершения протокола исследования (5 суток) были определены как вторичные критерии исключения. Расчет необходимого объема растворов для парентерального питания осуществлялся по формулам: аминокислоты 1,5 г/кг/сутки (в исследуемой группе 0,3 г/кг/ сутки приходилось на аланил-глутамин, остальные 1,2 г/кг/сутки на аминокислоты, содержащиеся в стандартных растворах аминокислот для парентерального питания). Мониторинг эффективности энергетической поддержки осуществлялся при контроле уровня глюкозы (10 ммоль/л и менее) и триглицеридов в крови (2,8 ммоль/л и менее). Объем суточного восполнения энергетических затрат рассчитывался по формуле 3 г/кг/сутки углеводов и 1 г/кг/сутки жиров. Парентеральное питание осуществлялось по методу раздельного введения питательных компонентов. В качестве препарата, содержащего аланил-глутамин, был выбран коммерчески доступный препарат дипептивен (Fresenius Kabi, Bad Homburg, Germany). Как только позволяла клиническая ситуация, осуществлялся переход на энтеральное питание. Парентеральное введение растворов аминокислот не прекращалось, пока эффективный объем энтерального питания не достигал 700 мл (объем введенной смеси минус рефлюкс). В состав используемых для энтерального питания смесей не входил глутамин. После перехода на энтеральное питание раствор аланил-глутамина назначался в течение всего периода, когда пациент требовал внутривенного введения других препаратов и присутствовал венозный доступ. Оценка проводимой питательной поддержки осуществлялась специалистами в данной области, которые сами не были вовлечены в процесс лечения. Исследование не оказывало влияние на другие направления терапии, кроме искусственного питания.
Во время пребывания в ОИТ ежедневно фиксировались данные о проводимой питательной поддержке, медикаментозном лечении, клинические и лабораторные параметры. При включении в исследование состояние пациента оценивалось при помощи шкалы APACHE II, при этом оценка по Шкале комы Глазго условно принималась равной 15 балам (так как пациенты находились в состоянии медикаментозной седации на ИВЛ). В исследование не были включены пациенты с тяжелыми хроническими заболеваниями, так что по данному пункту шкалы APACHE II все пациенты имели 0 балов. Ежедневно оценивалось выделение азота с мочой, кроме того потери азота оценивались при проведении длительной вено-венозной фильтрации с выполнением хемолюминисцентного анализа [18]. Ежедневно производился рас- чет азотистого баланса. До начала исследования, а затем дважды в неделю в течение периода пребывания в ОИТ выполнялось исследование уровня протеинов (методом нефелометрии BN 100, Dade Behring, Liederbach, Germany) и аминокислот плазмы (методом RP-HPLC-анализа и флюоресценции после предварительной обработки и добавления норвалина в качестве внутреннего стандарта) [19]. Прогностический индекс, оценивающий трофологический статус при воспалительной реакции (Prognostic Inflammatory Nutrition Index), рассчитывался по следующей формуле:
PINI=С-реактивный белок × á1-кислый гликопротеин/преальбумин × альбумин [20].
Для выполнения анализа были определены различные периоды времени: 1- до начала питательной поддержки, 2- проведение искусственного питания в течение 3-5 дней, 3 - проведение искусственного питания в течение 6-9 дней. Отдаленные результаты лечения спустя 6 месяцев после операции оценивались при помощи опроса по телефону пациентов, их родственников или семейных врачей.
Статистический анализ результатов выполнялся с использованием SPSS 10.0 for Windows. Данные были представлены относительными и абсолютными величинами, межгрупповые различия оценивались при помощи ч2-теста. Данные представлены в виде средних величин ± стандартное отклонение. Для статистической обработки данных использовался t-тест Стьюдента для независимых переменных и метод повторных измерений разницы (при значении
