
электив-пособие
.pdf
использованием меченных тритием веществ позво- лили установить окончательно этот факт.
При ферментативном гидролизе происходит гидролиз амидной связи в мидодрине и высвобождение активного лекарства и глицина.
|
|
|
OCH3 |
O |
|
|
|
|
|
OCH3 |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
H O,ферменты |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH-CH -NH- C-CH -NH |
2 |
|
|
|
|
|
|
|
CH-CH -NH |
+ |
HOOC-CH2-NH2 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
2 2 2 |
|
|
2 2 |
||||||||||||
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
OCH3 |
|
|
|
|
|
|
OCH3 |
|
|
||||||||||
|
|
|
|
|
|
|
пролекарство |
|
|
|
|
|
лекарство |
|
|
|||||
3.Одно из целей и направлений |
|
модификации |
|||||||||||||||||||||||||||
лекарств – это придание им способности легче |
|||||||||||||||||||||||||||||
проникать в ЦНС. Для решения этой задачи был |
|||||||||||||||||||||||||||||
предложен следующий подход. Он |
основан на |
|
при- |
||||||||||||||||||||||||||
менении реакции окисления, в результате которой |
|||||||||||||||||||||||||||||
незаряженное пролекарство in vivo переходит в |
|||||||||||||||||||||||||||||
заряженную форму, плохо проникающую через |
|||||||||||||||||||||||||||||
гистогематические барьеры. ( |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
Для ацилирования аминов в этом случае |
|||||||||||||||||||||||||||||
используют N-метил дигидроникотиновую кислоту. |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ге- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ма- |
|
|
|
|
ЦНС |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
то- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
эн- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
це- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
фа- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ли- |
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
O |
C |
|||||||||||
|
|
|
|
|
|
|
|
C |
|
|
|
че- |
|
|
|
|
C |
OH |
|||||||||||
|
|
|
|
|
|
|
|
NH-R |
|
|
|
|
|
|
|
NH-R |
|
|
|
|
|||||||||
R-NH |
|
|
|
|
|
|
|
|
|
|
|
ский |
|
|
|
|
|
|
|
+ |
|
|
+NH2-R |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
2 |
|
|
|
N |
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
N |
|
|
|||||||
лекарство |
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
лекарство |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
||||
|
|
|
CH3 |
|
|
|
|
|
барь- |
|
CH3 |
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
пролекарство |
|
|
|
|
|
A |
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ер |
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
В несколько |
стадий |
лекарство превращается в |
|
амид |
N-метилдигидроникотиновой |
кислоты |
||
(пролекарство). |
Это |
пролекарство |
в |
|
101 |
|
|
|
|

неионизированной форме преодолевает гематоэнцефалический барьер и ферментативно окисляется в ЦНС в заряженное пиридиниевое производное . Образовавшаяся четвертичная соль медленно выводится из мозга, что приводит к накоплению формы «А» и ее постепенному превращению в исходное лекарство в процессе гидролиза. При этом увеличивается и длительность центрального эффекта.
4. В качестве пролекарств известны амиды не
только |
карбоновых |
кислот. |
Существуют |
|
пролекарства |
с сульфамидными и |
фосфамидными |
||
фрагментами. |
Например, |
противоопухолевый |
||
препарат фопурин .Данный препарат содержит фосфамидную группировку и подвергается гидролизу в организме, что обеспечивает пролонгированный эффект.
O
N
NH-P N  Фопурин
Фопурин
N |
|
|
N |
|
CH3 |
|||
|
|
|
||||||
|
||||||||
|
|
|
|
|||||
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(CH3)2N N N
N N
5. |
Распространенным |
способом |
получения |
||
пролекарств |
из |
соединений, |
содержащих |
||
ароматическую первичную аминогруппу, является их превращение в азосоединения. При этом устра-
няется опасность быстрого дезаминирования лекарства в организме. В организме под действием редуктаз эти соединения восстанавливаются в соответствующий амин.
Примером такого типа пролекарств является салазосульфодиметоксин. В промышленности его
получают |
из |
салициловой |
кислоты |
и |
сульфадиметоксина. |
|
|
||
102

|
|
|
|
N |
OCH3 |
|
N |
OCH3 |
|
|
|
|
HNO2 |
+ |
|
||
|
|
|
|
|
SO2 NH |
N |
||
NH |
SO |
2 |
NH |
|
N |
N=N |
||
2 |
|
|
|
|
|
|
|
|
|
сульфадиметоксин |
|
OCH3 |
|
|
OCH3 |
||
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
COOH |
|
OCH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
HO |
N=N |
SO2 NH |
N |
салазодиметоксин |
OCH3 |
|
|
пролекарство |
|
Салазодиметоксин накапливается в ткани кишечника и постепенно расщепляется на два
лекарства |
— ПАСК и сульфадиметоксин, |
которые |
|||||||||||||||||||||||||||||||||||||||||||||||||||
оказывают |
противовоспалительное |
|
и бактерицидное |
||||||||||||||||||||||||||||||||||||||||||||||||||
действия |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OCH3 |
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
||||||||||||||||
HO |
|
|
|
|
|
|
|
|
|
|
N=N |
|
|
|
|
|
|
|
|
|
|
SO2 |
|
|
NH |
|
|
|
|
N |
|
редуктаза |
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OCH3 |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
салазодиметоксин |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пролекарство |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OCH3 |
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|||
|
|
|
|
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
|
NH2 + NH2 |
|
|
|
|
|
|
|
|
|
|
SO2 |
|
|
|
NH |
|
|
|
N |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OCH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
п-аминосалициловая |
сульфадиметоксин |
|
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кислота |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
6. При наличии в молекуле лекарства в α- |
|||||||||||||||||||||||||||||||||||||||||||||||||||||
положении |
|
|
|
|
к |
|
|
|
|
|
|
аминогруппе |
|
|
|
|
|
гидроксила |
или |
||||||||||||||||||||||||||||||||||
меркаптогруппы, а также в случае соединений, содержащих α-аминоамидную группировку, появ- ляются дополнительные возможности их химической модификации. При взаимодействии лекарств с кар-
бонильными |
соединениями |
(альдегидами |
или |
кетонами) |
образуются |
соответственно |
|
оксазолидины, тиазолидины |
и 4-имидазолидиноны : |
||
103 |
|
|
|

|
|
|
|
|
|
|
|
|
|
|
|
C-NH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C-N |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ O=C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
C-OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C-O |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
оксазолидины |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
C-NH |
O=C |
|
|
|
|
|
|
|
|
|
|
|
|
|
C-N |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
C-SH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C-S |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C-NH |
|
|
|
|
|
|
|
|
|
|
|
C-N |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
тиазолидины |
|||||||||||||||||||||
|
|
|
|
|
+ |
O=C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
C- |
NH |
|
|
|
|
|
|
|
|
|
|
|
C-N |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
4-имидазолидины |
||||||||||||||||
|
|
Примером |
|
использования этой |
|
реакции для |
||||||||||||||||||||||
создания |
|
пролекарств |
является |
|
|
модификация |
||||||||||||||||||||||
эфедрина. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
CH |
|
|
CH |
|
CH3 |
R1 |
|
|
|
|
|
|
|
|
CH |
|
|
CH |
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
+ O=C |
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
R2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
NHCH3 |
|
|
|
|
|
|
|
O |
N-CH3 |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
R2 |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
||||||||
Эфедрин кетон модифицированный эфедрин пролекарство)
4. МОДИФИКАЦИЯ ПО КАРБОКCИЛЬНЫМ ГРУППАМ
Существенным недостатком препаратов, содержащих карбоксильные группы, является их побочное ульцерогенное действие, выражающееся при приеме внутрь в поражении слизистой оболочки желудка и двенадцатиперстной кишки. Очевидно, такие осложнения связаны с кислотным характером большинства этих соединений и их низкой растворимостью в воде. Поэтому вполне обоснованными являются многочисленные попытки
104

тем или иным способом биообратимо «замаскировать» их кислотную функцию.
Основной реакцией, используемой для получения пролекарств, в этом случае, так же как и при модификации спиртов и фенолов, является реакция образования сложных эфиров. По отношению к исходной карбоновой кислоте эта реакция называется не ацилированием, а этерификацией. Превращение карбоновых кислот даже в самые простые (метиловые) эфиры приводит к снижению их гастротоксичности при практически полном сохранении противовоспалительных свойств.
Общие схемы реакций:
1. Взаимодействие с фенолами. Карбоновые кислоты с фенолами не реагируют, но с фенолами реагируют хлорангидриды или ангидриды карбоновых кислот.
|
|
|
фенолят натрия |
||||||||
|
|
|
|
|
|
|
ONa |
||||
тионилхлорид |
O |
|
|
|
|
|
O |
||||
|
|
|
|
|
|||||||
|
|
|
|
|
|||||||
O |
SOCl2 |
|
|
|
|
|
|||||
|
|
|
|
|
|||||||
R-C-OH |
R-C-Cl |
|
|
|
|
|
|
R-C-O-C6H5 + NaCl |
|||
|
|
|
|
|
|
|
|
||||
-SO2, HCl |
|||||||||||
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|||
карбоновая |
хлорангидрид |
|
|
|
сложный эфир |
||||||
кислота |
|
|
|
|
|
|
|
|
|
|
|
2. Взаимодействие спиртов возможно как с хлорангидридами и ангидридами карбоновых кислот, так и с самими кислотами.
O |
H+ |
O |
R-C-OH + R1-OH |
|
R-C-O-R1 +H2O |
|
Наиболее известными препаратами- пролекарствами по карбоксильной группе являются производные салициловой кислоты: салол (фенилсалицилат) и метилсалицилат. Салициловая
кислот |
обладает |
побочным |
ульцерогенным |
действием. |
Широко |
применяется |
фениловый эфир |
105

салициловой кислоты (салол). Он используется перорально при инфекционных заболеваниях кишечника. В щелочном содержимом последнего салол распадается на соли салициловой кислоты и фенола, которые и оказывают дезинфицирующее действие.
O |
O |
ONa |
|
C-O-C6H5 |
C-ONa |
||
|
|||
+ NaOH |
+ |
+ H2O |
|
OH |
OH |
|
|
фенилсалицилат |
салицилат |
фенолят |
|
|
натрия |
натрия |
В отечественной медицинской практике применяются еще один сложный эфир салициловой кислоты по карбоксильной группе — метилсалицилат , который также следует рассматривать как ее пролекарство:
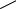 O
O

 C-O-CH3
C-O-CH3
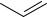
 OH
OH
Метилсалицилат
Метилсалицилат представляет собой жидкость, используется наружно в виде мазей и линиментов. Внутрь он не употребляется, так как при его гидролизе образуется токсичный метиловый спирт.
Другим способом модификации групп СООН является образование амидов.
Общая схема реакции:
O |
t |
O |
|
|
R-C-OH + NH3 |
R-C-NH |
+H O |
||
|
||||
|
|
2 |
2 |
|
карбоновая |
|
амид |
|
|
кислота |
|
карбоновой |
|
|
|
|
кислоты |
|
106

Известен |
амид |
салициловой |
кислоты |
(салициламид), |
амид |
никотиновой |
кислоты |
(никотинамид), |
которые |
отличаются |
лучшей |
переносимостью, |
чем исходная кислота. |
Так в |
|
связи с нейтральной реакцией водных растворов никотинамид, в отличие от свободной никотиновой кислоты, не вызывает местной реакции при инъекциях.
|
|
|
|
O |
|
|
|
|
|
|
O |
|
|
|
|
|
C-NH2 |
|
|
|
|
|
|
C-NH2 |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|||
|
|
|
|
|
|
|
|
|
|
|||
|
|
Cалициламид |
|
|
|
|
Никотинамид |
|
||||
|
|
Одним из интересных способом модификации |
||||||||||
карбоксильных |
групп является |
образование так |
||||||||||
называемых «двойных эфиров». Химическое название
этой реакции |
– образование |
ацилоксиметиловых |
|
эфиров. |
В |
1965 г. было |
установлено, что |
ацилоксиметиловые эфиры быстро гидролизуются в крови животных и человека. Первоначальной стадией гидролиза этих «двойных» эфиров является
ферментативное |
расщепление |
одной |
сложноэфирной |
|
связи |
с |
образованием |
нестабильного |
|
оксиметилового |
эфира, |
который |
спонтанно |
|
превращается в исходное лекарство, отщепляя молекулу формальдегида:
|
|
фермент |
|
|
||
|
|
эстераза |
|
|
||
O |
O |
|
H2O |
O |
спонтанно |
|
|
|
|
R1-C-O-CH2-OH |
|||
R1-C-O-CH2-O-C-R2 |
|
|
R2-COOH + |
|
||
|
|
|
||||
пролекарство |
|
|
карбоновая |
оксиметильный |
|
|
|
|
|
|
кислота |
эфир лекарства |
|
спонтанно
R1-COOH + HO-CH2-OH
лекарство 
 O
O
H2O H-C
H
формальдегид
107

Наряду с формальдегидом при конструировании пролекарств такого типа могут быть использованы и другие альдегиды (ацетальдегид, бензальдегид).
Наиболее интересные результаты использования модификации лекарств этим методом были получены для ампициллина .
|
|
O |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
S |
CH3 |
C6H5- |
|
CH-C-NH |
|
|
|
|
||||
|
|
|
|
|
|
CH3 |
||||
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
NH2 O |
|
N |
|
COOH |
||||||
|
|
|||||||||
|
|
|
|
|||||||
Существует способ химической модификации аспирина и других карбоксилсодержащих нестероидных противовоспалительных средств (индометацина, кетопрофена, ибупрофена, напроксена, диклофенака и др.) путем образования триглицеридов :
O
O CH2-O-C-R |
|
R-C-O-CH O |
остатки монокарбоновых кислот |
CH2-O-C-R
лекарство
остаток |
|
|
|
|
глицерина |
|
|
|
|
Эти |
эфиры |
в |
организме |
легко |
расщепляются под действием ферментов. Они устойчивы в кислой среде, поэтому при приеме внутрь не подвергаются существенному гидролизу в желудке, и их гастротоксичность значительно снижена. В то же время, благодаря высокой липофильности, они легко проникают сквозь стенки кишечника, обеспечивая высокую биодоступность лекарства. Производное противовоспалительного средства индометацина, полученное этим способом,
более активно. Чем простой
108

5. МОДИФИКАЦИЯ ГИДРОКСИКИСЛОТ.
Одним из перспективных способов модификации
γ- гидроксикислот является образование лактонов.
O |
|
|
O |
CH2 -C-OH |
t |
CH2 |
-C |
|
|||
|
|
|
O + H2O |
CH2- CH2-OH CH2- CH2
γ-гидрокси- лактон масляная кислота γ-гидроксимасляной
кислоты
Схимической точки зрения, эта реакция
внутримолекулярной |
этерификации, |
при |
этом |
|||
образующийся |
лактон |
– |
это |
циклический |
||
внутримолекулярный |
сложный эфир. |
При этом |
резко |
|||
повышается |
липофильность |
вещества, |
и |
|||
увеличивается |
всасываемость |
препарата в |
ЖКТ. |
|||
Так γ-оксимасляная кислота при внутривенном введении проявляет анестезирующие свойства и
антипаркинсоновое |
действие, |
но малоэффективна |
||
при |
пероральном |
применении |
из-за |
плохого |
всасывания в кишечнике. Превращение этой кислоты в соответствующий лактон приводит к сильному увеличению всасываемости препарата из ЖКТ. В организме лактон быстро гидролизуется, вновь превращаясь в окоикислоту. В результате, пероральное введение лактона приводит к достижению высокой концентрации у-оксимасляной кислоты в организме, сравнимой с концентрацией, достигаемой при внутривенном ее введении.
109
