
- •1. Моль. Количество вещества эквивалента (эквивалент) и молярная масса эквивалента (эквивалентная масса) простых и сложных веществ. Закон эквивалентов
- •Контрольные вопросы
- •2. Строение атома
- •Электронов на квантовых уровнях и подуровнях
- •Контрольные вопросы
- •3. Периодическая система элементов д.И. Менделеева. Химическая связь и строение молекул
- •Контрольные вопросы
- •4. Энергетика химических процессов (термохимические расчеты)
- •Контрольные вопросы
- •5. Энергия гиббса и направленность химических реакций
- •Контрольные вопросы
- •6. Химическая кинетика и равновесие
- •Контрольные вопросы
- •7. Способы выражения концентрации раствора
- •Контрольные вопросы
- •8. Свойства растворов
- •Контрольные вопросы
- •9. Ионно-молекулярные (ионные) реакции обмена
- •Контрольные вопросы
- •10. Ионное равновесие воды. Водородный показатель рН
- •Контрольные вопросы
- •11. Гидролиз солей
- •Контрольные вопросы
- •12. Окислительно-восстановительные реакции
- •Контрольные вопросы
- •13. Электродные потенциалы и электродвижущие силы
- •Контрольные вопросы
- •14. Электролиз
- •Контрольные вопросы
- •15. Коррозия металлов
- •Контрольные вопросы
- •16. Жесткость воды и методы ее устранения
- •Контрольные вопросы
- •Варианты контрольных заданий
10. Ионное равновесие воды. Водородный показатель рН
Вода является очень слабым электролитом и лишь в незначительной степени диссоциирует на ионы водорода и гидроксила:
Н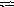 2О
Н+ +
ОН
2О
Н+ +
ОН![]() .
.
Этому процессу соответствует константа диссоциации:
![]() . (1)
. (1)
Константа диссоциации
воды очень мала (КД.(Н![]() О)=
1,86ּ10
О)=
1,86ּ10![]() ),
поэтому равновесная концентрация
недиссоциированных молекул воды
практически равна общей концентрации
воды:
),
поэтому равновесная концентрация
недиссоциированных молекул воды
практически равна общей концентрации
воды:
[H2O]
= СМ
=
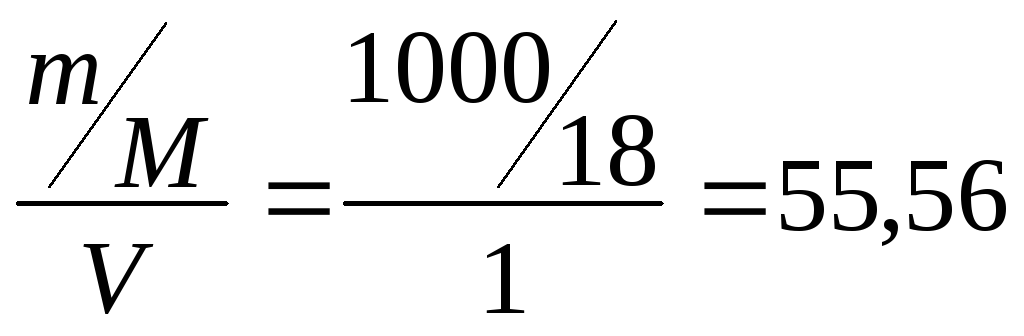 моль/л.
моль/л.
В разбавленных водных растворах концентрация воды меняется незначительно, так что ее можно считать постоянной. Тогда из формулы (1) получим
[H+]ּ[OH![]() ]
= КД.ּ[H2O]
= 1,86ּ10
]
= КД.ּ[H2O]
= 1,86ּ10![]() ּ55,56
= 10
ּ55,56
= 10![]() .
.
Таким образом,
произведение концентраций ионов водорода
и гидроксила представляет собой
постоянную величину (при данной
температуре) и называется ионным
произведением воды КН![]() O.
При стандартной температуре Т = 298К
(250С)
O.
При стандартной температуре Т = 298К
(250С)
КН![]() O
= [H+]ּ[OH
O
= [H+]ּ[OH![]() ]
= 10
]
= 10![]() . (2)
. (2)


Внейтральных растворах [H+]
=ּ[OH
![]() ]
=
10
]
=
10![]() = 10
= 10![]() моль/л.
моль/л.
Для характеристики кислотности (щелочности) среды используется водородный показатель рН – десятичный логарифм концентрации ионов водорода, взятый с обратным знаком:
рН = - lg [H+].
В нейтральных
растворах рН = 7. В кислых растворах [H+]
10![]() ,
следовательно, рН
7; в щелочных растворах [H+]
10
,
следовательно, рН
7; в щелочных растворах [H+]
10![]() ,
поэтому рН
7.
,
поэтому рН
7.
По аналогии с водородным показателем рН введен показатель рОН.
рОН
= - lg [OH![]() ].
].
Логарифмируя соотношение (2), получим рН + рОН = 14.
Пример 1. Определить концентрацию ионов водорода в растворе, если рН = 4,60.
Решение. По условию задачи рН = 4,60 = -lg [H+].
Отсюда [H+] = 10-4,60 = 2,5.10-5 моль/л.
Пример
2. Определть
концентрацию ионов [OH![]() ]
в растворе, если рН = 10,80.
]
в растворе, если рН = 10,80.
Решение. Из соотношения рН + рОН = 14 находим
ОН = 14 – 10,80 = 3,20.
Отсюда –lg
[OH![]() ]
= 3,20. Следовательно [OH
]
= 3,20. Следовательно [OH![]() ]
= 10-3,20
= 6,31.10-4.
]
= 10-3,20
= 6,31.10-4.
Пример 3. Вычислить рН 0,01 М раствора гидроксида натрия.
Решение. Гидроксид натрия является сильным основанием, диссоциирует на ионы практически полностью
NaOH
= Na+
+ OH![]() .
.
Из уравнения
диссоциации следует, что из одного моля
гидроксида натрия образуется один моль
ионов OH![]() ,следовательно
в 0,01 М растворе [OH
,следовательно
в 0,01 М растворе [OH![]() ]
= 0,01. Найдем рОН = - lg
[OH
]
= 0,01. Найдем рОН = - lg
[OH![]() ]
= -lg
0,01 = 2.
]
= -lg
0,01 = 2.
Отсюда рН = 14 – рОН = 12.
Контрольные вопросы
Определите рН раствора, в 0,5 л которого содержится 0,05 г NaOH. Ответ: 11;40.
Во сколько раз концентрация ионов водорода в крови (рН = 7,36) меньше, чем в желудочном соке (рН = 1,00)? Ответ: В 2,3∙10
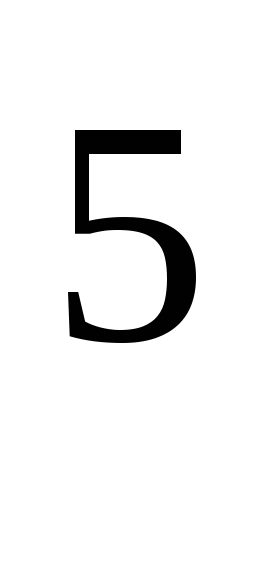 раз.
раз.Определите [H+] и [OH
 ]
в растворе, рН которого равен 6,2.
Ответ:
6,3∙10
]
в растворе, рН которого равен 6,2.
Ответ:
6,3∙10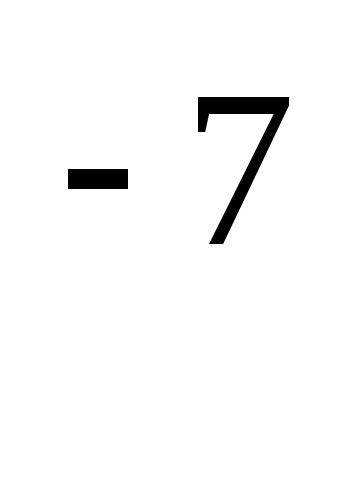 моль/л; 1,6∙10
моль/л; 1,6∙10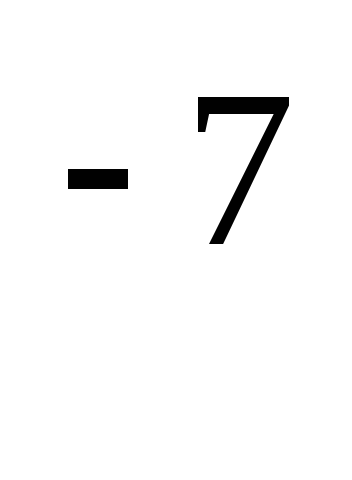 моль/л.
моль/л.Рассчитайте рН раствора, полученного смешением 25 мл 0,5 М раствора HCl, 10мл 0,5 М раствора NaOH и 15 мл воды. Ответ: 0,82.
Как изменится рН 0,2 М раствора HCl, если его вдвое разбавить водой?
Ответ: Увеличится на 0,3.
Вычислите рН 0,5%-ного раствора азотной кислоты. Ответ: 1,10.
К 500 мл воды прибавили 20 мл 0,1 н раствора НС1. Найдите рН полученного раствора.
Ответ: 2,4.
Вычислите рН 1,5%-ного раствора КОН. Ответ: 13,43.
25 мл 10%-ного раствора HCl (плотность 1,05) разбавили водой до 500 мл. Вычислите рН полученного раствора. Ответ: 0,84.
К 250 мл нейтрального раствора прибавили 50 мл 0,5 н раствора КОН. Вычислите рН полученного раствора. Ответ: 12,9.
10,0 мл 20%-ного раствора КОН (плотность 1,18) разбавили водой до 250 мл. Вычислите рН полученного раствора. Ответ: 13,23.
В мерную колбу на 250 мл налили 10,0 мл 24%-ного раствора HCl (плотность 1,12) и довели раствор водой до метки. Из полученного раствора 5,0 мл перенесли в мерную колбу на 100 мл и разбавили водой до метки. Найдите рН полученного раствора.
Ответ: 1,83.
К 25 мл 0,2 н раствора HCl прибавили 25 мл 0,1 н раствора NaOH.Вычислите рН полученного раствора.
Ответ: 1,3.
20,0 мл 12%-ного раствора NaOH (плотность 1,14) разбавили водой до 500 мл. 50,0 мл полученного раствора перенесли в другую колбу и разбавили водой до 1000 мл. Найдите рН последнего раствора. Ответ: 11,85.
К 100 мл 0,1 н раствора HNO3 прибавили 2 мл 6%-ного раствора NaOH (плотность 1,0). Найдите рН полученного раствора. Ответ: 1,2
Найдите рН раствора, в 100 мл которого содержится 0,12 мг NaOH. Ответ: 9,48.
К 100 мл 0,1 н раствора NaOH прибавили 5 мл 4%-ного раствора HCl (плотность 1,0). Найдите рН исходного и полученного раствора. Ответ: 13; 12,6.
К 100 мл 0,2 н раствора HCl прибавили 5 мл 3%-ного раствора КОН. Найдите рН исходного и полученного раствора. Ответ: 0,7; 0,78.
Какую массу NaOH следует растворить в 400 мл воды, чтобы получить раствор, рН которого равен 12?
Вычислите молярную концентрацию раствора гидроксида бария, если известно, что рН данного раствора равен 11.
