
ГОСы Все предметы / Биотехнология / 26.6 новые лактамы
.doc26. 6. На фармацевтическом рынке имеется большое количество полусинтетических пенициллинов.
Определите целесообразность увеличения номенклатуры полусинтетических пенициллинов на примере цефамицина, имипенема, монобактама-азтреонама.
Поиск новых природных беталактамов и целенаправленная трансформация беталактамной молекулы
В настоящее время одной из важных задач биотехнологии является поиск новых антибиотиков.
Это связано с несколькими причинами
1) резистентность микроорганизмов к широко используемым антибиотикам
2) рост числа бактерий, вызывающих инфекционные заболевания
3) использование антибиотиков в пищевой промышленности (как консерванты)
4) использование антибиотиков в научных исследованиях
Показано, что действие антибиотиков-беталактамов в бактериальной клетке обусловлено взаимодействием их с разными видами пенициллин связывающих белков (РВРs). Преимущественное воздействие на белок того или иного вида ведет к разным эффектам - литическому, бактерицидному без лизиса, бактериостатическому с разной длительностью бактериостазиса и т. п.
У некоторых встречающихся в клинике резистентных к беталактамам штаммов бактерий резистентность проявляется, как отмечалось, на уровне РВРs, т.е. мишени уменьшают сродство к «старым» беталактамам. Поэтому новые природные и полусинтетические беталактамы проверяются на степень сродства к РВРs этих штаммов.
Высокое сродство означает перспективность новых беталактамных структур. Далее, при оценке новых беталактамных структур проверяется их устойчивостьк действию разных беталактамаз -пенициллаз и цефалоспориназ плазмидного и хромосомного происхождения, выделенных из разных бактерий. С этой целью используются большие наборы беталактамаз, обладающих разной субстратной специфичностью. Если большинство используемых беталактамаз не инактивирует новую беталактамную структуру, то она признается перспективной для клиники и заслуживает дальнейшего углубленного изучения.
Таким образом, устойчивость микроорганизмов-патогенов к антибиотикам прежде всего связана с 2-мя причинами – изменением в структуре пенициллин-связывающих белков (РВРs) и наличием бактериальных -лактамаз.
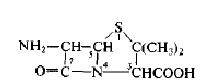
Первые успехи в этом направлении были получены, когда химиками были созданы нечувствительные к распространенным у стафилококков пенициллиназам полусинтетические пенициллины, такие как метициллин и оксациллин, а также нечувствительный к ферменту из синегнойной палочки карбенициллин. Получить эти полусинтетические пенициллины удалось после того, как из бензилпенициллина была выделена 6-аминопенициллановая кислота (6АПК):
условно названная «ядром» молекулы пенициллина. В промышленных условиях 6АПК производят ферментативным гидролизом либо бензилпенициллина (в России), либо феноксиметилпенициллина (за рубежом) с помощью фермента пенициллинацилазы, который осуществляет гидролиз пенициллина по связи СО—NН (между радикалом и ядром) с получением 6АПК.
Сама по себе 6-АПК не активна. Ацилированием 6-АПК были получены указанные антибиотики.
Далее было показано, что наличие метоксигруппы или некоторых других заместителей в 6-положении у пенициллинов и, соответственно, в 7-положении у цефалоспоринов приводит к тому, что многие беталактамазы теряют способность гидролизовать беталактамное кольцо у таких природных или полусинтетических беталактамных антибиотиков как, например, у цефамицина С:

Эффективность беталактамов против грамотрицательных бактерий зависит и от такого фактора, как скорость прохождения через пориновые каналы. Преимущество здесь имеют компактные молекулы, которые проникают и через катионоселективные, и через анионоселективные каналы. Получил, например, практическое применение антибиотик такого рода, как имипенем:

К его ценным свойствам относится также устойчивость к ряду беталактамаз.
Немалой ценностью обладают беталактамные структуры, у которых вводимые в ядро молекулы-заместители создают в ней катионный центр. Такие беталактамы высокоактивны против многих кишечных бактерий по причине катионоселективности пориновых каналов у бактерий, обитающих в кишечном тракте. В качестве примера можно привести структуру молекулы применяемого в клинике беталактама — цефтазидима:
![]()

Отметим, что химические модификации все чаще затрагивают структуру сконденсированного с беталактамом пяти- или шестичленного кольца. Если сера в пятичленном (пенициллины) или шестичленном (цефалоспорины) кольце замещена на кислород или углерод, то соединения называют «нетрадиционные» или «неклассические» беталактамы. К ним относится уже упоминавшийся, быстро проникающий через пориновые каналы имипенем.
Также к «нетрадиционным» относят и такие беталактамы, в которых беталактамное кольцо не сконденсировано с другим кольцом (пяти- или шестичленным). Они получили название «монобактамы», а наибольшую известность приобрел ценный для медицинской практики препарат азтреонам:

Значительный интерес представляют также природные соединения с гаммалактамным, т.е. пятичленным, кольцом, обладающие высокой антибактериальной активностью и широким спектром действия. Их мишенями, как и у беталактамов, являются транспептидазы пептидогликана, т.е. разные РВРк. При контакте с мишенью гаммалактамное кольцо подобно беталактамному расщепляется и происходит ацилирование одного из аминокислотных остатков в активном центре транспептидаз. Беталактамазы могут, как оказалось, инактивировать и гаммалактамы. Однако большая стабильность пятичленного гаммалактамного кольца по сравнению с четырехчленным беталактамным расширяет возможности химического синтеза, т.е. получение синтетических гаммалактамов с пространственной защитой гаммалактамного кольца от беталактамаз.
Ряды получаемых синтетических гаммалактамов быстро растут и некоторые из этих соединений уже проходят предклинические испытания.
